Конгломерат лимфоузлов средостения что это
Опухоли средостения
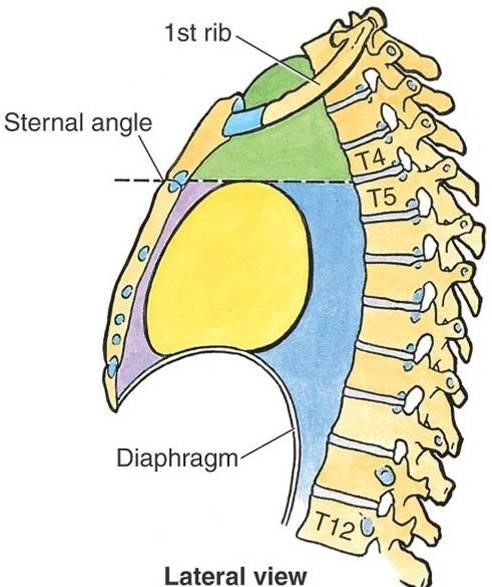
Опухоли средостения, или по-другому медиастинальные опухоли — это новообразования, которые берут свое начало из органов средостения. Средостение – это область, ограниченная легкими по бокам, грудиной спереди и позвоночником сзади. К органам средостения относятся сердце, аорта, пищевод, тимус, трахея, лимфатические узлы, сосуды и нервы.
Кто находится в «зоне риска»?
Медиастинальные опухоли встречаются достаточно редко. Они могут развиваться в любом возрасте и из любых органов и тканей, которые находятся в средостении, однако в большинстве случаев их диагностируют у пациентов от 30 до 50 лет. В детском возрасте чаще встречаются опухоли заднего средостения. Они обычно происходят из нервной ткани и, в большинстве случаев, не злокачественные. У взрослого населения преобладают опухоли переднего средостения – обычно там располагаются лимфомы и тимомы.
Классификация образований средостения
Средостение анатомически делится на 3 зоны. Соответственно этим зонам классифицируются и опухоли средостения.
Клиническая картина
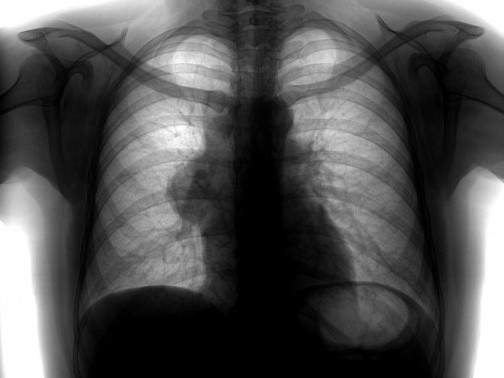
Чаще всего опухоли средостения являются случайной находкой при рентгенологических исследованиях, так как до 40% опухолей клинически не проявляются. Клинические проявления опухоли средостения будут зависеть от следующих факторов:
В зависимости от вышеописанных факторов клиническая картина может быть различной. Самые частые симптомы можно разделить на две группы:
Диагностика
Рентгенологический метод является основным для визуализации новообразования средостения. Компьютерная томография позволяет оценить локализацию опухоли и спланировать дальнейшее обследование.
Без гистологической верификации поставить окончательный диагноз невозможно. При вовлечении в процесс пищевода или трахеи выполняют эндоскопическое исследование для взятия биопсии и визуализации изменений.
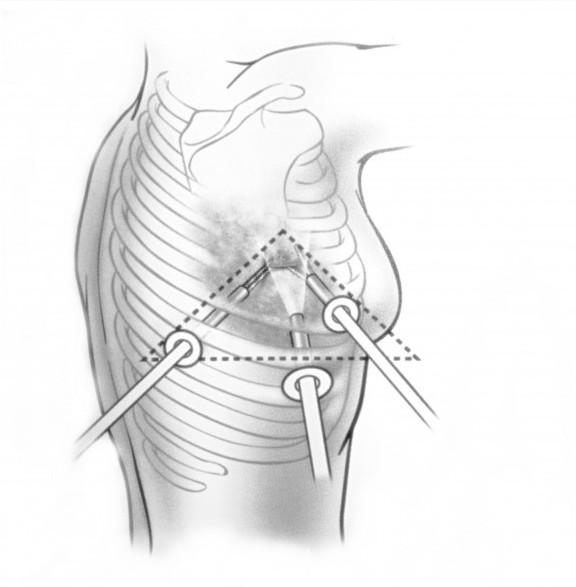
При невозможности получить образец ткани для исследования эндоскопически применяются инвазивные методы: трансторакальная биопсия, медиастиноскопия, видеоторакосокпия. Последние два метода — это серьезные операции, которые проводятся в специализированных медицинских учреждениях.
Лечение
В связи с разнообразием возможных причин медиастинальные опухоли лечатся в зависимости от типа опухоли:
Профилактика и прогнозы
К сожалению, достоверных методов профилактики для опухолей средостения не выявлено. Но результаты можно существенно улучшить, если выявить заболевание на ранней стадии. Если симптомы, описанные ранее не проходят в течение двух недель, возможно стоит обратиться за квалифицированной медицинской помощью. Прогнозы в данном случае трудно давать, они зависят, типа опухоли и ее злокачественности от проводимого лечения.
Список литературы:
1) Клинические рекомендации Ассоциации онкологов России (АОР, 2020)
2) Барболина Т. Д., Бычков М. Б., Аллахвердиев А. К., Борисова Т. Н., Владимирова Л. Ю., Герасимов С. С., Деньгина Н. В., Козлов Н. А., Лактионов К. К., Левченко Е. В., Малютина Д. В., Пикин О. В. Практические рекомендации по лекарственному лечению опухолей вилочковой железы (тимомы и рака тимуса). Злокачественные опухоли: Практические рекомендации RUSSCO #3s2, 2020 (том 10). С. 608-619.
3) Руководство по химиотерапии опухолевых заболеваний/ под ред. Н.И. Переводчиковой, В.А. Горбуновой. – 4-е изд., расширенное и дополненное. – М.: Практическая медицина, 2018.-688с.
4) Рациональная фармакотерапия в онкологии: руководство для практикующих врачей/под.ред. М.И. Давыдова, В.А. Горбуновой. – М.: Литтерра, 2017. – 880с. (Серия «Рациональная фармакотерапия»).
5) Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. Злокачественные новообразования в России в 2018 году. (заболеваемость и смертность) — М.: МНИОИ им. П.А. Герцена филиал ФГБУ «НМИЦ радиологии» Минздрава России, — 2019. –илл.-250с.
6) Пикин О.В. et al. Опухоли средостения: сборник под ред. академика РАН, профессора А.Д. Каприна. М.: Молодая гвардия, 2019. 232 p.
Новообразования средостения
Определение
Средостение — пространство в грудной клетке между легкими, в котором находятся сердце, крупные сосуды, трахея, пищевод, вилочковая железа (тимус), лимфатические узлы.
Новообразования средостения (опухоли и кисты средостения) — это группа разнородных по своему происхождению доброкачественных и злокачественных образований, объединенных общей локализацией и похожими симптомами. Наиболее часто встречающиеся образования средостения — это тимомы, кисты, опухоли нейрогенного происхождения и лимфомы. Саркоидоз, туберкулез, другие заболевания могут вызывать увеличение лимфатических узлов средостения.
Симптомы новообразований средостения
Симптомы зависят от локализации, размера и природы образования. Часто заболевание протекает бессимптомно, и новообразование средостения является случайной находкой при рентгенографическом исследовании или компьютерной томографии грудной клетки. Например, при опухолях тимуса, называемых тимомами, симптомов может не быть совсем, а может развиться нервно-мышечное заболевание – миастения.
Могут появляться общие — неспецифические симптомы – слабость, недомогание, похудание, небольшое повышение температуры тела. Может отмечаться боль в грудной клетке.
Существуют симптомы, связанные со сдавлением опухолью соседних органов. Например, при сдавлении верхней полой вены появляются одутловатость лица, головная боль, одышка в горизонтальном положении. Больные не могут выполнять работу, связанную с наклонами вперед.
При сдавлении трахеи наблюдаются кашель, одышка, шумное, затрудненное дыхание; при сдавлении пищевода — затруднение глотания.
Диагностика
Компьютерная томография выполняется всем пациентам с новообразованиями средостения и позволяет точно определить их размер, локализацию и соотношение с другими органами и тканями, а значит и возможность хирургического лечения образования. Иногда для повышения точности изображения и оценки взаиморасположения с другими органами и тканями применяют введение рентгеноконтрастных веществ. Используются также Ангио-КТ, МРТ, УЗИ.
Иногда для выяснения природы новообразования и, соответственно, определения лечебной тактики необходимо получить участок ткани для гистологического исследования. Мы не сторонники игловой биопсии операбильных опухолей. Такая процедура практически никогда не отменяет необходимости хирургического лечения, а значит бесполезна.
С другой стороны, при неудалимых опухолях следует получить материал для гистологического исследования наименее травматичным способом:
Лечение
Основным методом лечения новообразований средостения является хирургический. Вид операции зависит от локализации и размера опухоли. Когда это возможно, мы выполняем операции через небольшие разрезы (видеоассистированные или торакоскопические операции). Такие вмешательства значительно менее травматичны и существенно сокращают сроки выздоровления и пребывания больного в стационаре. Руководитель Центра торакальной службы, Пищик Вадим Григорьевич, является признанным европейским экспертом по лечению новообразований средостения, особенно торакоскопическим способом. Этому вопросу посвящена его докторская диссертация.
Лимфомы и герминогенные опухоли не требуют операции и хорошо поддаются химио-лучевой терапии.
Запись на консультацию и осмотр по телефону: +7 (921) 919-07-49
Диагностика лимфаденопатий
Общая информация
Краткое описание
Национальное гематологическое общество
НАЦИОНАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ДИАГНОСТИКЕ ЛИМФАДЕНОПАТИЙ
2018
Анализ публикаций отечественных [1—5,8] и зарубежных [12—14] авторов, посвященных алгоритмам диагностики ЛАП, а также многолетний опыт работы «НМИЦ гематологии» [5] позволили разработать и внедрить протокол дифференциальной диагностики лимфаденопатий [15—17].
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
Эпидемиология
Диагностика
Первый этап заключается в сборе жалоб, данных анамнеза жизни и анамнеза заболевания, эпидемиологического анамнеза и физикального исследования (рис.1) (II A).
Рисунок 1. Алгоритм первичной диагностики пациентов с ЛАП 
Жалобы и анамнез:
Таблица 1. Эпидемиологические данные, профессиональные факторы, важные в диагностике лимфаденопатий. 
Таблица 3. Географическое распространение основных эндемичных инфекционных заболеваний, сопровождающихся лимфаденопатией.
Таблица 4. Локализация лимфатических узлов, зоны дренирования лимфы и наиболее частые причины увеличения. 

Таблица 5. Значение клинических признаков при лимфаденопатии. 

Уровень убедительности рекомендаций В (уровень достоверности доказательств – IIВ).
Уровень убедительности рекомендаций В (уровень достоверности доказательств – II).
3. Правила выбора лимфатического узла и выполнения его биопсии:

Алгоритм дифференциальной диагностики после проведения биопсии лимфатического узла представлен на рисунке 2 и основан на выявленных морфологических изменениях. В случаях с морфологической картиной опухолевого поражения (лимфома или нелимфоидная опухоль) проводиться ряд дополнительных исследований (иммуногистохимическое и/или молекулярно-генетическое исследование) для уточнения нозологической формы согласно ВОЗ классификации. При отсутствии опухолевого поражения, устанавливается гистологический вариант ЛАП согласно дифференциально-диагностическим группам (таблица 6), в зависимости от которого проводятся/непроводятся дополнительные исследования – повторный сбор жалоб, данных анамнеза жизни, заболевания, объективного осмотра, лабораторное и инструментальное исследования (рисунок 2).
Рисунок 2. Алгоритм постбиопсийной диагностики ЛАП 
Лечение
Вид терапии зависит от окончательного диагноза, установленного после обследования, единого стандарта лечения лимфаденопатии не существует. Проводить консервативное лечение следует в случае доказанной неопухолевой природы ЛАП:
Уровень убедительности рекомендаций В (уровень достоверности доказательств – III).
Медицинская реабилитация
Профилактика
Информация
Источники и литература
Информация
Они предназначены для врачей-гематологов, онкологов, терапевтов, инфекционистов, хирургов, педиатров, работающих в амбулаторно-поликлинических условиях, организаторов здравоохранения.
Поспелова Татьяна Ивановна, д.м.н., профессор, заведующая кафедрой терапии, гематологии и трансфузиологии Федерального государственного бюджетного образовательного учреждения высшего образования «Новосибирский государственный медицинский университет» Министерства здравоохранения Российской Федерации.
Конгломерат лимфоузлов средостения что это
Давыдов М.И., Полоцкий Б.Е., Мачаладзе З.О., Тюляндин С.А., Карселадзе А.И., Савелов Н.А., Ахмедов Б.Б. (РОНЦ им. Н.Н.Блохина)
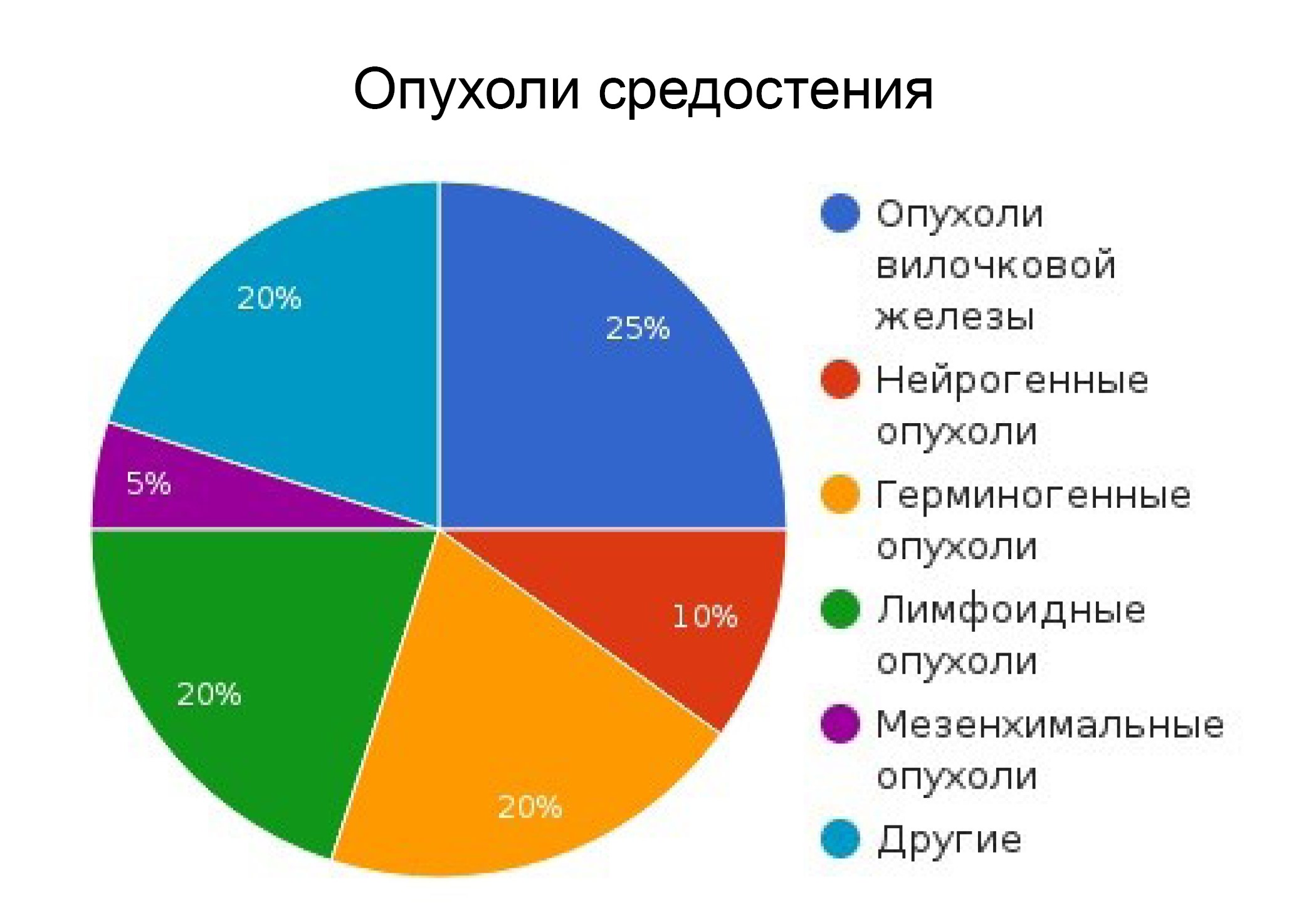
В материалах РОНЦ им. Н.Н.Блохина 1980-2005 гг. отражен опыт диагностики, хирургического и комбинированного лечения свыше 500 больных. Среди анализированных случаев – опухоли органов и тканей собственно средостения: вилочковой железы (16,9%), нейрогенные (17,7%) и мезенхимальные (10,4%) опухоли; новообразования из тканей, дистопированных в средостение (внегонадные герминогенные опухоли, тератомы, дермоидные кисты) – 22,7%, а также – процессы с изолированным поражением лимфатических узлов средостения: лимфомы Ходжкина и неходжкинске лимфомы (25,7%), случаи саркоидоза Бека (29), ангиофолликулярной гиперплазии (4) и др.
Обобщение опыта, накопленного, в особенности, в 1990-х – 2000-х гг., с учетом современных возможностей клинической онкологии, позволило оптимизировать уточняющую диагностику, обосновать расширение показаний к хирургическому и комбинированному лечению, повторным и паллиативным операциям. Результаты операций по поводу новообразований средостения, прежде всего при массивных опхолевых поражениях, сопряженных со сдавлением дыхательных путей, пищевода, магистральных сосудов (при условии должного реанимационно-анестезиологического обеспечения) характеризуются сравнительно низкой летальностью, улучшением качества жизни и увеличением ее продолжительности.
ОБЩИЕ ПОЛОЖЕНИЯ (КЛИНИКА, ДИАГНОСТИКА, ЛЕЧЕНИЕ. )
Материалы РОНЦ подтверждают известные сведения о локализации и преимущественно злокачественном характере опухолей осредостения. Соотношение злокачественных и доброкачественных новообразований составило 3:1. Тимомы, лимфомы, внегонадные герминогенные опухоли (ВГО), мезенхимомы локализовались в переднем средостении, нейрогенные опухоли – в заднем; несоответствие локализации и структуры новообразования отмечено у 15% больных нейрогенными опухолями – в тех случаях, когда новообразования локализовалась в переднем средостении. Определение исходной локализации процесса было затруднено при «гигантских» опухолях, когда (в 10-20% случаев) наблюдались поражения как переднего, так и заднего средостения с распространением процесса на б?льшую часть гемиторакса.
Длительность клинических проявлений составляла от нескольких месяцев до 3 лет. При небольших опухолях, не связанных с прилежащими анатомическими образованиями не отмечалось клинических проявлений (до 30-40% случаев). В остальных наблюдениях регистрировались проявления, обусловленные наличием опухоли – миастения (5%), осиплость (часто сопряженная с ВГО), медиастинальный компрессионный синдром (до 30-40% случаев, в особенности при злокачественных процессах); а также различные неспецифические симптомы (повышение температуры тела, кашель, боли и чувство сдавления за грудиной, др.). Рентгенологическое исследование, безусловно, позволяло определять локализацию и размеры опухоли. Для уточнения топографии новообразований, выявления связей с прилежащими анатомическими образованиями применялись КТ и МРТ. Чувствительность. специфичность и точность * этих методов соответствовали 90-80%, достигая 97-98% значимости оценки – как например, МРТ в диагностике распространенности тимом. Повышение уровня опухолевых маркеров сыворотки крови (АФП и ХГЧ) наблюдалось при несеминомных герминогенных опухолях средостения. Морфологическое подтверждение диагноза, кроме пункционной биопсии (информативность, при лимфопролиферативных заболеваниях, соответствует 48%), достигалось хирургическими методами диагностики. При этом, вместо медиастиноскопии и парастернальной медиастинотомии (16 и 43 исследования 1990-х гг.) в 2000-х гг. стала применяться видеоторакоскопия (53 исследования).
Следует отметить, что современные возможности диагностики позволяют устанавливать морфологический диагноз во всех случаях лимфопролиферативных заболеваний с поражением средостения. При этом, агрессивность применяемых методов лечения вынуждает считать недопустимой попытку лечения при данных новообразоованиях без морфологического диагноза.
Хирургический метод – основа лечения больных опухолями средостения. Исключения составляют злокачественные внегонадные герминогенные и лимфопролиферативные заболевания основу лечения которых составляют консервативные методы лечения. Учитывая низкую эффективность химио-лучевой терапии в отношении остальных медиастинальных новообразований хирургическое лечение, в том числе и с паллиативной целью, с выполнением повторных операций, способствует существенному продлению жизни. Выполнение боковой торакотомии в 73% случаев обеспечивало возможность удаления опухоли. Локализация процесса, безусловно, определяла особенности хирургического доступа. Так, при нейрогенных опухолях, растущих в форме «песочных часов» торакотомия дополнялась одномоментной ляминэктомией для радикального удаления внутригрудной и внутрипозвоночной частей опухоли – по N.Guleke (1916) в модификации H.Grillo et al. (1983). Для удаления местнораспространенных и «гигантских» опухолей выполнялась двусторонняя торакотомия, полная продольная стернотомия (4), иные комбинированные доступы.
ОСОБЕННОСТИ, ОБУСЛОВЛЕННЫЕ ЛОКАЛИЗАЦИЕЙ НОВООБРАЗОВАНИЙ
Опухоли вилочковой железы. Из 85 наблюдений в 44,7% случаев диагностированы доброкачественные новообразования, в 55,3% – злокачественные. Клиническое течение заболевания не всегда определялось гистологическим строением опухоли и характером её роста. Оперированы 70 (82,4%) больных; остальным проведено консервативное лечение из-за распространенности опухолевого процесса.
Радикальные операции составили 59 (84,3%) случаев; у остальных пациентов удаление опухоли выполнено с паллиативной целью, у 6 (8,6%) операция ограничена эксплоративной торакотомией. Адекватным объемом оперативного вмешательства при новообразованиях вилочковой железы является тимомэктомия – удаление опухоли и всей ткани вилочковой железы с жировой клетчаткой и лимфоузлами переднего средостения. Такой объем операции выполнен 44 больным. Кроме того, 15 пациентам выполнены расширенно-комбинированные тимомэктомии в связи с инвазией опухолей в окружающие структуры. Дополнительная лучевая и химиотерапия проведена в 19,2% случаев (в основном – при III-IV стадиях тимом типов В2, В3 и С). Отдаленные результаты хирургического лечения. Более 3 лет после радикального хирургического лечения прожили 84,8%, более 5 лет – 82,6% и более 10 лет – 73,9% больных. Отдаленные результаты определялись распространенностью процесса (инвазия капсулы, поражение плевры), гистологическим типом опухоли. Так, тимомы типов А и В1 прогностически наиболее благоприятны (10-летний срок переживают 90% пациентов). Для тимом типов АВ, В2 и В3 5-летняя выживаемость соответствовала 64-68%; прогноз при тимомах типа С достоверно хуже – 32%. При отсутствии инвазивного роста гистологическая форма тимомы не влияет на отдаленные результаты хирургического лечения. Тимомы с инвазией в пределах капсулы являются злокачественными по клиническому течению и требуют назначения послеоперационного лучевого лечения.
Нейрогенные опухоли (89 случаев) распределены в две гистогенетические группы: новообразования из клеток нервной ткани (22; 24,7%) и из оболочек периферических нервов (67; 75,3%). Доброкачественные опухоли (шванномы, нейрофибромы, ганглионевромы, параганглиомы) выявлены у 69,7%, злокачественные (саркомы Юинга, нейробластомы, ганглионейробластомы, др.) – у 30,3% пациентов. Решение лечебных задач определялось характерной локализацией нейрогенных опухолей и особенностями их распространения.
Оперированы (большинство из них – радикально) 86 (96,6%) пациентов. Радикальные операции в основном выполнены при доброкачественных нейрогенных опухолях; при злокачественных новообразованиях радикальные хирургические вмешательства составили 54,2%, паллиативные – 45,8%. Типичный вариант операции, в объеме удаления опухоли средостения, осуществлен в 81,4%, комбинированный – в 18,6% случаев. При злокачественных опухолях это соотношение составило 62,5 и 37,5% соответственнои 7 больных), а комбинированные рогенными опухолями средостения типичные опурации выполнены. Проведение послеоперационной лучевой или химиотерапии показано при сомнении в радикализме операции, выявлении значительной распространенности опухоли. Назначение дополнительной лучевой или химиотерапии обосновывается сведениями о патоморфозе опухолей и наблюдениях опухолевой регрессии. Частота рецидивов после радикальных операций соответствовала 4,8%. Продолженный рост опухоли после паллиативных операций в 72,8% случаев выявлялся уже в конце первого года наблюдения. В связи с этим, очевидна целесообразность повторных (и многократных) хирургических вмешательств по поводу рецидивов нейрогенных медиастинальных опухолей – лишь хирургический метод позволяет добиться продления жизни, устранения тягостных местных проявлений заболевания. Общая 3-5-летняя выживаемость после повторных операций составила 70,8-38,6%, сравнительно с 25,0-12,5% среди больных, леченных консервативно.
Мезенхимальные опухоли (52 наблюдения) представлены различными гистологическими формами: сосудистые опухоли – 17 (32,6%); жировые – 15 (28,8%); фибробластические – 6 (11,5%), фиброгистиоцитарные – 2 (3,8%); костно-хрящевые – 5 (9,6%); мезенхимомы – 2 (2,8%), а также опухоль из скелетных мышц – 1 (1,9%); синовиальная саркома – 1 (1,9%); саркомы неясного генеза – 3 (5,8%). Доброкачественные опухоли составили 42,3%, злокачественные – 57,7% случаев. Лечение больных мезенхимальными опухолями, в особенности – злокачественными, в условиях низкой эффективности химиолучевой терапии, является только хирургическим. Оперативные вмешательства отличаются большой сложностью, что обусловлено, как правило, распространенностью процесса. Хирургическое лечение проведено 40 пациентам, консервативное – 12. В плане дополнительного лечения только 7 больным проведена пред- или послеоперационная химиолучевая терапия. После хирургического лечения в группе из 19 больных злокачественными новообразованиями рецидивы выявлены в 13 случаях (68,4%) – в том числе, в 9 из 11 паллиативных и в 4 из 8 радикальных операций (81,8 и 50% соответственно). По поводу рецидивов выполнялись повторные операции, один из больных оперирован трижды, другой – четырежды. Показатели общей и безрецидивной 5-летней выживаемости при доброкачественных мезенхимальных опухолях стремятся к 100%. При злокачественных – 1-3-5-летняя продолжительность жизни составила 75; 62,5; 48,6% после радикальных операций и 63,6; 27,2; 18,1% – после паллиативных.
Таким образом, даже при распространенном опухолевом процессе и при локорегиональных рецидивах должна применяться активная хирургическая тактика. Повторные (и многократные) операции, в том числе и с паллиативной целью, позволяют вновь добиться продления жизни. Присущий мезенхимальным опухолям агрессивный местный рост и склонность к рецидивам обосновывают целесообразность дальнейшего поиска вариантов комбинированного лечения, с применением неоадъювантной или адъювантной химиолучевой терапии. Каждую составляющую лечения следует использовать в полном объеме, постоянно развивая и совершенствуя.
Внегонадные герминогенные опухоли (ВГО). Наблюдались 114 пациентов с внегонадными герминогенными опухолями средостения: мужчин – 97 (85,1%), женщин – 17 (14,9%) в возрасте от 14 до 72 лет, средний возраст – 26 лет. Семинома диагностирована в 17,5%, несеминома – в 82,5% случаев. Среди больных несеминомными ВГО был выявлен эмбриональный рак, опухоли желточного мешка, хориокарциномы, тератомы различной степени зрелости, дермоидные кисты. Общие принципы диагностики и лечения. При повышении уровня опухолевых маркеров (АФП, ХГ, ЛДГ) без признаков поражения яичек необходима компьютерная томография органов грудной клетки, брюшной полости и забрюшинного пространства. При морфологическом подтверждении диагноза злокачественной внутригрудной герминогенной опухоли показано проведение 4-6 курсов химиотерапии (схемы ВЕР, ВР, др), лучевой терапии (РОД= 2-3 Гр; СОД – до 60-70 Гр). Полный эффект лечения больных внегонадными семиномами регистрируется в 80%, несеминомами – в 23% случаев. Частота рецидивов выше в группе внегонадных несеминомных опухолей (6,7 и 29,4%; р