Концентрическое ремоделирование стенок лж что это
Концентрическое ремоделирование левого желудочка: что это такое
Что такое концентрическое ремоделирование левого желудочка
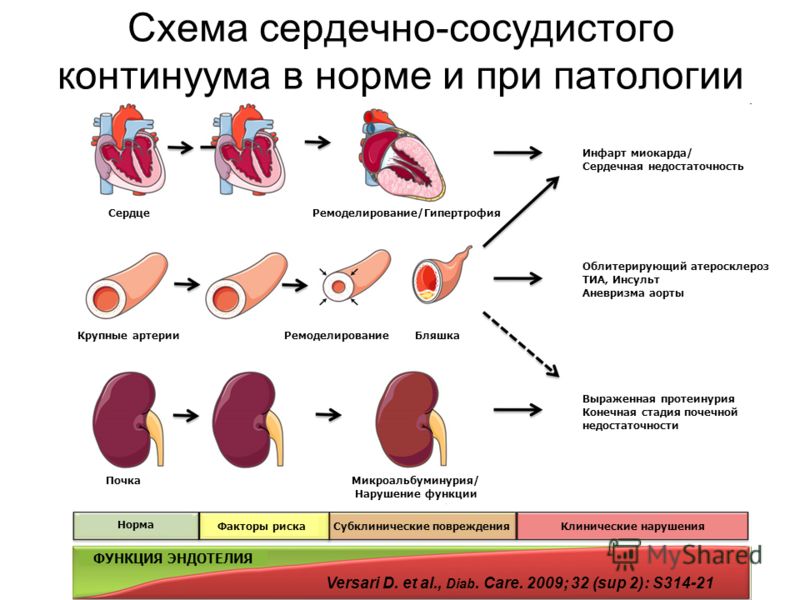
Концентрическое ремоделирование миокарда левого желудочка считается наиболее распространенной формой данной болезни. Как правило, оно развивается в первую очередь у людей, имеющих артериальную гипертензию. Данный тип не имеет способности изменять внутреннее пространство левого желудочка, происходит лишь изменение стенок сердца и увеличение перегородки между сердечными отделами. Стоит сказать, что эта форма может начать свое развитие на фоне имеющейся гипертрофии левого желудочка. Кстати, гипертрофия, как правило, развивается при увеличенных физических нагрузках, либо же, как следствие гипертонии. Помимо стандартных причин возникновения, имеются и другие, которые не лучшим образом влияют на здоровье человека, а это могут быть пагубные привычки, такие как курение, злоупотребление алкоголем и др.
Начинается заболевание с гипертрофии левого желудочка и проявляется повышением толщины его стенки
Важно знать, что самостоятельная диагностика ремоделирования миокарда не приведет ни к чему хорошему, но, все-таки следует разбираться в первоначальных признаках, которые способствуют возникновению болезни, это такие, как:
При первых же проявлениях подобных симптомов необходимо обратиться к специалисту, который должен назначить кардиограмму. Только этот метод исследования поможет определить наличие данной болезни. Следует сказать, что запущенная форма может привести к необратимым последствиям, например, к развитию хронической сердечной недостаточности.
Ремоделирование сердца
Нет ничего сложнее, нежели перенести тяжелую болезнь сердца, которая приводит также к определенным последствиям. Одной из таковых является ремоделирование сердца. Ремоделирование сердца — это структурные изменения органа, разрушающие его свойства в ответ на внешние воздействия и другие патологические процессы в организме человека.
Ремоделирование сердца проишодит под воздействием негативных факторов и заболеваний
Причины возникновения
Необходимо уточнить, что данный недуг может развиваться и на почве других сердечных заболеваний, это и приводит к особенным формам развития. Помимо таких негативных факторов, как болезни, ремоделирование миокарда может проявиться и как следствие некачественного лечения. Важно знать, что абсолютно разные причины влияют на развитие той или иной физиологической особенности сердца. О важности правильного диагностирования причин возникновения говорить не стоит, ведь это и так понятно, что следует в первую очередь обращать внимание на фактор, который способствовал возникновению данного анатомического изменения.
Вследствие повышенного артериального давления возникают некоторые болезни, которые приводят к данным изменениям. Помимо этих деформаций сердца, можно также наблюдать и другие нарушения:
Большое значение имеет масштабность ремоделирования миокарда, которое имеет разные значения и объясняется двумя основными причинами возникновения:
| активация нейрогормонов | Подобный случай возникает в результате поражения организма инфарктом миокарда. Стоит сказать, что данная активация обусловлена значительным повреждением сердечной мышцы. Кстати, данная повышенная активация должна работать над регулированием общей работы сердечного органа и нормализацией артериального давления. Но, если не принять вовремя меры предосторожности, то такая патология перерастает в более тяжелую форму ремоделирования миокарда |
| симпатическая нервная система и ее активация | Данная причина возникновения основного недуга объясняется увеличенным напряжением левого желудочка. Это приводит к тому, что данному отделу необходимо большее количество кислорода |
Если говорить об эксцентрическом ремоделировании миокарда, то оно может быть вызвано значительной перегрузкой данной мышечной ткани. Кроме того, это сопровождается удлинением одноядерных клеток и уменьшением в размерах стенок сердца.
Патофизиология болезни
Сегодня инфаркт миокарда звучит не так страшно, как несколько лет назад. В большинстве случаев пациенты имеют возможность продолжать свою стандартную жизнедеятельность, несмотря на перенесенный стресс для сердца, да и всего организма. Стоит сказать, что качественное лечение и хорошая реабилитация, дают свои плоды, но, к сожалению, помимо этого, все же остаются последствия перенесенного инфаркта. Ремоделирование миокарда патофизиология которого только обостряется, имеет достаточно неприятные последствия. В данном случае, если своевременно не проводить квалифицированные осмотры, можно придать свой организм осложнениям, таким как плохое кровообращение и хроническая сердечная недостаточность.
Инфаркт миокарда, как правило, приводит к серьезным физиологическим изменениям левого желудочка, что не очень хорошо сказывается на общем состоянии пациента. Такое изменение структуры сердечного отдела приводит также к следующим изменениям:
Если проследить данную особенность, то можно заметить, что все процессы в организме взаимосвязаны, и ничего не возникает просто так. Из-за того что постоянно повышается артериальное давление, наша сердечная мышца пытается приспособиться к данному явлению. Как следствие, происходит изменение в размерах мышечной ткани. Именно так возникает данное заболевание, которое сопровождается рядом других недугов.
Концентрическое ремоделирование стенок лж что это
а) Патогенез. Концентрическая гипертрофия левого желудочка или его дилатация. При аортальном стенозе левый желудочек реагирует на перегрузку давлением развитием концентрической гипертрофии, направленной на поддержание постоянного напряжения желудочковой стенки (закон Лапласа). Однако реакция желудочка на перегрузку давлением не у всех больных проявляется развитием гипертрофии. Так, существуют отчетливые половые различия: у женщин аортальный стеноз значительно чаще приводит к гипертрофии миокарда левого желудочка, чем у мужчин (81% против 54%).
Если хроническая постнагрузка не сопровождается адекватной гипертрофией левого желудочка, направленной на компенсацию повышенного напряжения его стенки, то происходит расширение его полости и глобальное снижение сократительной функции [феномен «несоответствия постнагрузке» (англ, «afterload mismatch»)]. Такая форма ремоделирования при аортальном стенозе у мужчин наблюдается чаще, чем у женщин. Снижение фракции выброса левого желудочка сопровождается уменьшением потока крови через аортальный клапан вследствие снижения градиента давления на аортальном клапане.
Даже если сократимость левого желудочка не нарушена и фракция выброса еще нормальная, то уже на ранней стадии заболевания вследствие увеличения постнагрузки и гипертрофии левого желудочка развивается диастолическая дисфункция и снижается мощность систолического выброса.
б) Значение эхокардиографии:
1. Стадии ремоделирования левого желудочка. Важными задачами эхокардиографического исследования у больных аортальным стенозом являются определение стадии ремоделирования левого желудочка и количественная оценка такой геометрической перестройки. Особенно важна своевременная диагностика сниженной систолической функции левого желудочка, так как у больных с высокой степенью аортального стеноза и сниженной сократительной функцией прогноз неблагоприятный, даже при отсутствии клинических проявлений, что делает целесообразным протезирование аортального клапана.
2. Фракция выброса левого желудочка (LVEF). Выполняя ЭхоКГ, следует дать как количественную, так и качественную оценку систолической функции левого желудочка в целом. Для количественной оценки наряду с определением фракции укорочения при ЭхоКГ в М-режиме следует определить также фракцию выброса левого желудочка по Симпсону.
Редактор: Искандер Милевски. Дата публикации: 5.1.2020
Опубликовано в журнале:
Резюме
Проведено ультразвуковое и ангиографическое обследование 75 больных с диагнозами миокардита, подтвержденного данными патоморфологического исследования биоптатов, полученных с помощью прижизненной эндомиокардиальной биопсии.
Установлено, что ремоделирование миокарда является ключевым звеном в патогенезе развития недостаточности кровообращения при миокардите. Данный процесс характеризуется первоначальным поражением левого желудочка с последующим вовлечением правых отделов сердца. Признаки ремоделирования миокарда (изменение геометрии сердца, преобладание дилатации над гипертрофией миокарда) возникают на начальных стадиях миокардита и прогрессируют на стадии хронического воспаления.
Ключевые слова: миокардит, недостаточность кровообращения, ремоделирование миокарда.
Одним из осложнений многих заболеваний сердечно-сосудистой системы является сердечная недостаточность. Несмотря на снижение смертности от сердечно-сосудистых заболеваний (ССЗ) в развитых странах, в настоящее время отмечается стойкая тенденция к увеличению показателей смертности от недостаточности крообращения (НК).
Материал и методы исследования
Результаты исследования
Таблица 1
Показатели центральной гемодинамики у больных миокардитом с НК (М+/-m)
Изучение показателей ренин-ангиотензин-альдостероновой системы у исследуемых больных продемонстрировало, что при остром миокардите активность ренина была меньше, чем при хроническом (1,7+/-0,1 нг/мл/час и 2,0+/-0,1 нг/мл/час, р 0,05).
Обсуждение
Поражение мышцы сердца при миокардите происходит, чаще всего, вследствие токсического воздействия вирусного агента. При этом происходит не только гибель кардиомиоцитов [1], но и такие явления, как ускорение апоптоза [5], активизация фагоцитарной функции лейкоцитов, макрофагов с выделением цитотоксина TNFcc [3], являющегося одним из факторов с негативным инотропным эффектом и способностью стимулировать гипертрофию кардиомиоцитов. Одновременно, при миокардите в биоптатах обнаруживается повышенный уровень энзима конверсии ангиотензина и ангиотензина II, который обладает вазоконстриктивным эффектом и стимулирует развитие коллагена [8]. Микротромбоз, обнаруживаемый в капиллярном русле, приводит к диффузной ишемии миокарда. Весь этот комплекс изменений вызывает прогрессирующую дилатацию сердца, ведет к систолической и диастолической дисфункции, ухудшению насосной функции сердца. Появление и прогрессирование сердечной недостаточности при миокардите, как продемонстрировано и в нашем исследовании, сопровождается изменением конфигурации сердца, которая становится более сферичной. Ранее аналогичные данные были получены при изучении процессов ремоделирования сердца у больных с постинфарктным кардиосклерозом [9]. При этом, несмотря на прогрессирующее увеличение массы миокарда, процессы дилатации преобладают над процессами гипертрофии. Ремоделирование миокарда является бивентрикулярным процессом, паралельно вовлекающим левый и правый желудочки с едиными патофизиологическими механизмами.
Как видно из полученных данных, можно заключить, что, в основном, ремоделирование миокарда, а не сократительная дисфункция мышцы сердца, является ключевым фактором развития хронической сердечной недостаточности. При этом, первые признаки ремоделирования возникают на этапе первичного поражения миокарда. Другие звенья прогрессирующей сердечной недостаточности (активизация нейрогуморальной системы, вазоконстрикция) возникают уже при хронизации воспалительного процесса на стадии выраженного нарушения диастолической и систолической функции миокарда.
Заключение
1. Первичное повреждение миокарда приводит к нарушению сократительной функции миокарда с включением всех патофизиологических механизмов развития сердечной недостаточности.
2. Ремоделирование миокарда является ключевым звеном в патогенезе развития недостаточности кровообращения при миокардите и характеризуется поражением левого желудочка с последующем вовлечением в процесс правых отделов сердца.
3. Изменение формы сердца от эллипсоидной к более сферичной сопровождается преобладанием дилатации над гипертрофией миокарда. Признаки ремоделирования миокарда возникают уже на начальных этапах воспалительного процесса и усугубляются на хронической стадии миокардита.
ЛИТЕРАТУРА
1. Anversa P., Kajstura J., Olivetti G. Myocyte death in heart failure. // Current opinion in Cardiology, 1996, №11, p. 245-251.
Abstract
We have studied 75 patients with a verified pathologically (by means of endomyocardial biopsy) myocarditis with the usage of ultrasound and angiography.
We have found myocardial remodeling to be the key process in the development of heart failure in myocarditis. The process is characterized by the initial involvement of the left ventricle with the later influence upon the right heart. Remodeling patterns (altered heart geometry, dilation dominating over myocardial hypertrophy) are assessable on the early stages and an subject to further progress.
Key words: myocarditis, heart failure, myocardial remodeling.
Лечение гипертрофической кардиомиопатии
Гипертрофическая кардиомиопатия (ГКМП) – это генетически обусловленное заболевание миокарда, проявляющееся комплексом специфических морфо-функциональных изменений
Лечение гипертрофической кардиомиопатии
Гипертрофическая кардиомиопатия (ГКМП) – это генетически обусловленное заболевание миокарда, проявляющееся комплексом специфических морфо-функциональных изменений и постепенно прогрессирующим течением с высоким риском развития жизнеугрожающих аритмий и внезапной смерти.
Типичными являются морфологические изменения: аномалия архитектоники сократительных элементов миокарда (гипертрофия и дезориентация мышечных волокон), развитие фибротических изменений мышцы сердца, патология мелких интрамиокардиальных сосудов.
При ГКМП происходит массивная гипертрофия миокарда левого (и реже правого желудочка), чаще асимметричного характера за счет утолщения межжелудочковой перегородки, часто с развитием обструкции выходного тракта левого желудочка (ЛЖ) при отсутствии каких-либо явных причин.
Общепризнанной является представление о преимущественно наследственной природе ГКМП. В связи с этим, широкое распространение получил термин «семейная гипертрофическая кардиомиопатия». К настоящему времени установлено, что более половины всех случаев заболевания являются наследуемыми, при этом основной тип наследования – аутосомно-доминантный. Оставшиеся приходятся на так называемую спорадическую форму; в этом случае у пациента нет родственников, болеющих ГКМП или имеющих гипертрофию миокарда. Считается, что большинство, если не все случаи спорадической ГКМП, также имеют генетическую причину, т. е. вызваны случайными мутациями.
Гипертрофическая кардиомиопатия – это генетически гетерогенное заболевание, причиной которого являются более 200 описанных мутаций нескольких генов, кодирующих белки миофибриллярного аппарата. К настоящему времени известны 10 белковых компонентов сердечного саркомера, выполняющих контрактильную, структурную или регуляторную функции, дефекты которых наблюдаются при ГКМП. Причем в каждом гене множество мутаций могут становиться причиной заболевания (полигенное мультиаллельное заболевание).
Наличие той или иной ассоциированной с ГКМП мутации признается «золотым» стандартом диагностики заболевания. При этом описанные генетические дефекты характеризуются разной степенью пенетрантности, выраженностью морфологических и клинических проявлений. Тяжесть клинической картины зависит от присутствия и степени гипертрофии.
Таким образом, ГКМП характеризуется крайней гетерогенностью вызывающих ее причин, морфологических, гемодинамических и клинических проявлений, разнообразием вариантов течения и прогноза, что существенно затрудняет выбор адекватных и наиболее эффективных лечебных подходов по контролю и коррекции имеющихся нарушений.
Возможны три гемодинамических варианта обструктивной ГКМП:
Cимптомы болезни разнообразны и малоспецифичны, связаны с гемодинамическими нарушениями (диастолическая дисфункция, динамическая обструкция путей оттока, митральная регургитация), ишемией миокарда, патологией вегетативной регуляции кровообращения и нарушением электрофизиологических процессов в сердце. Диапазон клинических проявлений крайне велик: от бессимптомных до неуклонно прогрессирующих и трудно поддающихся медикаментозному лечению форм, сопровождающихся тяжелой симптоматикой.
Повышение диастолического давления в левом желудочке из-за диастолической дисфункции, динамическая обструкция выносящего тракта левого желудочка проявляются одышкой в покое и при физической нагрузке, утомляемости, слабости. Нарастание давления в малом круге кровообращения сопровождается развитием острой левожелудочковой недостаточности (чаще в ночные часы – сердечная астма, альвеолярный отек легких).
Падение фракции выброса при физической нагрузке или нарушениях сердечного ритма сопровождается ухудшением кровообращения головного мозга. Преходящая ишемия мозговых структур проявляется кратковременной потерей сознания (обморок) или предобморочными состояниями (внезапная слабость, головокружение, потемнение в глазах, шум и «заложенность» в ушах).
Методы исследования:
ЭХО-КГ – основной метод диагностики ГКМП. Критериями диагностики ГКМП на основании данных ЭХО-КГ являются:
Если в покое обструкции выносящего тракта левого желудочка нет, ее можно спровоцировать медикаментозными (ингаляция амилнитрита, введение изопреналина, добутамина) или функциональными пробами (проба Вальсальвы, физическая нагрузка), которые уменьшают преднагрузку или повышают сократимость левого желудочка.
Катетеризация сердца и коронарная ангиография проводятся для оценки коронарного русла перед миоэктомией или операцией на митральном клапане, а также чтобы выяснить причину ишемии миокарда. При этом к характерным признакам ГКМП относят:
Сцинтиграфия миокарда и позитронно-эмиссионная томография
При гипертрофической кардиомиопатии сцинтиграфия миокарда имеет некоторые особенности, однако в целом ее значение в диагностике ишемии такое же, как и обычно. Стойкие дефекты накопления указывают на рубцовые изменения после инфаркта миокарда, обычно они сопровождаются снижением функции левого желудочка и плохой переносимостью физической нагрузки. Обратимые дефекты накопления указывают на ишемию, вызванную снижением коронарного резерва при нормальных артериях или коронарным атеросклерозом. Обратимые дефекты часто никак не проявляются, однако, по-видимому, они повышают риск внезапной смерти, особенно у молодых больных с гипертрофической кардиомиопатией. При изотопной вентрикулографии можно выявить замедленное наполнение левого желудочка и удлинение периода изоволюмического расслабления.
Позитронно-эмиссионная томография – более чувствительный метод, кроме того, она позволяет учесть и устранить помехи, связанные с затуханием сигнала. Позитронно-эмиссионная томография с фтордезоксиглюкозой подтверждает наличие субэндокарлиальной ишемии, вызванной снижением коронарного резерва.
Современные подходы к лечению ГКМП
По современным представлениям, лечебная стратегия определяется в процессе разделения больных на категории в зависимости от описанных выше вариантов течения и прогноза.
Все лица с ГКМП, включая носителей патологических мутаций без фенотипических проявлений болезни и пациентов с бессимптомным течением заболевания, нуждаются в динамическом наблюдении, в ходе которого оцениваются характер и выраженность морфологических и гемодинамических нарушений. Особое значение имеет выявление факторов, определяющих неблагоприятный прогноз и повышенный риск внезапной смерти (в частности, скрытых, прогностически значимых аритмий).
Общие мероприятия
Ограничение значительных физических нагрузок и запрещение занятий спортом, способных вызывать усугубление гипертрофии миокарда, повышение внутрижелудочкового градиента давления и риска внезапной смерти.
Медикаментозное лечение
До настоящего времени окончательно не решен вопрос о необходимости проведения активной медикаментозной терапии у наиболее многочисленной группы больных с бессимптомной или малосимптомной формами ГКМП и низкой вероятностью внезапной смерти. Противники активной тактики обращают внимание на то, что при благоприятном течении заболевания продолжительность жизни и показатели смертности не отличаются от таковых в общей популяции. Некоторые же авторы указывают на то, что использование в этой группе пациентов β-адреноблокаторов и антагонистов кальция (верапамил) может приводить к сдерживанию гемодинамических нарушений и клинической симптоматики. При этом никто не оспаривает тот факт, что выжидательная тактика в случаях бессимптомного или малосимптомного течения ГКМП возможна лишь при отсутствии признаков внутрижелудочковой обструкции, обмороков и серьезных нарушений сердечного ритма, отягощенной наследственности и случаев ВС у близких родственников.
Следует признать, что лечение ГКМП, генетически обусловленного заболевания, обычно распознаваемого на поздней стадии, пока может быть в большей степени симптоматическим и паллиативным. Тем не менее к основным задачам лечебных мероприятий относятся не только профилактика и коррекция основных клинических проявлений заболевания с улучшением качества жизни пациентов, но и положительное влияние на прогноз, предупреждение случаев ВС и прогрессирования заболевания.
Основу медикаментозной терапии ГКМП составляют препараты с отрицательным инотропным действием: β-адреноблокаторы и блокаторы кальциевых каналов. Для лечения весьма распространенных при этом заболевании нарушений сердечного ритма используются также дизопирамид (антиаритмический препарат IA класса) и амиодарон.
Предпочтение отдается β-блокаторам без внутренней симпатомиметической активности. Наибольший опыт накоплен по применению пропранолола (обзидан, анаприлин). Его назначают начиная с 20 мг 3-4 раза в день, с постепенным увеличением дозы под контролем пульса и артериального давления (АД) до максимально переносимой в большинстве случаев 120–240 мг/сут. Следует стремиться к применению возможно более высоких доз препарата, так как отсутствие эффекта терапии β-блокаторами, вероятно, связано с недостаточной дозировкой. При этом нельзя забывать о том, что повышение дозировок существенно увеличивает риск известных побочных эффектов.
Инвазивные методы лечения:
1. Чрезаортальная септальная миэктомия
2. Вальвулопластики или протезирования митрального клапана
В ряде случаев при наличии дополнительных показаний для уменьшения выраженности обструкции и митральной регургитации одномоментно выполняется операция вальвулопластики или протезирования митрального клапана низкопрофильным протезом. Улучшить отдаленные результаты миэктомии позволяет последующая длительная терапия верапамилом, обеспечивающая улучшение диастолической функции ЛЖ, что не достигается при хирургическом лечении.
3. Иссечения межжелудочковой перегородки
В настоящее время разработаны и успешно применяются отличные от классической миэктомии методики. В частности, в НЦССХ им. А. Н. Бакулева под руководством академика Л. А. Бокерия разработана оригинальная методика иссечения зоны гипертрофированной МЖП из конусной части правого желудочка. Этот способ хирургической коррекции обструктивной ГКМП является высокоэффективным и может стать методом выбора в случаях одновременной обструкции выходных отделов обоих желудочков, а также в случаях среднежелудочковой обструкции ЛЖ.
4. Транскатетерная септальная аблация
Другим альтернативным методом лечения рефракторной обструктивной ГКМП является транскатетерная алкогольная септальная аблация. Методика предполагает инфузию через баллонный катетер в перфорантную септальную ветвь 1–3 мл 95% спирта, вследствие чего возникает инфаркт гипертрофированного отдела МЖП, захватывающей от 3 до 10% массы миокарда ЛЖ (до 20% массы МЖП). Это приводит к значимому уменьшению выраженности обструкции выходного тракта и митральной недостаточности, объективной и субъективной симптоматике заболевания.
В Волынской больнице отработана методика выполнения транскатетерной септальной аблации при ГКМП. Доказан положительный результат данного вмешательства при относительно низком риске развития осложнений.
Ремоделирование левого желудочка
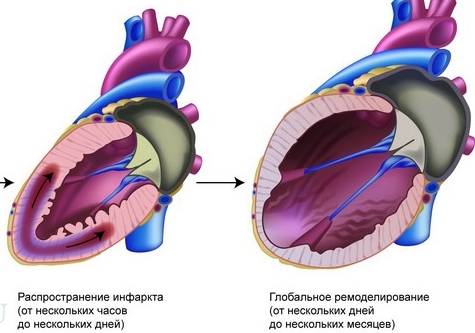
Термин «ремоделирование сердца» был предложен N. Sharp в конце 70-х годов прошлого века для обозначения структурных и геометрических изменений после острого инфаркта миокарда (ОИМ). Затем он получил более широкое толкование.
Ишемическое ремоделирование – динамический, обратимый процесс изменения толщи миокарда,
размера и формы камер сердца, дисфункции левого желудочка (ЛЖ).
Гипертрофия левого желудочка – начальный этап ремоделирования при артериальной гипертензии (АГ),
зависит не столько от уровня АД – гемодинамическая перегрузка, сколько от активности РААС.
Риск развития хронической сердечной недостаточности (ХСН) увеличивается в 15 раз. ГЛЖ развивается по концентрическому типу (добавление саркомеров внутри кардиомиоцита). А11 стимулирует рост мышечных волокон, альдостерон изменяет внутриклеточный матрикс с формированием диастолической дисфункции – ДД.
ДД – ранний этап ремоделирования ЛЖ, маркер фиброза миокарда.
Расслабление – наиболее энергозависимый процесс, при ГЛЖ страдает в первую очередь. Наибольшую гемодинамическую перегрузку при ДД испытывает ЛП. Дилатация ЛП вызывает митральную регургитацию.
Важный этап – переход концентрической ГЛЖ в эксцентрическую. К систолической перегрузке давлением добавляется диастолическая перегрузка объемом. Дилатация ЛЖ сопровождается систолической дисфункцией. А это увеличивает летальность на 50%. ХСН движется к финишной стадии.
ИАПФ вызывают регресс концентрической гипертрофии, уменьшая толщину стенок ЛЖ; нормализуют диастолу Уменьшается объем мышечных волокон и миокардиальный фиброз.
архитектурная перестройка, определяющая прогноз заболевания. После повреждения и гибели части кардиомиоцитов и в нормальной, и поврежденной зоне идет процесс склерозирования. Миоциты гипертрофируются, меняется их взаимное расположение; нарушается соотношение: «основание/верхушка». Активизируются процессы поддержания сердечного выброса и нормализации напряжения стенки ЛЖ. Изменяется радиус кривизны стенок ЛЖ, от которого зависит разная жесткость стенок ЛЖ и распределение внутрижелудочкового объема. Механизм поддержания сердечного выброса и нормализации напряжения стенки ЛЖ реализуется через РААС и гипертрофию не поврежденных сегментов миокарда.
В 1978 г. G. Hutchius и B. Bulkley описали процесс острого увеличения и истоньчения зоны инфаркта без дополнительного некроза миокарда. В первые часы после гибели миоцитов отек и воспаление локализуют зону инфаркта. Дальше наблюдается пролиферация фибробластов и замещение этого участка коллагеном. Зона инфаркта может истончаться и расширяться. Длина сариомеров не изменяется. Таким образом, увеличение объема ЛЖ происходит вследствие перегруппировки миофибрилл без их растяжения. Стенка истончается из-за скольжения мышечн.ых волокон друг относительно друга в результате ослабления связей между миоцитами в инфарктной зоне. При ЭХО КГ определяется увеличение зоны акинезии без ферментативного сдвига.
Экспансия вероятнее всего при трансмуральном ИМ и заканчивается ХСН, аневризмой и разрывом миокарда. Передне-верхушечная область более уязвимая, так как она наиболее изогнута. Возможна дилатация непораженной зоны с тотальным расширением ЛЖ.
Постинфарктное ремоделирование ЛЖ (ПРЛЖ)
Резкое растяжение жизнеспособного миокарда по закону Франка – Старлинга, увеличение
хроно-ино-тропных эффектов при стимуляции адренорецепторов поддерживает насосную
функцию в условиях уменьшения сокращающейся части миокарда. При поражении более
20% массы ЛЖ компенсация будет неадекватной.
Увеличение полости ЛЖ помогает восстановить УО на фоне снижения ФВ.
Дилатация увеличивает миокардиальный стресс, порочный круг замыкается. В качестве компенсации наступает гипертрофия миоцитов: до 78% от исходного объема.
Гипертрофия может быть концентрическая без увеличения полости и эксцентрическая с дилатацией Гипертрофия может восстановить напряжение стенки ЛЖ При обширном ИМ дилатация не пропорциональна приросту массы миокарда
Роль цитокинов. Цитокины – маркеры ХСН
Развитие ХСН сопровождается увеличением провоспалительных цитокинов – интерлейкина— – 1,6; в плазме крови и в миокарде. Без увеличения антивоспалительных цитокинов, что приводит к усилению воспаления. Экспрессия цитокинов и их рецепторов на мембранах кардиомиоцитов подтверждает центральную роль цитокинов в патогенезе ХСН.
В норме вырабатывается кардиомиоцитами предсердий и регулирует водно-солевое равновесие и снижает АД. При уменьшении сердечного выброса у больных асимптоматической дисфункцией ЛЖ и ФК I ХСН растет синтез НП в желудочках сердца. Это блокирует активность циркулирующего звена РААС и компенсирует состояние больных. Прогрессирование ХСН активизирует РААС. Снижается натрий-уретический ответ на рост активности НП. Это приводит к задержке натрия и воды, системной и почечной вазоконстрикции.
Постинфарктная аневризма ЛЖ
Классическим вариантом постинфарктного ремоделирования ЛЖ является постинфарктныая аневризма ЛЖ (ПА), развивается в 8-34% случаев трансмурального инфаркта миокарда: характеризуется акинезией или дискинезией стенки ЛЖ. Изменяется геометрия, объем и масса ЛЖ. Клинически проявляется в виде ХСН у 50% больных и более, желудочковых нарушений ритма, тромбоэмбоэмболического синдрома.
Хирургическим методом лечения является реваскуляризация миокарда и пластика
ЛЖ. Прогностически неблагоприятны ранние аневризмы при переднем ИМ.
— более 2-х ИМ в анамнезе;
— поражение трех основных бассейнов коронарных артерий.
Прогноз ремоделирования ЛЖ
Рентгенологически видимое увеличение ЛЖ неблагоприятно и увеличивает летальность в 3 раза, прогнозирует развитие ХСН. Подъем с. SТ со снижением или отсутствием з. R на ЭКГ помогает не только диагностировать ИМ, определить его размеры, но и предполагать ремоделирование ЛЖ. Компенсаторные процессы зависят от состояния коронарного кровотока уцелевшего миокарда, при неадекватном кровоснабжении дилатация больше, выше летальность. Стеноз артерий ограничивает компенсаторную гипертрофию миокарда и повышенную нагрузку. Дилатация полостей прямо коррелирует с риском фатальных аритмий.
Первичная профилактика не вызывает сомнений: это наиболее раннее и адекватное восстановление перфузии у больных ОКС. Профилактика ХСН начинается в первые часы ОИМ. Надо ограничить зону некроза: тромболитики, нитраты. БАБ, антиагреганты.
1 Доказан эффект ИАПФ: предпочтительны пролонгированные препараты и действующие на тканевой АПФ. Летальность от ХСН достоверно снижается, ФВ – увеличивается.
ИАПФ более эффективны при переднем ИМ. Терапия ИАПФ назначается в первые сутки
2 БАБ оказывают не только антиаритмическое действие, но и тормозят ремоделирование ЛЖ. K. Shiono не отметил эффект от атенолола. Метопролол вызывает редукцию объема и регрессию массы ЛЖ; улучшает геометрию ЛЖ.
3 Эффективны антагонисты кальция: амподипин, дилтиазем и изоптин, но лечение
должно быть длительным.
4 Нитраты ограничивают раннее постинфарктное ремоделирование ЛЖ.
5 Дигоксин в результате инотропной стимуляции при переднем ИМ может увеличивать инфарктное выпячивание ЛЖ без снижения содержания коллагена.
6 L- карнитин в остром и отдаленном периоде ИМ уменьшал дилатацию ЛЖ (S. Iliceto).
1 Кардиология, 2003, 8, стр. 83-94.
2 Кардиология, 2003, 8, стр. 68-72.
3 Бузиашвили ЮИ и др Кардиология, 2002, 10, стр. 88-94.