Коронарные сосуды что это и где находится
Артерии и вены сердца (ангиография, КТ).
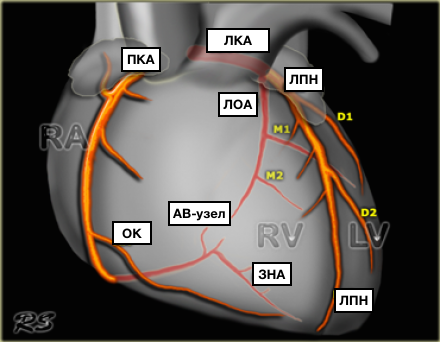
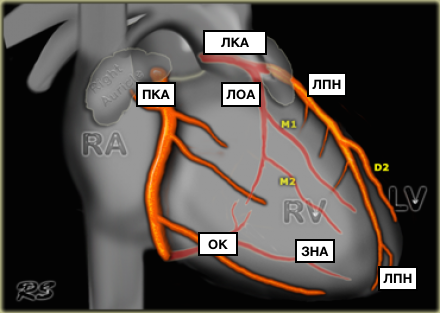
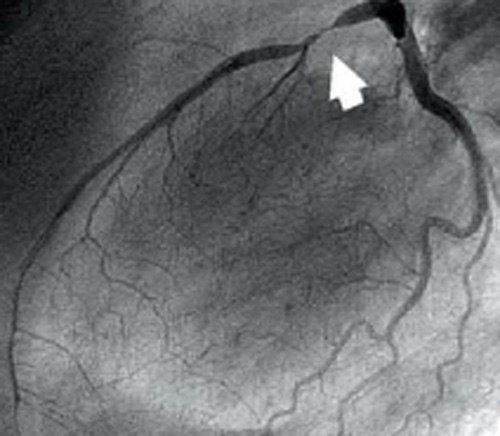
Представлены коронарные артерии в латеральной проекции.
Анатомия коронарных артерий используемая при ангиографии.
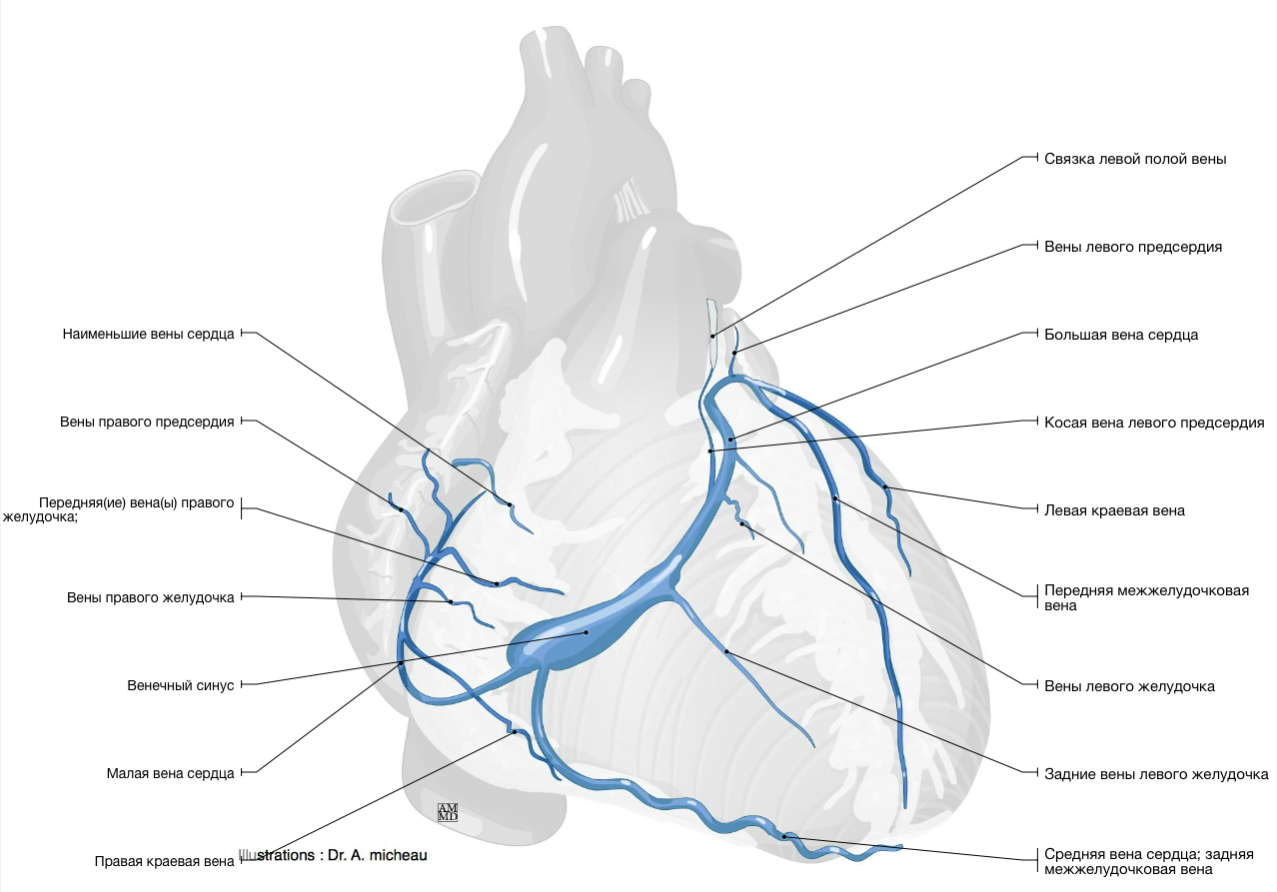
Вены сердца
Вены сердца открываются не в полые вены, а непосредственно в полость сердца. Они начинаются в виде сетей, располагающихся в различных слоях его стенки. Венозное русло значительно преобладает над артериальным.
Венозный отток идет по трем путям: в венечный синус, sinus coronarius; в передние вены сердца; в малые вены Тебезия [Thebesian], впадающие непосредственно в правый отдел сердца.
Венечный синус, sinus coronarius лежит сзади, в венечной борозде, и открывается в правое предсердие несколько ниже ствола нижней полой вены.
В венечный синус приносят кровь большая вена сердца, v. cordis magna, которая собирает кровь от передней поверхности обоих желудочков. Сначала она располагается в передней межжелудоч-ковой борозде, рядом с ramus interventricularis anterior левой венечной артерии, затем уходит под левое ушко и переходит на заднюю поверхность, где впадает (продолжается) в венечный синус.
Средняя вена сердца, v. cordis media, из задней межжелудочковой борозды переходит в венечную борозду и впадает в венечный синус справа. Кроме этих крупных вен, в венечный синус впадают малая вена сердца, v. cordis parva, задняя вена левого желудочка, v. posterior ventriculi sinistri, и косая вена левого предсердия, v. obliqua atrii sinistra [Marshall].
Передние вены сердца, vv. cordis anteriores, несут кровь от верхнего отдела передней стенки правого желудочка и впадают в правое предсердие.
Малые вены, vv. cordis minimae, собирают кровь в глубине стенок сердца и через множество отверстий впадают непосредственно в правое предсердие.
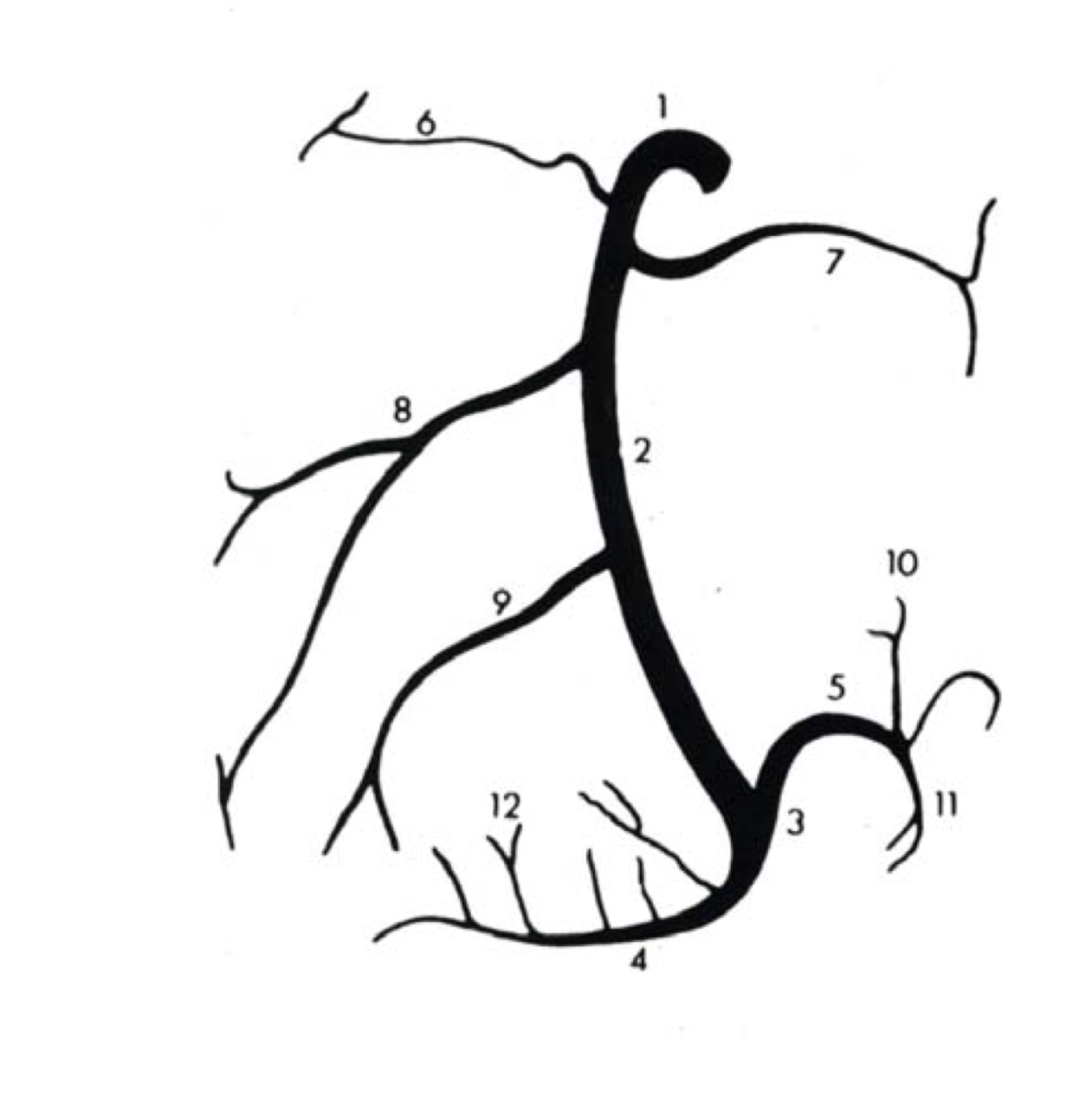
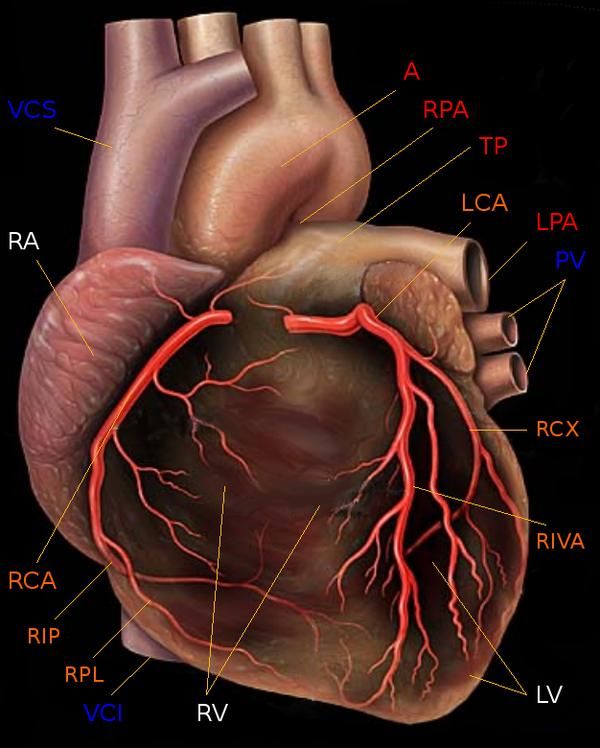
Анатомия сердечно-сосудистой системы
1. Правая коронарная артерия
2. Передняя нисходящая артерия
3. Ушко
4. Верхняя полая вена
5. Нижняя полая вена
6. Аорта
7. Лёгочная артерия
8. Ветви аорты
9. Правое предсердие
10. Правый желудочек
11. Левое предсердие
12. Левый желудочек
13. Трабекулы
14. Хорды
15. Трикуспидальный клапан
16. Митральный клапан
17. Клапан лёгочной артерии
Большой круг включает в себя аорту (восходящая и нисходящая, дуга аорты, грудной и брюшной отдел), по которой течёт кровь от левых отделов сердца. От аорты кровь попадает в сонные артерии, кровоснабжающие головной мозг, подключичные артерии, кровоснабжающие руки, почечные артерии, артерии желудка, кишечника, печени, селезёнки, поджелудочной железы, органов малого таза, подвздошные и бедренные артерии, кровоснабжающие ноги. От внутренних органов кровь оттекает по венам, которые впадают в верхнюю полую вену (собирает кровь от верхней половины туловища) и нижнюю полую вену (собирает кровь от нижней половины туловища). Полые вены впадают в правое сердце.
Малый круг кровообращения включает в себя лёгочную артерию (по которой, тем не менее, течёт венозная кровь). По лёгочной артерии кровь поступает в лёгкие, где обогащается кислородом и становиться артериальной. По лёгочным венам (четыре) артериальная кровь поступает в левое сердце.
Клапанный аппарат сердца
Работа сердца
Из левого и правого предсердия кровь поступает в левый и правый желудочек, при этом митральный и трикуспидальный клапан открыты, аортальный и клапан лёгочной артерии закрыты. Эта фаза в работе сердца называется диастолой. Затем митральный и трикуспидальный клапаны закрываются, желудочки сокращаются и через открывшиеся аортальный и клапан лёгочной артерии кровь, соответственно, устремляется в аорту и лёгочную артерию. Эта фаза называется систолой, систола короче диастолы.
Проводящая система сердца
Кровоснабжение сердца
Теперь, когда Вы стали специалистом в области анатомии сердечно-сосудистой системы перейдём к её заболеваниям.
Заболевания периферических артерий:
Оглавление
Ряд серьезных заболеваний требует точной и быстрой постановки диагноза, благодаря чему удается не только избавить человека от неприятных симптомов, но и спасти его жизнь. В клиниках МЕДСИ используются современные диагностические методики, одна из которых – коронарография – чрезвычайно важна при наличии ишемической болезни сердца, нарушениях ритма и проводимости сердца и других патологиях сердечнососудистой системы. ИБС – заболевание, которое является одной из основных причин смертности во всех странах мира. ИБС диагностируется преимущественно у мужчин после 40 лет, однако коронарографию следует проходить при наличии показаний, вне зависимости от пола. Исследование применяется с середины 20 века, и в развитых странах является вторым по распространенности среди малоинвазивных процедур.
Что такое коронарография
Коронарная ангиография – малоинвазивное исследование сосудов сердца, в ходе которого врач получает рисунок сосудов сердца с помощью введения в артерии рентгенконтрастного вещества. Сегодня данная процедура считается одной из самых информативных в кардиологии в отношении патологии сосудов.
Инвазивность коронарографии заключается в выполнении прокола вены для введения специальной тонкой трубки – катетера, которая в ходе процедуры будет продвинута к сердцу. Ход продвижения катетера контролируется врачом с помощью оборудования. При коронарографии вводят рентгенконтрастное вещество – такое, которое способно поглощать рентгеновские лучи. Благодаря данному веществу и работе рентген-аппарата на экране монитора формируется картина сосудов, и врач может в деталях изучить места сужения артерий и степень данной патологии. Коронарография сосудов сердца редко требует общего наркоза, в подавляющем большинстве случаев достаточно местной анестезии. Исследование не требует длительной госпитализации и имеет высокую диагностическую ценность для определения состояния здоровья пациента, методики его лечения и объема необходимых хирургических манипуляций.
Виды коронарографии отличаются объемом проведения исследования:
В зависимости от методики проведения коронарография сердца может быть следующих видов:
Показания к коронарографии
Показаний к процедуре достаточно много, их список постоянно расширяется, но к наиболее часто встречающимся относят следующие:
Коронарографию сосудов проводят в том числе перед серьезными операциями по трансплантологии, а также для людей с профессиями повышенных рисков – летчиков, космонавтов и других.
Противопоказания
Процедура может быть проведена для любого пациента, однако ее откладывают или проводят с большой осторожностью в некоторых случаях.
При наличии у пациента таких состояний исследование по возможности не проводят до стабилизации здоровья, однако в экстренных случаях коронарография сосудов допустима, так как она имеет большую диагностическую ценность и может быть чрезвычайно важной для спасения жизни человека.
Подготовка к коронарографии
Перед процедурой пациент проходит различные исследования – крови, УЗИ сердца, электрокардиографию, нагрузочный тест и сдает другие анализы, полный список которых назначается лечащим врачом.
Коронарография выполняется в первой половине дня, натощак, и длится от 30 до 120 минут. Если исследование проводят амбулаторно, предварительной госпитализации не требуется, и пациент приходит утром сразу на коронарографию. В стационаре же госпитализация выполняется накануне.
Для уменьшения нервозности перед исследованием проводится инъекция препарата, успокаивающего нервную систему. В процессе выполнения процедуры пациент может наблюдать на экране ход коронарной ангиографии, общаться с врачом, но в некоторых случаях возможно также использование общего наркоза.
Для введения рентгенконтрастного вещества выполняется пункция артерии на руке или бедре, поэтому место пункции следует заранее освободить от волосяного покрова.
Как производится коронарография
Коронарография сердца проводится в специально оснащенной рентген-оборудованием операционной. Пациента подключают к датчикам электрокардиограммы, обрабатывают место прокола вены антисептиками и выполняют местное обезболивание. Когда операционное поле готово, сосуд прокалывают для введения катетера. Он представляет собой тонкую трубочку, которую врач продвигает к устью артерии, контролируя это продвижение с помощью аппаратуры. Когда устье артерии достигнуто, через конец катетера в месте пункции врач начинает подавать контрастное вещество, которое через катетер доходит до сосудов сердца. В это время выполняются рентген-снимки и видеозапись процесса заполнения сосудов веществом. И пациент, и врач могут следить за выполнением коронарографии на экране. Когда снимки сделаны, врач завершает процедуру, извлекая катетер и накладывая на место пункции давящую повязку.
Возможные осложнения
В перечень возможных осложнений входят следующие.
Однако все эти осложнения маловероятны, их суммарная частота составляет не более 2 %, а проведение исследований до процедуры и врачебное наблюдение после нее делают риски для пациентов минимальными.
После коронарографии
Сразу после завершения исследования на место прокола артерии накладывают салфетку и с силой фиксируют ее специальным прибором для остановки кровотечения. Через 10-15 минут салфетку меняют тугой повязкой. В ближайшие 5-10 часов пациент должен находиться под врачебным наблюдением в обычной палате. Срок пребывания в лечебном учреждении зависит в том числе от показателей свертываемости крови. Все это время пациент должен сохранять горизонтальное положение, не разрешается также сгибать руку или ногу, на которой проводилась пункция. Прием пищи возможен сразу после процедуры. Обычно пациент на второй день после процедуры полностью работоспособен и может покинуть палату. Врачи тщательно изучают полученные снимки и видео.
Преимущества проведения коронарографии в МЕДСИ
В клиниках МЕДСИ коронарография сосудов сердца проводится только врачами высшей категории. Для удобства пациентов и получения точных результатов мы предлагаем:
Коронарография сосудов в МЕДСИ позволяет быстро и точно установить диагноз и выбрать наиболее эффективную методику лечения болезни. Звоните, чтобы получить дополнительную информацию и записаться на прием к врачу.
Коронарная ангиопластика и стентирование коронарных артерий
(Ангиопластика сердца, стентирование, коронарная ангиопластика, стентирование сосудов сердца)
Правильное название процедуры: Коронарная ангиопластика со стентированием или чрескожное коронарное вмешательство.
Для простоты иногда говорят просто «стентирование».
Что такое стентирование коронарных артерий
Кому показано стентирование сосудов сердца?
Стентирование сосудов сердца показано пациентам с тяжелой стенокардией, после инфаркта миокарда и предынфарктным состоянием, больным с доказанной ишемией (нехваткой крови сердцу) по результатам нагрузочных проб. При этом решение о стентировании принимается только по результатам коронарографии – контрастного исследования сосудов сердца. Коронарография, как и стентирование, выполняется в рентгеноперационной. Часто коронарография «переходит» в стентирование сосудов т.к. выполняется через один и тот же прокол в артерии.
Какие альтернативные стентированию методы существуют?
Как выбрать между стентированием, шунтированием и медикаментозной терапией?
Это задача вашего кардиолога, который учитывает следующие данные:
Методика стентирования коронарных артерий (с профессиональным жаргоном)
Первый инструмент, который попадает к месту сужения артерии – коронарный баллон диаметром чаще всего от 1 до 3.5 мм длиной 10-20 мм. Баллон надевается на проводник и движется по нему до места максимального сужения где он раздувается. Давление внутри баллона при этом достигает 15-20 атмосфер.
Внутрь имплантированного стента заводится жесткий баллон и раздувается большим давлением (до 25 атмосфер). Чаще всего после этого стент расправляется и хорошо прилегает к стенкам артерии.
Контрольная коронарография
Гемостаз
Что делать с отверстием в артерии?
Если вмешательство проводилось через лучевую артерию (на руке) – на запястье надевается специальный браслет с валиком (гемостатическая манжета), который будет давить на место вкола и не допустит кровотечения. В зависимости от ситуации манжета останется на руке от 3 до 12 часов.
В случае бедренного доступа возможны 2 основных варианта:
Коронарная ангиопластика и стентирование
Риск серьезных осложнений очень зависит от степени поражения артерий, локализации бляшек, извитости артерий, наличия кальциноза и, конечно, опыта оператора.
В среднем риск серьезного осложнения не превышает 1%. Этими осложнениями могут быть:
«Малые осложнения» стентирования:
Коронарография
Физиологические основы
В университетскую программу первых курсов входит изучение строения сердца и его коронарных сосудов. Но чаще всего авторы учебников ограничиваются описанием только крупных сосудов. Клиницисты же используют совершенно иную, но также международную номенклатуру. Коронароангиография и имплантация стентов требуют более подробного описания сосудов сердца, что нашло применение и в международной практике.
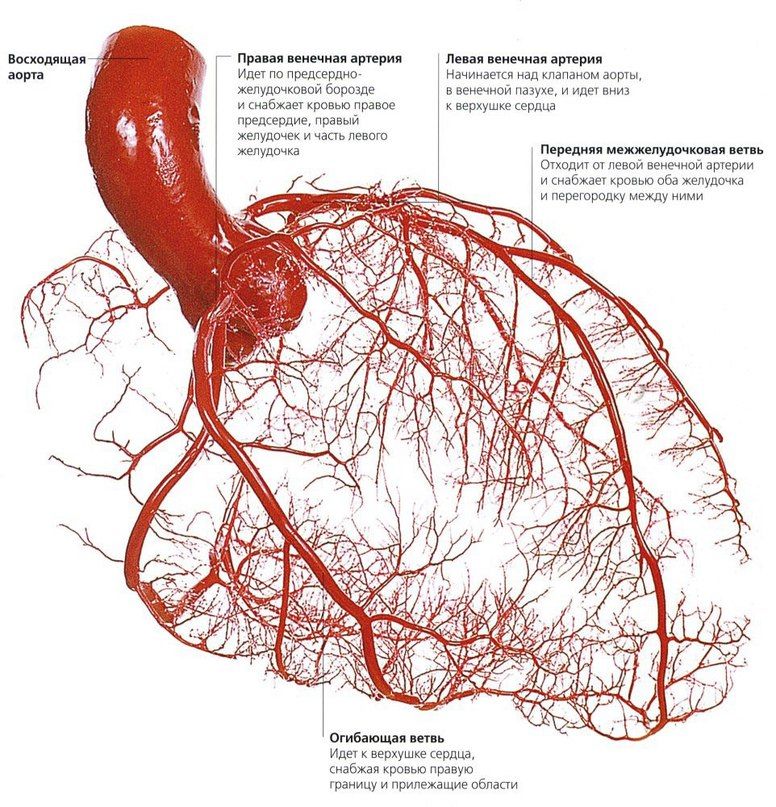
Из курса анатомии каждый узнал, что от аорты отходят две артерии, кровоснабжающие само сердце: левая и правая коронарные артерии. Утолщения на корне аорты, из которых и выходят эти артерии, называются соответственно левым и правым коронарными синусами.
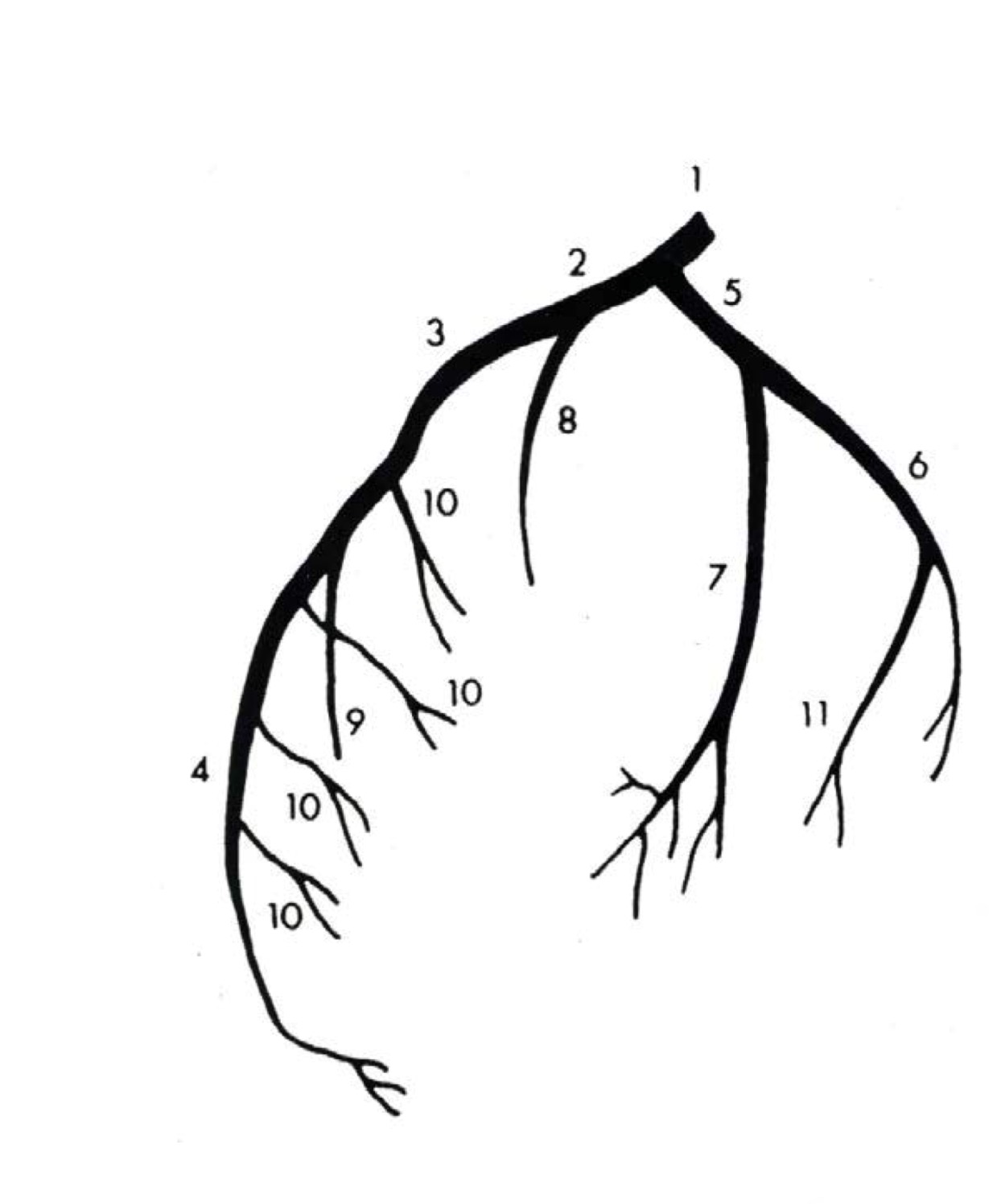
Выделяют следующие части левой коронарной артерии (LCA, left coronary artery): главный ствол, который делится на переднюю межжелудочковую ветвь (ramus interventricularis anterior, RIVA или left anterior descending, LAD), а также огибающую артерию (left circumflex coronary artery, LCх).
Проксимальный сегмент ПМЖВ начинается своим ответвлением от ствола и продолжается до места отхождения от нее первой перегородочной или первой RD, средняя часть — до ответвления второй перегородочной ветви или второй RD, дистальная — до верхушки сердца/после отхождения второй RD.
Иногда непосредственно после самого устья от сосуда отходит маленькая ветвь — ветвь артериального конуса (ramus coni arteriosi, CB), а также много мелких ветвей к правому предсердию.
Итак, перечислим еще раз все сокращения:
Левая коронарная артерия — left coronary artery (LCA):
— Передняя межжелудочковая ветвь (ПМЖВ), или передняя нисходящая артерия — left anterior descending artery (LAD); иначе — ramus interventricularis anterior (RIVA/RIA);
— Диагональные артерии (ветви) — ДА; ramus diagonalis (RD/Diag);
— Огибающая ветвь (ОВ) левой коронарной артерии, огибающая артерия — left circumflex coronary artery (LCх));
— Ветвь тупого края, obtuse marginal artery, obtuse marginal branch, (OMB);
— Перегородочные межжелудочковые ветви, ramus septalis (RSA);
— Промежуточная артерия, ramus intermedius (RIM).
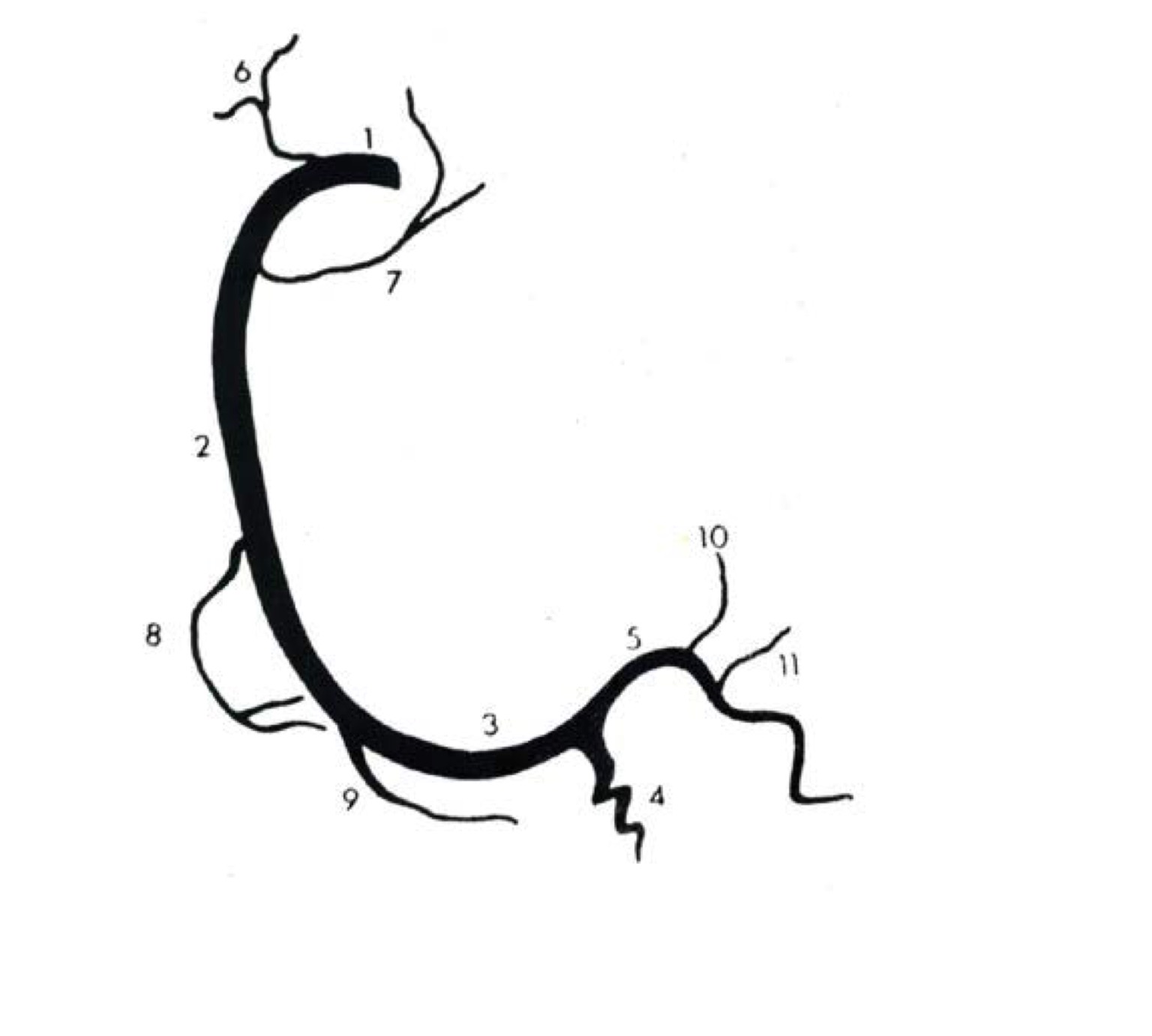
Правая коронарная артерия — right coronary artery (RCA):
— Ветвь острого края, acute marginal artery, (AMB);
— Артерия синоатриального узла — ramus nodi sinuatrialis (S-A node artery, SNASA/RNS);
— Задняя межжелудочковая ветвь (ЗМЖВ), или задняя нисходящая артерия — posterior descending artery (PDA); иначе — ramus interventricularis posterior (RIVP/RIP).
И еще раз для повторения (важное задание для диагностики локализации ишемии при инфаркте миокарда): LAD/RIVA, LCx кровоснабжает левую камеру спереди и сбоку, а RCA — сзади. Левое предсердие кровоснабжают LCx, RCA. Перегородку — RSA от LAD. Правую камеру сзади — RCA, спереди — RCA, LAD. Правое предсердие — RCA.
Следует также напомнить о доминантности кровоснабжения миокарда. При так называемом правом типе кровоснабжения сердца, наблюдающемся у 70 % людей, задняя нисходящая артерия (PDA) отходит от правой коронарной артерии. При левом типе кровоснабжения сердца (10 % людей) огибающая артерия (LCx) достигает уровня задней межжелудочковой борозды и образует заднюю нисходящую артерию (PDA). При еще более редком, так называемом смешанном содоминантном типе (20 % людей), имеются две задних желудочковых ветви (RIVP/RIP), отходящих от правой венечной и огибающей артерий.
Электрокардиограмма представляет собой не что иное, как запись распространяемых электрических потенциалов сердца, фиксируемых электродами на конечностях и грудной стенке. ЭКГ включает в себя три стандартных отведения по Эйнтховену (I, II, III), и три усиленных по Гольдбергу (aVR, aVL, aVF). Прикрепление еще шести грудных электродов по Вильсону (V1-V6) позволяет зарегистрировать распространение возбуждение по сердечной стенке в горизонтальной проекции. В зависимости от изменений в этих отведениях еще на догоспитальном этапе при помощи ЭКГ можно предположить локализацию инфаркта и возможную «проблемную» артерию.
Например, при инфаркте правых отделов сердца (задней стенки) часто особенно сильно поражается правый желудочек. Чаще всего это происходит из-за тромба в RCA. Правые отделы сердца не способны сокращаться должным образом, что приводит к снижению преднагрузки левой камеры сердца, поскольку таким образом снижается объем крови, транспортируемый к левому предсердию. Сниженный сердечный выброс сердце пытается компенсировать увеличением частоты сокращений. При инфаркте же левых отделов сердца основным осложнением является кардиогенный шок.
Специально для наших подписчиков мы сделали таблицу, в которой показаны изменения ЭКГ в зависимости от локализации возможного повреждения коронарных артерий.
Стоит также повторить и классификацию острых коронарных синдромов:
Нестабильная стенокардия без повышения тропонина. Эта форма классифицируется по Браунвальду на 3 класса в зависимости от выраженности клинических признаков:
I — недавно возникшая боль за грудиной (менее 2-х месяцев, более 3-х раз в день);
II — боль за грудиной в покое (минимум один раз за прошедший месяц, но не в течении последних 48 часов);
III — боль за грудиной в покое (минимум один раз за последний 48 часов).
Нестабильную стенокардию классифицируют на 3 группы по причинам возникновения:
А — вторичная нестабильная стенокардия (инфаркт миокарда, анемия, повышение температуры, гипотензия, тахиаритмия, тиреотоксикоз, дыхательная недостаточность);
B — первичная нестабильная стенокардия;
C — нестабильная стенокардия после инфаркта (минимум 2 недели после инфаркта).
Инфаркт миокарда без элевации сегмента ST (NSTEMI) с повышением концентрации кардиального тропонина в крови.
Инфаркт миокарда с элевацией сегмента ST (STEMI) с повышением концентрации кардиального тропонина в крови.
ПБКА и стентирование
Sones еще в 1959 году описал метод, позволяющий оценить состояние отдельных коронарных сосудов. Judkins модифицировал описанный метод в 1967 году. Именно этот способ исследования коронарных сосудов применяется и по сей день. Первая транслюминальная баллонная коронарная ангиопластика (ТБКА) была проведена 16 сентября 1977 в Цюрихе в Швейцарии. С этого момента количество пациентов с ОКС, подвергшихся ТБКА, возросло с 10 до 65 %. По последним данным, недавно опубликованным в журнале The Lancet, смертность вследствие сердечно-сосудистых заболеваний в 2010 году снизилась на четверть по сравнению с 1950 годом, когда 400 из 100 000 случаев заканчивались летальным исходом. Первым пациентом был 38-летний мужчина-курильщик, у котого наблюдался стеноз LAD. После операции мужчина прожил еще 37 лет.
При ПБКА баллонный катетер с помощью проводника вводится вплоть до места стеноза. Баллон раздувается и тем самым «сплющивает» атеросклеротические бляшки, растягивая сосудистую стенку. Мелкие повреждения интимы во время раздувания баллона часто не имеют последствий, однако иногда именно в этих местах позже начинается пролиферация тканей, что в 30–40 % случаев приводит к рестенозам и рецидивам в течение последующих трех месяцев. Частота экстренных операций по созданию шунтов (bypass) составляет менее 0,5 %. С помощью имплантации стента сосудистая стенка стабилизируется. Существовала также техника primary stenting — имплантация стента без предшествующего дилатирования сосудов баллоном, однако ныне она используется крайне редко и только на начальных этапах сужения просвета сосуда. Исследования последних лет показали, что при значительных сужениях просвета сосуда, у таких пациентов в первые часы после ангиопластики наблюдалась ишемия миокарда, что требовало немедленного повторного хирургического вмешательства или повторной дилатации. Это осложнение возникает вследствие отрыва бляшки от эндотелия. Обнажение поверхности гладкомышечных клеток приводит к тромбообразованию за счет высвобождения молекул коллагена и тканевых факторов, запускающих каскад свертывания крови. Во избежание развития тромбов и рестеноза в настоящее время чаще всего ангиопластику совмещают с имплантацией стентов на месте стеноза.
Первую имплантацию стента провел Sigwart в 1987 году. Тогда стенты монтировались непосредственно на баллон самим врачом. Сейчас же вся конструкция идет в комплекте, что позволило снизить риск потери стента в кровеносном русле при его недостаточной фиксации.
Появились и новые типы самих баллонов. Некоторые из них имеют на своей поверхности режущие зубцы, что расположены параллельно оси сосуда, а также баллоны из нитинола и нейлона хеликальные или же параллельные оси сосуда. Эти конструкции позволяют создать идеальную площадку для имплантации будущего стента. Сперва в процессе исследований ученые не заметили разницы между такими баллонами и стандартными, однако недавно выяснилось, что такие надсекающие баллоны, покрытые лекарственными средствами, показывают лучшие результаты.
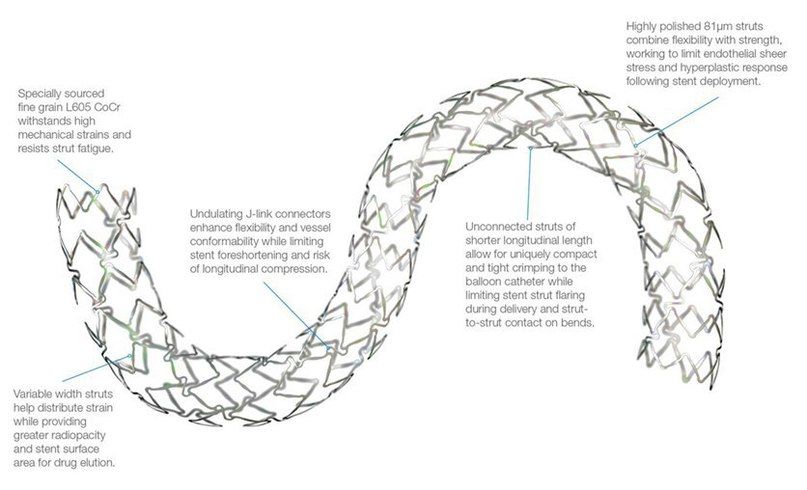
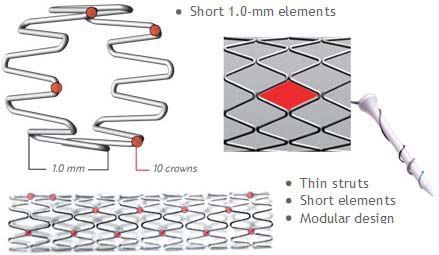
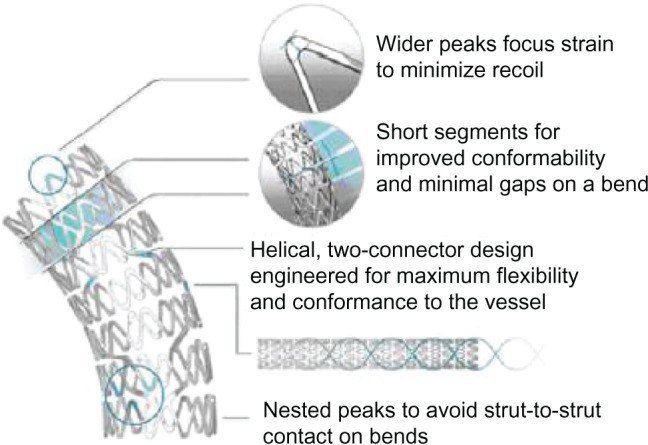
Различают два типа металлических стентов: саморасширяющиеся и прикрепленные к дилатирующему баллону. Исследования показывают, что применение первого типа стентов чаще вызывает развитие неоинтимальной гиперплазии. Поэтому в настоящее время часто используются стенты второго типа. Как правило, они состоят из металлической трубочки, в которой с использованием различных техник создаются отверстия. После расширения сосуда баллонным катетером в его просвете создается сеть, обволакивающая его стенки изнутри. Прототипом такого типа стентов являлся стент Palmaz-Schatz, который сейчас уже не применяется.
Исследование 1994 года не показало разницы между имплантацией такого стента и обычной ангиопластикой. Развитие этого направление позволило разработать новые типы стентов. Чаще всего они состоят из нескольких модулей, соединенных коннекторами. Изначально их производили из стали, однако сейчас в качестве материала для изготовления стентов используется платина, кобальт, нитинол (никель-титан), а также только титан. Из-за этого они стали существенно меньше и легче. РКИ выявили преимущества стентов с толстым каркасом перед таковыми с тонким. Предполагают, что они меньше травмируют сосуды, предотвращая таким образом реэндотелизацию.
Существуют также стенты с особым покрытием, создающим непроницаемый для крови барьер. К таким вещества относят политетрафторэтилен и полиэтилен. Сперва их использовали для экстренного закрытия небольших перфораций коронарных артерий, однако сейчас их применяют в профилактике коронарных аневризм и артериовенозных фистул.
Drug-eluting-stents (DES) покрыты специальными веществами, подавляющими пролиферацию клеток эндотелия, таким образом препятствуя рестенозированию сосуда, чаще всего развивающемуся в течение 4–8 месяцев после имплантации.
Стенты – ферромагнетики, плотно устанавливающиеся в сосудистом русле не являются противопоказанием для проведения МРТ.
Существуют специальные стенты для позиционирования их в устьях и разветвлениях сосудов. Как и любой инородный объект в кровеносном русле, стенты являются дополнительным фактором тромбообразования. Поэтому после самой процедуры пациенту всегда назначают ДААТ или ТАТ.
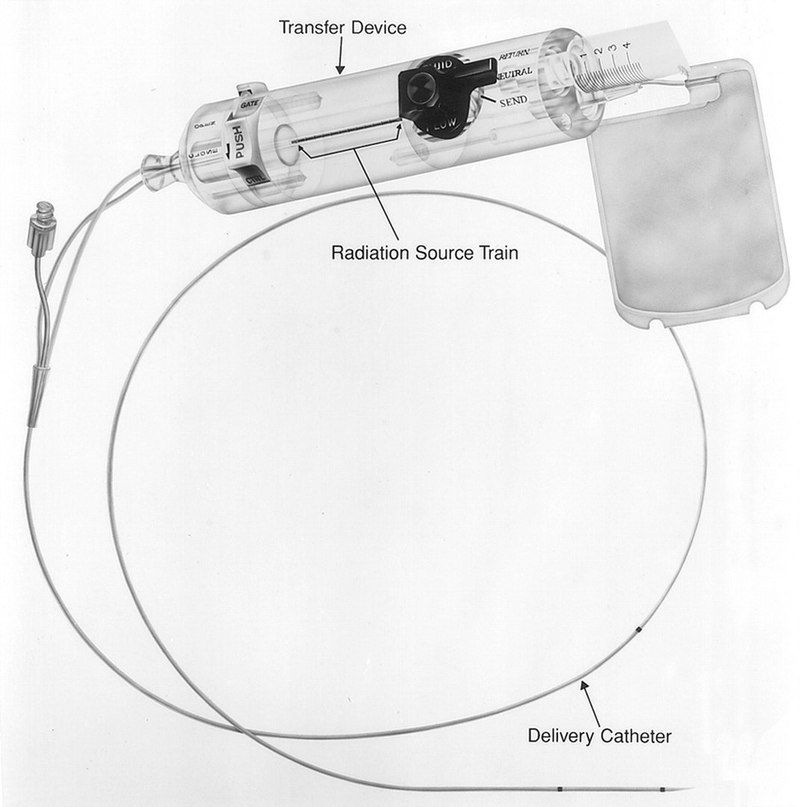
Брахитерапия
Этот метод основан на радиоактивном облучении коронарных артерий при рецидивах после имплантации стентов. Для этого используется бета-излучение, поскольку оно способно проникать лишь на несколько миллиметров внутрь толщи ткани. При этом методе катетер вводят в место стеноза, который прежде был дилатирован баллоном. С помощью этого катетера зону определенное количество времени (3–5 минут) облучают рассчитанной дозой. Васкулярная брахитерапия используется с 1996 года. В феврале 2005 года прекратила свое существование фирма, разрабатывающая аппараты для брахитерапии коронарных сосудов (Beta-Cath-System).
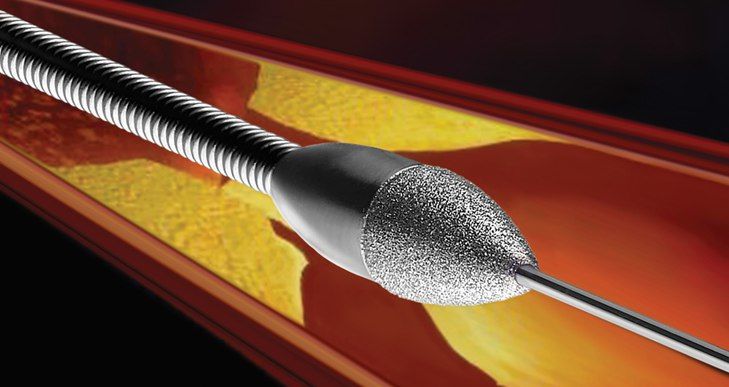
Ротаблационная пластика
Этот метод используется с 1989 года. В сосуд вводится алмазный бор, способный вращаться с частотой 190 000 об. в минуту. С его помощью удаляются ткани в месте рестенозирования. Величина таким образом измельченных частиц составляет 5–10 микрометров (длина эритроцита — 7,5 микрометров). Образуемый канал очень небольшой в диаметре, но достаточный для проведения ПТКА. Как правило, метод используют в случае образования на месте рестеноза кальцификатов. Диаметр головки бора варьируется от 1,25 до 2,5 мм. Поскольку кабель для ротаблационного бора плохо проходит место стеноза, успех операции составляет 80–95 %. К осложнениям относят спазмы сосудов, возникающие чаще (5 %), чем при ПТКА.
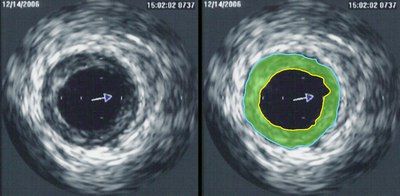
Интраваскулярный ультразвук
Еще одним инструментом кардиолога является метод интраваскулярного ультразвука (IVUS). В сосуд вводят ультразвуковой зонд.
Порядок манипуляций напоминает таковой при ПТКА: после позиционирования проводника зонд проводят к месту стеноза. Ультразвук позволяет просмотреть 1 мм тканей на расстоянии от излучателя. Всего на верхушке катетера используется 64 таких кристалла (пьезоэлемента). С помощью этого метода возможно определить состав бляшек и их фибринные, липидные и кальциевые составляющие. Чаще всего к ультразвуку прибегают при неоднозначности ангиографической картины, используя как дополнительный метод обследования.
Всех нас на физиологии мучили графиками давления в сосудах. Мало кто на младших курсах мог подумать, что эти данные действительно используются в диагностике. При каждой коронароангиографии исследуют давление в коронарных артериях и его изменения в зависимости от наличия стенозированных участков. Для этого к исследуемому участку подводят детектор диаметром 0,014 дюймов. Этот катетер продвигают до самого конца коронарной артерии. Потом его тянут обратно. Таким образом фиксируется давление на всем протяжении артерии. На мониторе врачи наблюдают изменение давления; в месте наибольшего его перепада чаще всего и оказывается самый стенозированный участок. Постепенное изменение давления является свидетельством диффузного заболевания сосудов. Важно откалибровать детектор до самого исследования. После аппликации аденозина наблюдается гиперемия, то есть увеличение циркуляции крови, что симулирует состояние нагрузки. После этого давление на протяжении сосуда измеряется еще раз, что позволяет определить, являются ли места стенозирования важными, вызывают ли именно они боли у пациента при физических нагрузках. Аденозиновый тест не является безопасным: возможно развитие нарушений сердечного ритма, однако из-за короткого периода полувыведения аденозина лишь кратковременно.
Спазмы коронарных сосудов и ацетилхолиновый тест
Спазмы коронарных артерий часто являются причиной болей за грудиной в ночное время суток у пациентов без видимых изменений коронарных сосудов. Таким пациентам также назначают коронароангиографию и проводят вышеуказанный провокационный тест, чтобы исключить психогенные или некардиальные причины таких симптомов. Сейчас у каждого человека, уже сдавшего физиологию, должна промелькнуть мысль: «Почему ацетилхолин?». Если вы не находите ответа, возможно, придется снова открыть учебник. Дело в том, что эндотелий сердца при аппликации ацетилхолина вырабатывает NO, что приводит к расширению сосудов. Ацетилхолин оказывает вазоконстрикторное действие на гладкомышечные клетки сосудов в результате прямой их стимуляции, если эндотелий поврежден. Таким образом можно отличить здоровый эндотелий от поврежденного. Здоровые сосуды реагируют на ацетилхолин расширением, поврежденные же сужаются. При сужении сосудов более чем на 75 % по сравнению с аппликацией нитроглицерина внутрикоронарно говорят о коронарном спазме.
Источники: