Креатинин после удаления почки вырос что делать
Жизнь после удаления почки: диета, мониторинг состояния
Операции по удалению почки проводят по одной из трех причин: врожденная патология, необратимое повреждение вследствие болезни или травмы, донорское пожертвование. В любом случае человеку приходится учиться жить с одной почкой. Какие сложности и ограничения ждут после операции, расскажут специалисты Государственного института урологии.
Фактическими показаниями к нефрэктомии являются: поликистоз почки, поражение органа с гнойным осложнением, онкологическое перерождение тканей, травмирование с последующим разрывом. Врачи Государственного института урологии ориентированы на органосохраняющие стратегии. Целесообразность хирургического вмешательства в каждом случае определяет консилиум после тщательного обследования пациента.
В чем сложности для организма
Как жить с одной почкой после удаления – вопрос, который тревожит многих пациентов. Важно понимать, что нагрузка, которая ранее приходилось на два органа, сейчас ложится на один. Из-за этого оставшаяся почка претерпевает изменения, чтобы обеспечить достаточный объем и уровень фильтрации. Она увеличивается в размерах, компенсация происходит за счет роста самих клеток и более быстрой клеточной пролиферации.
Компенсаторное увеличение может сопровождаться болями тупого характера в области удаленной почки. Как правило, они временны, неопасны и проходят сами по себе. Врачи рекомендуют воздержаться от приема болеутоляющих средств, чтобы дополнительно не нагружать здоровый орган.
Продолжительность жизни после нефрэктамии
Реабилитация сразу после нефрэктомии
Восстановительный период после нефрэктомии занимает до 6 недель. Перед операцией врач проведет несколько бесед, расскажет, больно ли удалять почку и как правильно вести себя в дальнейшем. Нефрэктомия – серьезная операция, поэтому на стационарном лечении и после него вводится обязательная медикаментозная поддержка. Пациенту назначают антибиотики, противовоспалительные средства, обезболивающие.
В послеоперационный период необходимо:
отказаться от алкоголя;
ограничить физические нагрузки;
носить поддерживающий бандаж;
не поднимать тяжести;
вести размеренный образ жизни, избегать переутомления и стресса.
Диета предполагает отказ от чрезмерно соленой и острой еды, копченостей. В рацион вводят овощные супы, каши, соки, отварные рыбу и мясо, показан прием молочных продуктов. Питание осуществляется небольшими порциями. Такой формат необходимо соблюдать до конца адаптации организма.
Рекомендации по образу жизни
Жизнь после удаления почки имеет некоторые ограничения. Важно соблюдать питьевой режим и сбалансированно питаться. Следует избегать резких перемен в рационе, максимально ограничить консерванты, соления и острую пищу. После нефрэктомии не стоит злоупотреблять минеральными водами, поскольку одна почка будет плохо справляться с выведением солей, что может увеличить риск камнеобразования.
Врачи рекомендуют придерживаться следующих правил:
не принимать бесконтрольно лекарственные препараты;
при назначении любого типа терапии уведомить врача о нефрэктомии;
своевременно лечить воспалительные заболевания горла и проводить санацию ротовой полости;
заниматься лечебной гимнастикой, ввести в режим обязательные прогулки.
Рассматривая вопрос, как живут люди после удаления почки, нельзя не сказать о контрольных обследованиях. После операции в течение первого года УЗИ брюшной полости проводят каждые 3 месяца. Также пациенту необходимо сдавать биохимический анализ крови и делать рентгенографию легких. Если не наблюдается осложнений, в последующие годы профилактический осмотр следует проходить раз в 6 месяцев.
Инвалидность
Дают ли инвалидность при удалении почки – тема, которую затрагивают многие пациенты. Решение принимает специальная комиссия, направление на которую выдает лечащий врач. Каждую заявку рассматривают в индивидуальном порядке. В случае положительного ответа пациенту присваивается вторая или третья группа на один год. Проходить переосвидетельствование необходимо ежегодно.
Квалифицированную помощь в диагностике и лечении урологических заболеваний вам окажут в Государственном институте урологии. Подробную консультацию на любую тему предоставят лучшие специалисты Москвы.
Хроническая почечная недостаточность
Почечная недостаточность – симптомокомплекс, возникающий на фоне различных заболеваний почек из-за объемного поражения нефронов. Бывает острой и хронической. Если изменения в почечной ткани при острой почечной недостаточности преимущественно обратимы, то с хронической формой заболевания все гораздо сложнее.
В основе возникновения хронической почечной недостаточности (ХПН) лежит гибель главных рабочих клеток почки – нефронов. Несмотря на достаточно высокую компенсаторную способность почек, прогрессирующая гибель нефронов приводит к постепенному угасанию их функций и нарушению жизнедеятельности всего организма. Результатом данного состояния сначала является уменьшение размеров почек (сморщенная почка), а затем полный отказ органа.
Согласно статистике, хроническая почечная недостаточность диагностируется сегодня у 500 из одного миллиона пациентов, что не так уж мало. И с каждым годом в Москве число больных с таким диагнозом неуклонно растет.
Почечная недостаточность: причины развития
Спровоцировать почечную недостаточность может множество факторов, которые исключить из жизни современного человека просто невозможно. К появлению хронической почечной недостаточности в первую очередь приводят такие неприятные недуги, как хронический пиелонефрит и особенно хронический гломерулонефрит. Также почечная недостаточность часто возникает на фоне подагры, сахарного диабета, амилоидоза, красной волчанки и многих других системных заболеваний и ревматических процессов:
Причиной развития хронической почечной недостаточности также являются врожденные аномалии почек и заболевания сосудов, провоцирующие нарушения в почечном кровотоке.
Симптомы хронической почечной недостаточности
Несмотря на высокие компенсаторные способности почек (даже 10 % оставшихся дееспособными нефронов могут в организме поддерживать относительно нормальный водно-электролитный баланс), уже на первых стадиях хронической почечной недостаточности нарушается электролитный состав крови, развивается ацидоз (закисление), в организме нарушается обмен белка и начинают накапливаться продукты метаболизма: креатинин, мочевина, мочевая кислота.
ХПН характеризуется прогрессирующим течением и имеет четыре основных стадии развития:
Независимо от причины заболевания, клиническая картина хронической почечной недостаточности одинаковая. Симптоматика нарастает с каждой стадией болезни. На первом этапе ХПН человек может даже не подозревать о наличии проблемы, поскольку патология проявляет себя не слишком специфичными жалобами – бессонницей, снижением аппетита, быстрой утомляемостью. Обычно такая симптоматика просто остается без внимания и списывается на простую усталость после трудового дня.
Компенсированная стадия почечной недостаточности приносит усиление симптомов, кроме того, картина дополняется новой симптоматикой:
Дальнейшее развитие хронической почечной недостаточности отличается еще большим снижением компенсаторной способности почек. Нарастают симптомы интоксикации, резко снижается диурез, кожа становится сухой, желтушной, истончается, теряется мышечная масса, появляется анемия, отеки, возникает устойчивое повышение артериального давления, одышка.
Если на начальных стадиях ХПН патологический процесс еще можно контролировать медикаментозно и при помощи специальной диеты, то терминальная стадия хронической почечной недостаточности сопровождается необратимыми изменениями в тканях почек и падением их фильтрационной возможности до минимума. В этом случае пациенты нуждаются в регулярном проведении гемодиализа и, в идеале, в трансплантации почки.
Диагностика
При подозрении на ХПН обязательно требуется консультация нефролога и проведение ряда лабораторно-инструментальных исследований. Самыми достоверными являются лабораторные пробы по Зимницкому, Ребергу, общие и биохимические анализы крови и мочи. Для постановки такого диагноза, как хроническая почечная недостаточность, основанием является:
На УЗИ, КТ или МРТ почек выявляется уменьшение их размера и выраженное снижение толщины паренхиматозной ткани, а эходоплерография сосудов почек демонстрирует снижение почечного кровотока.
Мощная диагностическая база Клиники Современной Медицины позволяет проводить комплексное обследование на ХПН и оперативно получать результаты, необходимые для установления правильного диагноза. Объем необходимых исследований специалисты клиники определяют на первичной консультации.
Лечение хронической почечной недостаточности
Современная нефрология располагает широкими возможностями в лечении хронической почечной недостаточности. Применение инновационных терапевтических методик позволяет принципиально изменить качество лечения ХПН и значительно замедлить прогрессирование болезни. Врачи нашей Клиники для лечения хронической почечной недостаточности в додиализной стадии применяют самые передовые медикаментозные и физиотерапевтические методики, позволяющие затормозить развитие болезни и минимизировать выраженность проявлений почечной недостаточности.
Терапевтическую схему врач-нефролог подбирает в каждом клиническом случае строго индивидуально, в зависимости от стадии заболевания, основной причины развития ХПН, клинической картины и ее выраженности, возраста пациента и общего состояния его здоровья. Терапевтические мероприятия направлены на устранение симптоматики, компенсацию уремии и нормализацию гемостаза. Немаловажную роль в лечении хронической почечной недостаточности играют диета и питьевой режим.
Следует помнить, что консервативное лечение демонстрирует высокие результаты только на начальных стадиях ХПН, когда отсутствуют необратимые изменения в почках. Поэтому пациентам, страдающим различными заболеваниями мочевыводящей системы, так важно регулярно обследоваться у нефролога, ведь даже минимальные исследования – анализы крови и мочи – дают достаточно информации о состоянии почек.
Наш медицинский центр оказывает самый широкий спектр услуг. Вы всегда можете обратится к нам по вопросам лечения нефрологических заболеваний. Мы готовы оказать вам услуги лечения хронического гломерулонефрита и лечения хронического интерстициального нефрита.
Креатинин после удаления почки вырос что делать
Наблюдения проведены у103больных за 2010-2012 гг., оперированных по поводу различных заболеваний почки, приведшей кнефрэктомии. Всем больным проводились вдинамике клинические анализы крови, мочи, УЗИ почек иЭКГ исследования. Первую группу (62) составили больные, направленные непосредственно из стационарного этапа на санаторно-курортное долечивание. Во вторую группу вошли 41пациентов, не получавших реабилитационные мероприятия вусловиях санатория. Под влиянием комплексного санаторного лечения убольшинства пациентов наблюдалась благоприятная динамика клинических проявлений ввиде нормализации сниженного аппетита, исчезновения запоров итошноты, астенического синдрома, отсутствие нарушений психоэмоционального статуса, повышенной утомляемости. Вгруппе сравнения, без курса санаторной реабилитации, втечение срока наблюдения убольшинства пациентов отмечались астеноневротический, болевой синдромы, диспепсические нарушения.
Актуальность проблемы. Внастоящее время частота нефрэктомий колеблется от 39 % до 60 % от общего числа выполняемых операций на почках, особенно при мочекаменной болезни.
Функциональное состояние оставшейся почки впослеоперационном периоде, вкакой-то степени оказывается нарушенной, которая зависит от многих причин. Узначительного числа пациентов развивается хронический пиелонефрит, нередко наблюдается нефролитиаз, реже– опухоли итуберкулез [1]. Выделительная функция единственной почки нарушается, часто возникает артериальная гипертензия (АГ), развивается ряд сопутствующих заболеваний, отягощающих общее состояние пациентов. Все это требует своевременной иэффективной реабилитации оперированных, что способствует первичной ивторичной профилактики ряда заболеваний единственной почки, атакже экстранефральной патологии [2, 3].
Целью исследования явилась разработка эффективных комплексов восстановительного лечения больных после нефрэктомии сиспользованием минеральных вод сучетом клинико-функциональных особенностей послеоперационного периода.
Материал иметоды. Наблюдения проведены у103больных за 2010-2012гг., оперированных по поводу различных заболеваний почки, приведшей кнефрэктомии, среди которых наиболее частыми оказались: мочекаменная болезнь, острый осложненный пиелонефрит, осложненный гидронефроз, травмы иранения почки. Средний возраст оперированных –45,0±5,3лет, женщин – 57, мужчин – 46.
Всем больным проводились вдинамике клинические анализы крови, мочи, УЗИ почек иЭКГ исследования. Определяли общий белок ибелковые фракции, уровни креатинина имочевины всыворотке крови, клиренса эндогенного креатинина или скорости клубочковой фильтрации, концентрационной способности почки. По показаниям проводили хромоцистоскопию, внутривенную урографию.
В зависимости от проводимой терапии вотдаленном послеоперационном периоде, оперированные разделены на две группы.
Первую группу (62) составили больные, направленные непосредственно из стационарного этапа на санаторно-курортное долечивание. Во вторую группу вошли 41пациентов, не получавших реабилитационные мероприятия вусловиях санатория.
Для восстановительной терапии для больных первой группы разработан лечебный комплекс, включающий лечебное питание по системе Института питания АМН РФ, режим двигательной активности, соответствующий состоянию больного, лечебную физкультуру, внутренний прием минеральной воды. Казанчинская минеральная вода (санаторий Танып), относящаяся кгидрокарбонатно-сульфатным натриево-кальциевым маломинерализованным водам, атакже минеральные ванны из этой же воды.
Минеральная вода назначалась за 45-60минут до еды 3раза вдень по 200-250мл на каждый прием. Процедуры минеральных ванн проводились при t=37°C через день, 8-10сеансов на курс лечения.
Больные второй группы (сравнения) наблюдались вамбулаторно-поликлинических условиях без получения специальных реабилитационных мероприятий.
Статистический анализ полученных результатов проведен сиспользованием программы Statistic for Windows v.6.0.
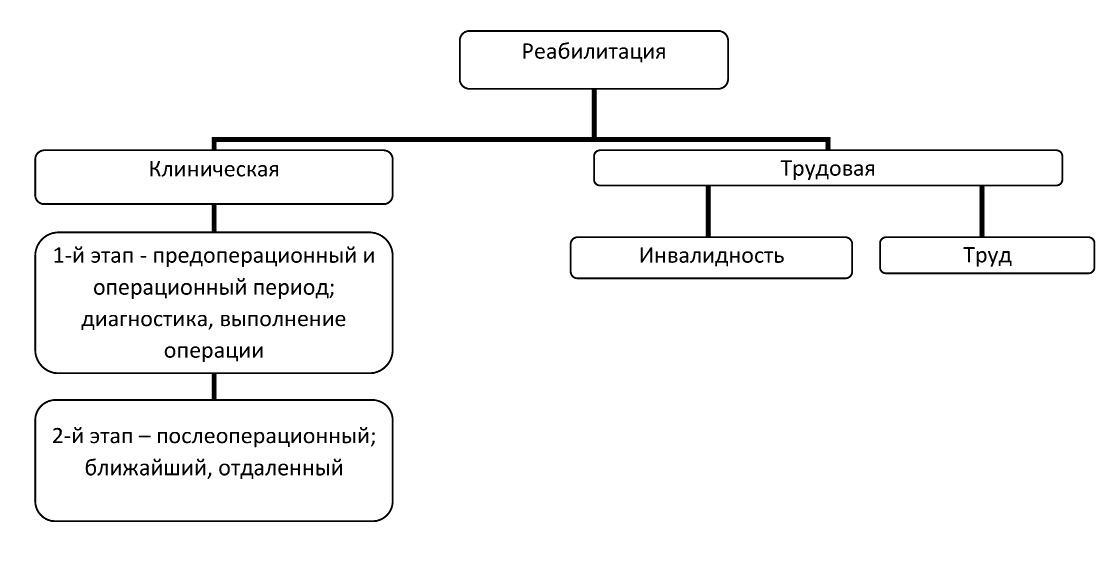
Клиническую реабилитацию пациентов после нефрэктомии разделяем на 2периода:
1.Предоперационный иоперационный периоды включает установку иуточнение диагноза: подготовку пациента коперации, выполнение оперативного вмешательства идинамическое наблюдение.
2.Послеоперационный период (до 12месяцев после операции)– включает лечебные мероприятия, проводимые пациенту после оперативного вмешательства до восстановления пациентом трудоспособности. Взависимости от тяжести состояния больного ифункции единственной почки больным рекомендовали труд или инвалидность. Этот период включает 2этапа:
–ближайший послеоперационный период (от момента окончания операции до 20суток):
–отдаленный послеоперационный период (от 20дней до 12месяцев).
1этап– предоперационный, включал всебя: оценку жалоб пациента, результатов обследований, помогающих врачу сформулировать клинический диагноз иопределить показания кдинамическому наблюдению ик операционному лечению. Сцелью снижения интра- ипослеоперационных осложнений пациентам, проводилась инфузионная, антибактериальная терапия, профилактика тромбозов. Эластическое бинтование нижних конечностей проводится всем пациентам без исключения.
2этап: послеоперационный период включает лечебные мероприятия смомента операции до восстановления пациентом трудоспособности.
Первые сутки после операции всем больным назначалась диета №0, со вторых суток– диета №1, споследующим переходом с3суток на диету №15(по М.И. Певзнеру).
В раннем послеоперационном периоде проводилась обязательная постоянная катетеризация мочевого пузыря катетером Фоллея сцелью устранения внутрипузырного давления иисключения пузырно-мочеточникового рефлюкса.
При стерильном посеве мочи враннем послеоперационном периоде используются цефалоспорины 2-3-го поколений (цефотаксим, цефтриаксон) по 1,0г. х1-2раза, внутримышечно всуточных дозах, сроком 7-10дней.
Активизация пациентов после выполнения нефрэктомии проводилась на 3-4-е сутки. Косметический шов снимался на 10-е сутки после операции. Больной выписывался на 20сутки инаправлялись на санаторный этап долечивания.
После выписки из стационара пациенты продолжали принимать по показаниям– уросептики, срегулярным контролем общего анализа мочи, сучетом результатов исследования посевов мочи (1раз вдве недели). Также по показаниям назначались спазмолитики илитолитики.
За время нахождения всанатории больные, после нефрэктомии, получали разработанную методику лечения.
При анализе лабораторных данных выявлено возрастание концентрации гемоглобина вкрови, снижение креатинина крови, увеличение плотности мочи, увеличение минутного диуреза (табл.1), что свидетельствуют об улучшении резервной функциональной возможности единственной почки.
Влияние разработанного лечения на функциональное состояние единственной почки
Жизнь при хронической почечной недостаточности
Как живут люди с хронической почечной недостаточностью? Если болезнь не на терминальной стадии, то пациенты проходят консервативное лечение. Стадию определяют по скорости клубочковой фильтрации (СКФ). При терминальной 5-й стадии она ниже 15 мл/мин/1,73м² — здесь уже требуется диализ или трансплантация почки. Хронической считают почечную недостаточность с 3-ей по 5-ю стадии — СКФ ниже 60 мл/мин/1,73м². На любой из них пациент должен вести особый образ жизни: соблюдать диету и ряд рекомендаций, назначаемых врачом.
В чем особенности жизни при ХПН и что делать
При хронической недостаточности почки перестают нормально выполнять свою функцию — выведение продуктов обмена с мочой. В результате они копятся в организме человека. В первую очередь это мочевина и креатинин. Именно по уровню последнего оценивают функцию почек. Высокий креатинин — это нарушение функции почек. Поэтому при ХПН важно регулярно сдавать анализы для проверки уровня этого продукта распада. Чтобы он не повышался, необходимо следовать ряду правил.
Избегать тяжелой физической нагрузки
Она повышает уровень креатинина. Это обусловлено тем, что данное вещество — конечный продукт креатин-фосфатной реакции в мышцах при их энергетическом обмене, работе и возникновении травм. Отсюда высокая физическая нагрузка — это высокий уровень креатинина, с которым и без того не работающие почки не могут справиться.
Ограничить белковые продукты
При хронической почечной недостаточности в диете ограничивают белок: при СФК ниже 50 мл/мин — до 30-40 г/сут., ниже 20 мл/мин — до 20-24 г/сут. Это необходимо, чтобы уменьшить нагрузку на почки. В то же время с началом диализа количество белка увеличивают до 1,1-1,5 г/кг/сут. Все потому, что в процессе диализа вымывается много важных компонентов, и белок на состояние почек влияет уже не так сильно.
Употреблять достаточно углеводов и жиров
Вместо белка в рационе должно быть достаточное количество углеводов и жиров. Основу рациона составляют сложные углеводы, которые не повышают глюкозу и медленно всасываются, и ненасыщенные жиры, полезные для сердца и сосудов.
Соблюдать калорийность рациона
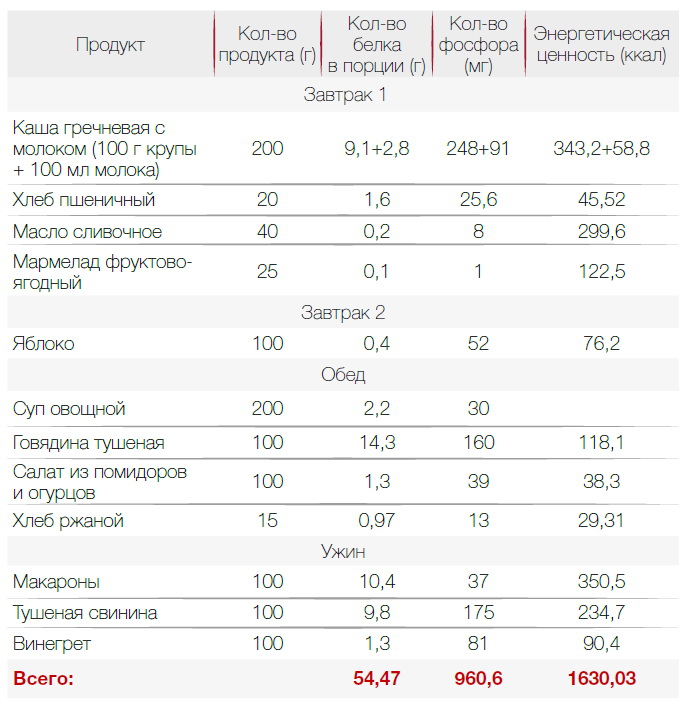
В диете при хронической почечной недостаточности важна калорийность. Она должна быть высокой — около 3000 ккал для восполнения всех витаминов и минералов. Диета назначается индивидуально, поэтому 3000 ккал — ориентировочное число. Пример меню с учетом требований приведен ниже.
Контролировать поступление микроэлементов и воды
Поскольку почки плохо работают, они не выводят калий, а от его избытка нарушается работа сердца. Поэтому количество калия, поступающего с пищей, нужно контролировать. Он содержится в картофеле и других овощах. Чтобы снизить количество калия, эти овощи перед приготовлением нужно порезать и замочить на 6-10 часов, причем как можно чаще воду менять.
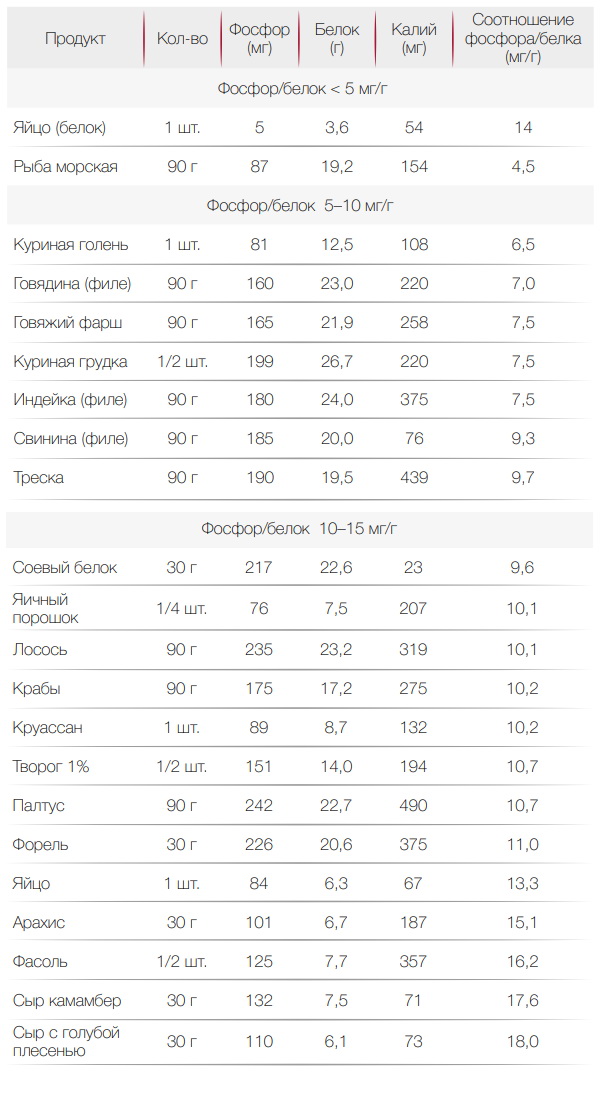
Еще необходимо ограничить поступление фосфора. При ХПН он может привести к поражению костей и сердца. Фосфор содержится в белковой пище. В растительной тоже есть, но из нее фосфор усваивается хуже. Также его количество снижается при термической обработке пищи. Выбирая продукты, стоит обращать внимание на те, что имеют низкий фосфорно-белковый индекс — ниже 20 мг/г. Примеры продуктов питания при почечной недостаточности с таким индексом приведены в таблице.
Другое важное правило питания при ХПН — следить за питьевым режимом. При выраженных отеках приходится уменьшить количество выпиваемой воды. В таком случае нужно ежедневно в одно время, после опорожнения мочевого пузыря и кишечника взвешиваться. Если вес резко увеличился — значит произошла задержка жидкости. При ограничениях количества воды можно рассасывать кусочек льда, а с сухостью во рту поможет справиться полоскание, жевательная резинка, леденцы или долька лимона.
Контролировать артериальное давление
Кровяное давление нужно контролировать, оно должны быть на уровне не выше 130/80, максимальные показатели — 140/90. Для этого на диете при ХПН количество соли в день ограничивается 2-3 г в сутки. При развитии выраженной гипертензии необходимо перейти на бессолевую диету.
Чтобы уменьшить количество соли в сутки, можно следовать таким советам:
Полезные советы для пациентов с ХПН
Образ жизни пациента с хронической почечной недостаточностью действительно полон ограничений, но это помогает долгое время поддерживать организм в нормальном состоянии. Специалисты рекомендуют вести дневник питания, внося в него все употребляемые продукты. Этот дневник в дальнейшем может быть полезен и для врача, который сможет скорректировать рацион, если состояние вдруг ухудшилось.
На кухне под рукой всегда стоит держать таблицы с содержанием в продуктах всех микро- и макроэлементов и их энергетической ценности. Для более точных расчетов рациона нужно иметь кухонные весы. Все это поможет предотвратить повышение креатинина и ухудшение работы почек.
Всегда нужно учитывать, что приведенные советы носят общий характер. Для получения точных рекомендаций необходимо обратиться к врачу. В Государственном центре урологии вы можете получить помощь по полису ОМС. Диагностика и лечение будут для вас бесплатными. Просто запишитесь на прием в онлайн-форме или по контактному номеру клиники.
Варианты оценки почечной функции после органосохраняющих операций у пациентов с почечно-клеточным раком
Серегин А.В., Индароков Т.Р., Шустицкий Н.А., Серегин А.А.
Сведения об авторах:
ВВЕДЕНИЕ
Одной из самых актуальных проблем современной онкоурологии является радикальность лечения злокачественных опухолей почек. Оперативное лечение остается в настоящее время основным методом лечения почечно-клеточного рака (ПКР). С течением времени с появлением новых современных методов диагностики и, соответственно, с выявлением все большего количества локализованных форм рака почки возникла необходимость в пересмотре подходов к оперативному лечению и расширении показаний к выполнению органосохраняющего лечения ПКР [1].
После выполнения радикальной нефрэктомии существенно возрастает риск возникновения хронической почечной недостаточности, а также других осложнений со стороны сердечно сосудистой системы 2. Выбор резекции почки при локализованных формах ПКР представляется оправданным, особенно когда речь идет о перспективах дальнейшей жизни пациента. Остающаяся после нефрэктомии единственная почка в силу природных регенеративных способностей при отсутствии в ней патологических процессов в состоянии обеспечить выполнение основных функций поддержания гомеостаза [6]. Тем не менее даже исходно здоровая единственная почка в процессе жизни индивидуума способна поражаться различными болезнями, ведущими к нарушению ее основных функций. Поэтому пациент с единственной почкой не может рассматриваться как абсолютно здоровый, даже при условии радикального удаления опухоли в противоположном органе [7].
Несмотря на совершенствование и разработку различных оперативных и абляционых методик лечения рака почки остается открытым вопрос о функциональном состоянии почки после оперативного лечения 13. Наряду с достижением онкологических результатов сохранение почечной функции является основной задачей в лечении опухолевых заболеваний почек [14, 15]. Компенсаторные возможности почечной паренхимы зачастую играют негативную роль при снижении функции почки. Интенсивный характер противоопухолевого лечения как хирургического, так и консервативного приводит к истощению почечной функции, которая не всегда выявляется при применении рутинных методов диагностики [16]. Исследования последних десятилетий показывают, что хронические заболевания почек (ХЗП) распространены намного больше, чем это считалось ранее. По данным ряда авторов частота нефрологических осложнений при оперативном лечении онкологического процесса в почках достигает от 5–20% до 40–60% и даже, в некоторых случаях 80% [17, 18].
В связи с изложенным возникает необходимость в дополнительном обследовании пациентов, направленном на оценку почечной функции как в до-, так и в послеоперационном периоде [19, 20]. Одним из таких методов является динамическая нефросцинтиграфия (ДНСГ), которая в нашем исследовании была проведена всем пациентам.
Целью исследования явилось изучение с использованием ДНСГ функциональных результатов органосохраняющих операций с применением превентивного шва без пережатия почечной ножки, а также на фоне пережатия почечной ножки.
МАТЕРИАЛЫ И МЕТОДЫ
В основу работы положен анализ результатов обследования и лечения 150 больных с раком почки в стадиях pT1a-Т2аN0M0, в том числе с кистозными формами, которым в период с 2013 по 2017 гг. была выполнена резекция почки с применением превентивного шва без пережатия почечной ножки, а так же 25 пациентов, оперированных в тот же период со стадиями pT1a-Т2аN0M0, которым была выполнена резекция почки с тепловой ишемией. По данным послеоперационного гистологического исследования у всех пациентов были выявлены злокачественные опухоли почек.
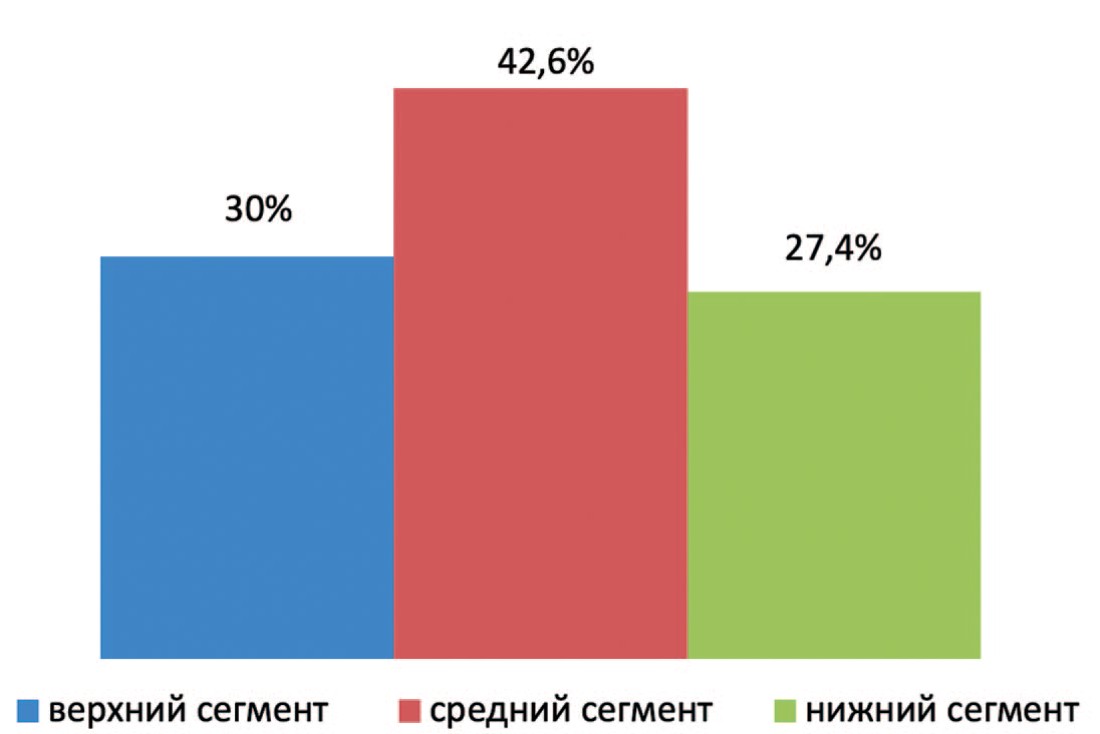
У 64 (42,6%) пациентов первой группы опухоль располагалась в среднем сегменте, опухоль верхнего сегмента выявлена у 45 (30%) пациентов и у 41 (27,4%) пациента опухоль располагалась в нижнем сегменте, что представлено на рисунке 1.
Рис. 1. Частота расположения опухолей в сегментах почки в первой группе
Fig. 1. Location of tumors in kidney segments in the 1-st group
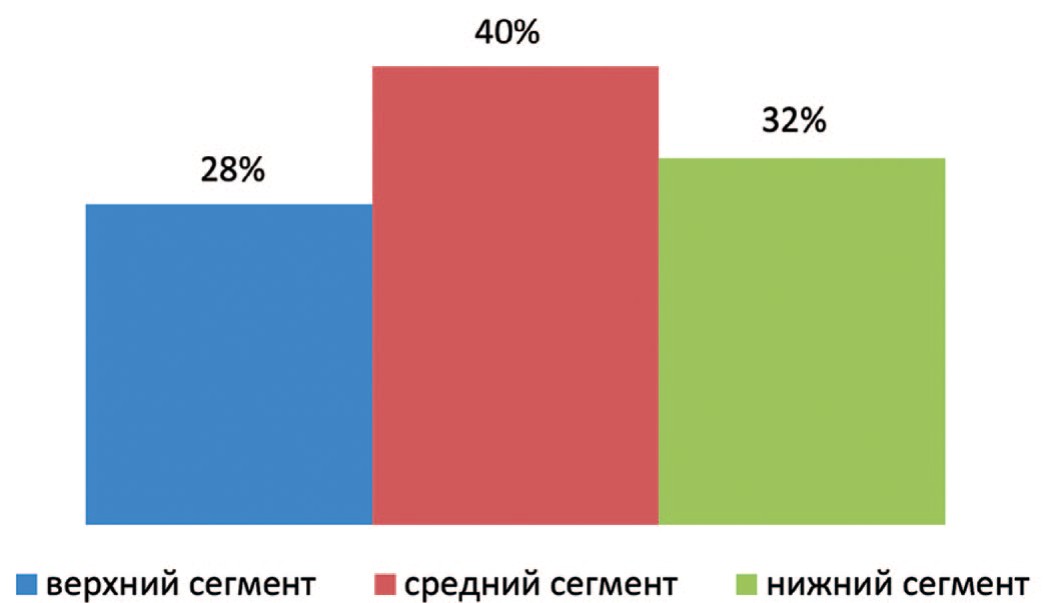
Во второй группе, также как в первой, у большей части пациентов опухолевый узел располагался в среднем сегменте – 10 (40%) человек, в верхнем сегменте – у 7 (28%) пациентов, и – у 8 (32%) пациентов в нижнем сегменте (рис. 2).
Рис. 2. Расположение опухолей по сегментам почки в группе сравнения
Fig. 2. Location of tumors by segment of the kidney in the comparison group
По стадиям опухолевого процесса пациенты в первой группе разделились следующим образом: стадия T1a была установлена у 74 пациентов, стадия T1b – у 53, стадия T2a – у 4-х. Также в наше исследование вошли 19 пациентов с кистозными опухолями почек (pT1). По абсолютным показаниям резекция почки выполнена 7,8% пациентам, по относительным – 91,2%. Во второй группе пациенты по стадиям распределились следующим образом: стадия T1a была установлена 16 пациентам, стадия T1b – 8, стадия T2a – 1 пациенту. В этой группе пациентов с кистозными опухолями почек не было.
С целью определения сложности предстоящей операции по данным компьютерной томографии (КТ) с контрастным усилением, нами была использована нефрометрическая шкала R.E.N.A.L. Согласно данным этой шкалы пациенты в обеих группах исследования были распределены на 3 группы риска: низкая группа тяжести – в первой группе 78 пациентов, во второй – 18; средняя группа тяжести – в первой 53 пациента, во второй – 6; а тяжелая группа – в первой 19 пациентов, во второй – всего лишь 1.
Основным методом, с помощью которого производилась оценка почечной функции в нашем исследовании, была ДНСГ. Радионуклидные методы исследования почек in vivo в большинстве онкологических клиниках не входят в протокол обязательного скринингового исследования и используются только в качестве вспомогательных методов, однако в разработанном нами алгоритме оценки почечной функции ДНСГ является одним из основных.
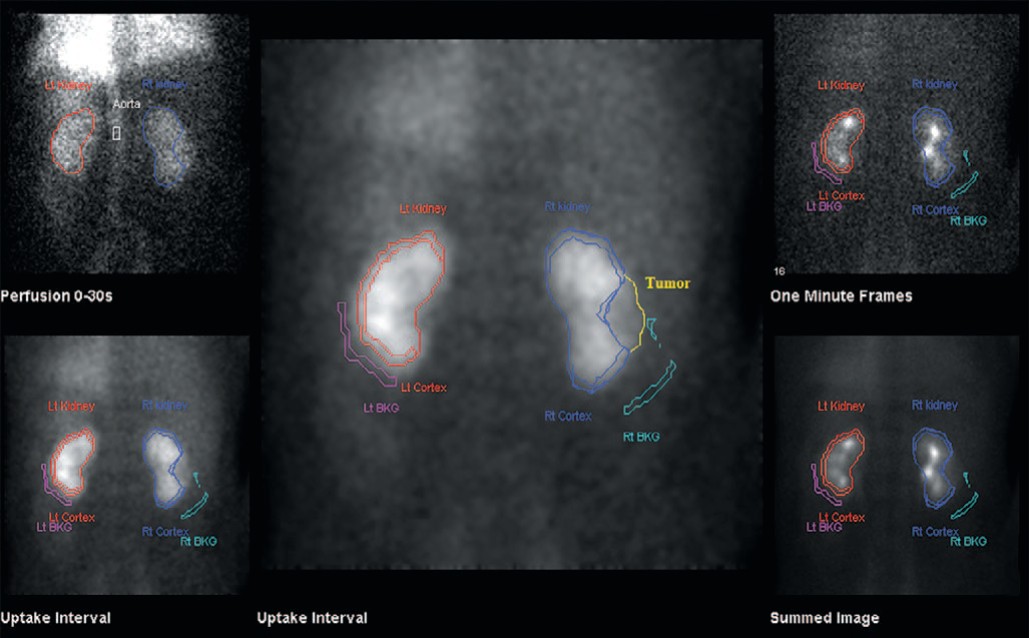
Основными показателями для оценки функции пораженной почки были следующие: перфузионный индекс (ПИ), ренальный индекс (РИ) до операции, скорость клубочковой фильтрации (СКФ), время максимального накопления радиофармпрепарата (РФП) в паренхиме (Tmax), средняя площадь функционирующей паренхимы. Расчет показателей проводился с помощью ДНСГ с непрямой изотопной ангиографией до операции и через 1 месяц после оперативного лечения. ДНСГ выполнялась на гаммакамере Infinia Hawkeye 4 GE по стандартной методике с использованием РФП – Тс99m – ДТПА (пентатех, ОАО «Диамед») 370 Мбк внутривенно болюсно. Проводилась визуальная оценка распределения РФП на паренхиматозной и сосудистой фазе исследования. На рисунке 3 представлен результат ДНСГ с дефектом накопления в проекции среднего полюса правой почки, выявленный в паренхиматозной фазе исследования, обусловленного опухолью.
Рис. 3. Динамическая нефросцинтиграфия. Опухоль среднего сегмента левой почки
Fig. 3. Dynamic nephroscintigraphy. Tumor of the middle segment of the left kidney
Статистический анализ не проводился. В исследовании приведены данные дополнительных обследований, проведенных всем пациентам, не требующих проведения статистического анализа.
РЕЗУЛЬТАТЫ
Всем 175 пациентам выполнены органосохраняющие операции. Средняя продолжительность оперативного лечения и объем средней кровопотери в обеих группах была одинаковой, и составили 130±40 мин. и 250±70 мл, соответственно. В первой группе пациентов не проводилось пережатия почечной ножки ни в одном случае. Среднее время тепловой ишемии во второй группе составило 13±2 мин. Результаты оперативного вмешательства представлены в таблице 1.
Таблица 1. Результаты оперативного лечения
Table 1. Results of surgical treatment
| Показатель Index | Группа 1 group 2 | Группа 2 group 2 |
|---|---|---|
| Продолжительность операции, мин. Duration of surgery,min | 120±40 | 1250±35 |
| Среднее время общей анестезии, мин. Average time of general anesthesia, min | 130,5±15 | 130,7±11 |
| Средний объем кровопотери, мл. Average blood loss, ml | 170±70 | 110±80 |
| Средний уровень гемоглобина, г/л Average hemoglobin level, g/l | 114±10 | 110±10 |
| Средний уровень креатинина, мкмоль/л Average creatinine levels, mmol/l | 86±15 | 93±10 |
| Средний уровень мочевины, мкмоль/л Average level of urea, mmol/l | 5,4±2 | 6,0±2,5 |
| Время ишемии Ischemia time | 0 | 13±2 |
Всем пациентам в до– и послеоперационном периоде проводилось лабораторное обследование, в том числе определение уровня креатинина и мочевины. При этом достоверно значимых различий по лабораторным показателям в обеих группах выявлено не было, что свидетельствует о необходимости определения функции почки в послеоперационном периоде не только по данным лабораторного обследования.
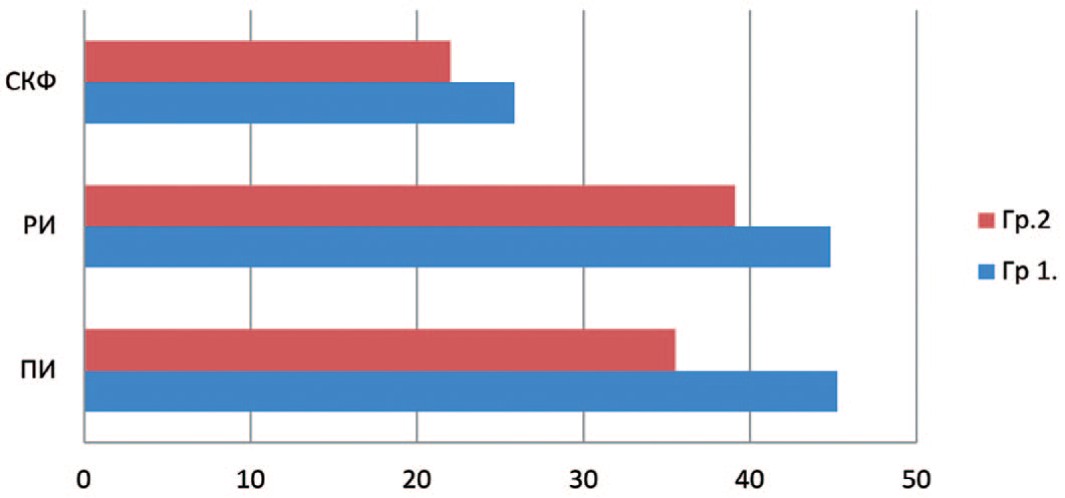
Через 1 месяц после оперативного вмешательства всем пациентам была выполнена динамическая сцинтиграфия. У больных первой группы отмечено незначительное снижение основных показателей функционального вклада и перфузии пораженной почки: ПИ составил 45,23±3% (до операции 54,13±2), РИ – 44,82±2,39% (до операции 53,24±4), СКФ – 25,84±1,7 мл/мин (до операции 33,84±2), что не выходит за пределы допустимых различий, связанных с ослаблением гамма-излучения Тс99m в мягких тканях при различной глубине залегания РФП в почках. Время максимального накопления РФП в среднем составило 3,6±1,5 мин. (до операции 3,3±1). Данные показатели также находятся в пределах нормальных значений. У пациентов второй группы отмечены более низкие значения показателей, что связанно с тепловой ишемией: ПИ составил – 35,5±3,3% (до операции 48±2,5%), РИ – 39,1±1,4% (до операции 46,3±26%), при этом отмечено снижение более чем на 10 единиц СКФ – до операции средний показатель составлял 36 мл/мин, после операции 22 мл/мин. Уровень суммарной СКФ до операции составлял 79,3 мл/мин, однако через 1 месяц после оперативного лечения выявлено значительное снижение СКФ до 47 мл/мин (рис. 4).
Рис. 4. Функциональное состояние почек в послеоперационном периоде у больных сравниваемых групп
Fig. 4. The functional state of the kidneys in the postoperative period in patients of the compared groups
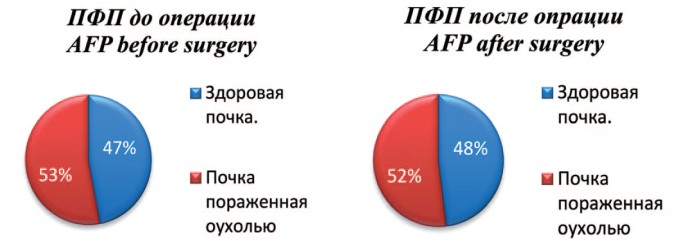
С целью визуальной оценки изменений в площади почечной паренхиме, ниже представлены рисунки, которые в процентом соотношении показывают изменения в почечной паренхиме без ишемии с использованием нашей методики, и даже с кратковременной ишемией, по отношению к здоровой почке. Одним из основных показателей, заслуживающих внимания, является площадь функционирующей паренхимы (ПФП), которая оценивалась по данным ДНСГ в до- и послеоперационном периоде. Средняя площадь функционирующей паренхимы в первой группе до операции составила 53±10%, а после операции 52±10% (рис. 5).
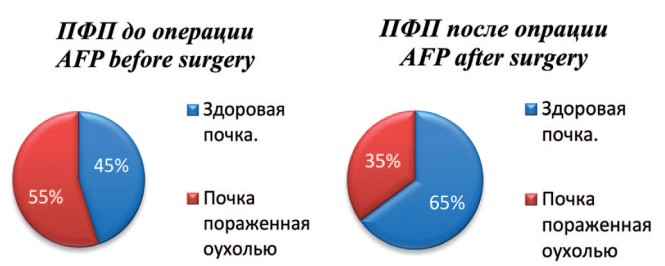
Во второй группе отмечено выраженное снижение ПФП по сравнению с дооперационными показателями: 55±7%, против 35±9%. При этом обращает на себя внимание выраженное увеличение ПФП до 65±5см2, что свидетельствует о ее гиперфункции (рис. 6).
Рис. 5. Соотношение площади паренхимы здоровой и оперированной почек до и после оперативного лечения в 1 группе
Fig. 5. The ratio of the parenchyma area of healthy and operated kidneys before and after surgical treatment in group 1
Во второй группе отмечено выраженное снижение ПФП по сравнению с дооперационными показателями: 55±7%, против 35±9%. При этом обращает на себя внимание выраженное увеличение ПФП до 65±5см2, что свидетельствует о ее гиперфункции (рис. 6).
Рис. 6. Соотношение площади паренхимы здоровой и оперированной почек до и после оперативного лечения в группе сравнения
Fig. 6. The ratio of the parenchyma area of healthy and operated kidneys before and after surgery in the comparison group
ВЫВОДЫ
Даже кратковременная ишемия во время выполнения органосохраняющих операций ведет к значительному снижению функции почки, пораженной опухолью. При этом далеко не всегда стандартные лабораторные методы (определение уровня креатинина, мочевины и клиренса креатинина) позволяют в послеоперационном периоде вовремя диагностировать нарушения их функции. Таким образом, на наш взгляд проведенное исследование демонстрирует необходимость в дополнительном обследовании – динамической нефросцинтиграфии, которая позволяет оценить функциональный вклад именно оперированной почки у больных в послеоперационном периоде.