Кровоток в сма что это
Кровоток в сма что это
Плод с задержкой внутриутробного развития является плодом, который не достигает своих потенциально возможных параметров роста. Факторами, влияющими на возникновение неблагоприятного для него окружения, могут служить заболевания матери (сахарный диабет, гипертоническая болезнь, хронические заболевания почек, системные сосудистые коллагенозы или гестоз), а также курение, прием лекарственных препаратов или нарушение маточно-плацентарного кровообращения.
Нарушение формирования и поддержания адекватного маточно-плацентарного кровообращения является, вероятно, одной из наиболее широко распространенных причин возникновения ЗВРП. Однако у пациенток без факторов риска первопричина, приводящая к плацентарной недостаточности, может остаться неизвестной.
В большинстве случаев ЗВРП не повторяется в последующей беременности. Однако в некоторых случаях она формируется во всех следующих беременностях (так называемая идиопатическая повторяющаяся ЗВРП).
Плоды с задержкой внутриутробного развития имеют более высокий риск неблагоприятного перинатального исхода по сравнению с нормальными или конституционально маловесными плодами. Ультразвуковая допплерометрия помогает идентифицировать тех плодов, у которых меньшие размеры обусловлены именно плацентарной недостаточностью.
Оценка скоростей кровотока у плода
У некоторых плодов может регистрироваться снижение диастолического кровотока, которое остается постоянным по мере увеличения срока беременности и никогда не становится нулевым или отрицательным, что может быть следствием легкой формы плацентарной недостаточности.
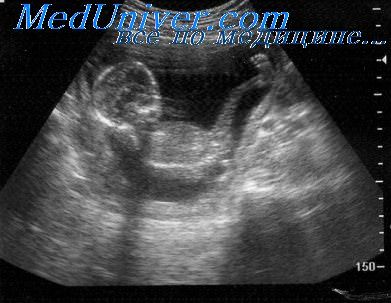
Эксперименты на животных и человеке показали, что при ЗВРП кровообращение головного мозга увеличивается. Это увеличение кровотока может быть диагностировано с помощью допплерометрического исследования СМА. Данный эффект был назван эффектом защиты головного мозга (brain sparing effect), который проявляется низкими значениями ПИ в его сосудах. Важно подчеркнуть, что значения ПИ в СМА изменяются с возрастанием срока при физиологическом течении беременности.
Эффект защиты головного мозга может быть непродолжительным, как это было показано в экспериментах на плодах животных с длительной гипоксемией; в частности, при истощении компенсаторных возможностей в ответ на сильный стресс у плода человека также может теряться способность к проявлению данного защитного эффекта.
Было выявлено, что ПИ СМА находится ниже нормативных значении, когда снижается РО2. Максимальное снижение ПИ регистрируется, когда РО2 у плода находится в пределах от 2 до 4 стандартных отклонений ниже нормативных значений для соответствующего гестационного возраста.
Когда дефицит кислорода становится еще больше, появляется тенденция к увеличению ПИ, что предположительно связано с развитием отека головного мозга.
Исчезновение эффекта защиты головного мозга и/или наличие отрицательного (обратного) диастолического кровотока в СМА у плодов с задержкой внутриутробного развития указывает на критическую ситуацию и является предвестником его гибели.
Это было подтверждено результатами исходов у таких плодов в ситуациях, когда родители отказывались от экстренного родоразрешения. К сожалению, для того чтобы доказать эту концепцию, необходимо проведение лонгитудинальных типов исследований на плодах с тяжелой степенью задержки развития вплоть до их агонального состояния. Отрицательный (обратный) кровоток в профиле КСК в СМА может наблюдаться при физиологической беременности в результате сдавления головки плода.
Кровоток в сма что это
Скорость кровотока по средней мозговой артерии (СМА) контрлатеральной стороны мозга при функциональной мышечной пробе должна возрастать [2, 5, 10, 11]. Такой прирост объясняли увеличением минутного объёма сердечного выброса, повышением уровня системного артериального давления, а также накоплением в крови углекислоты. Действительно, при увеличении физической нагрузки скорость кровотока по СМА становилась выше на 25-30 %, однако в дальнейшем, при превышении максимального вентиляционного порога, начинала снижаться [1, 8, 10].
С помощью метода позитронно-эмиссионного анализа показано так же стимулирующее влияние на активность мозговых структур при воздействии на ткани конечностей болевого фактора [3, 9, 12, 13]. Установлено, что при болевом воздействии на контрлатеральную конечность у обследуемых 18-35 лет реакцию увеличения скорости кровотока по СМА на 40-50 % можно в значительной степени нивелировать при применении анестетиков [6, 7], что подтверждает рефлекторный механизм наблюдающегося ускорения мозгового кровотока. У пожилых людей уменьшение скорости мозгового кровотока рассматривают как причину возрастного ограничения скорости локомоций и связывают с падением чувствительности сосудов головного мозга к углекислоте [12].
Ещё сложнее найти взаимосвязь показателей скорости мозгового кровотока и интеллектуальных способностей пожилых людей. Не менее интересен вопрос о наличии такой взаимосвязи у людей с ограниченными физическими возможностями, а также у работников физического труда и спортсменов.
Количественный анализ реакции мозговых артерий на дополнительную работу мышц во время лечения больных важен для определения возможности их ранней мобилизации, определения объема двигательной активности, перевода стационарных пациентов на амбулаторный режим лечения. Практическое значение реакции сосудов мозга при функциональной пробе в травматологии связано с рекомендацией автора метода лечения больных применять функциональное нагружение оперированной конечности с первых дней после остеосинтеза [4].
Целью настоящего исследования явилась проверка гипотезы о причине возрастного снижения скорости кровотока по СМА, возникающего как условие сохранения резерва функциональной адаптации сосудистого русла, необходимого для поддержания механизма ауторегуляции мозгового кровотока и работоспособности человека.
Материалы и методы исследования
Исследование скорости кровотока по СМА проводилось с помощью метода ультразвуковой допплеровской флоуметрии с датчиком с несущей частотой 2 МГц. При этом у больных после записи скорости мозгового кровотока в покое повторно выполняли записи при сжимании эластического эспандера правой и затем левой кистью. Для оценки работоспособности обследуемых, снижающейся у пациентов под влиянием болевого фактора, использовали психо-физиологический тест SF-36.
Обследованы 30 больных с отставанием в росте одной из нижних конечностей на величины от 2 до 15 см в возрасте от 5 до 62 лет. Исследования выполнены до и в процессе оперативного удлинения сегментов конечности по методу Илизарова. Контрольную группу составили 30 практически здоровых людей 18-60 лет.
Результаты исследования и их обсуждение
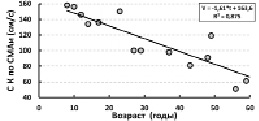
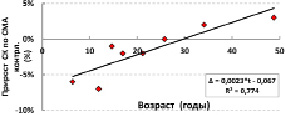
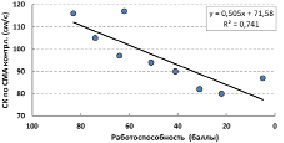
У здоровых людей с увеличением возраста (t, годы) наблюдалось снижение скорости кровотока по СМА: V = 102 – 0,48*t; R² = 0,350. Ещё более быстро происходило возрастное снижение скорости кровотока по СМА у больных с ортопедической патологией (рис. 1). Выявлено возрастное увеличение степени прироста скорости кровотока по СМА при проведении функциональной мышечной пробы (рис. 2). Следовательно, чем меньше абсолютные значения скорости кровотока, тем больше её прирост. В таком случае, возрастное снижение показателя обусловлено необходимостью сохранения резервов функциональной адаптации сосудистого русла для осуществления ауторегуляции мозгового кровотока при изменениях потребностей тканей в кислороде.
Рис. 1. Возрастная динамика скорости кровотока по СМА контрлатеральной стороны мозга у больных с отставанием одной из конечностей в продольных размерах
Рис. 2. Возрастная динамика изменения скорости кровотока по СМА при проведении функциональной мышечной пробы
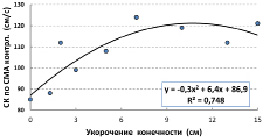
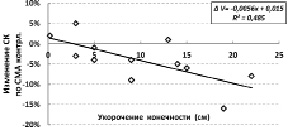
У больных с отставанием в продольном росте одной из конечностей соотношение величин скорости мозгового кровотока на контрлатеральной и ипсилатеральной сторонах зависел от тяжести заболевания. По мере увеличения тяжести патологии скорость кровотока по СМА контрлатеральной стороны возрастала (рис. 3). При этом с увеличением тяжести патологии изменение показателя скорости кровотока становились все меньше (рис. 4), то есть имелась обратная взаимосвязь величин скорости кровотока по СМА и прироста показателя при проведении функциональной мышечной пробы:
?V = – 0,0039*v + 0,38; R² = 0,739.
Рис. 3. Скорость кровотока по СМА контрлатеральной стороны от величины укорочения конечности
Рис. 4. Зависимость изменения СК по СМА контрлатеральной стороны при проведении мышечной пробы от величины укорочения конечности
Рис. 5. Влияние снижения работоспособности под действием болевого фактора на скорость кровотока по СМА контрлатеральной стороны
В процессе оперативного удлинения конечности при приобретенной патологии скорость кровотока по СМА контрлатеральной стороны не увеличивалась, а при врожденной снижалась со 113 ± 3 до 94 ± 5 см/с (p ≤ 0,01). Снижение показателя было тем более выражено, чем ниже была работоспособность, которую лимитировало действие болевого фактора (рис. 5).
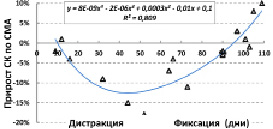
В этих условиях на протяжении лечения наблюдались отрицательные значения изменения показателя мозгового кровотока при выполнении функциональной мышечной пробы (рис. 6).
Рис. 6. Динамика изменений скорости кровотока по СМА контрлатеральной стороны в процессе лечения больных
Следовательно, в условиях действия болевого фактора даже при снижении абсолютных значений скорости по СМА реакция на дополнительную соматическую афферентацию не приводило к ускорению кровоснабжения мозга. Работоспособность пациентов оказывалась существенно сниженной.
Выводы
1. Выявленное возрастное снижение скорости кровотока по средним мозговым артериям у здоровых людей и у пациентов с патологией опорно-двигательного аппарата является необходимым условием сохранения ауторегуляции мозгового кровотока.
2. При оперативном удлинении конечности, несмотря на снижение абсолютных значений скорости мозгового кровотока, не произошло сохранение резерва функционального резерва адаптации сосудистого русла мозга, выявляемого при функциональной пробе, работоспособность пациентов оказалась сниженной.
Сосудистая патология головного мозга
Проблема сосудистых заболеваний головного мозга является социально значимой. Главной причиной цереброваскулярной патологии (от начальных признаков недостаточности мозгового кровообращения до инсультов) остаются артериальная гипертензия и атеросклероз. Неврологи Юсуповской болезни диагностируют церебральную ишемию, гипоплазию ПМА и асимметрию кровотока головного мозга с помощью новейшей аппаратуры ведущих мировых производителей.
Врачи клиники неврологии применяют для лечения пациентов новейшие лекарственные препараты. При ишемии в области бассейна ПМА длительность восстановления зависит от степени нарушения кровоснабжения мозга и адекватности реабилитационных мероприятий. Специалисты клиники реабилитации для восстановления кровотока по ПМА используют физиотерапевтические процедуры, массаж, иглотерапию, нетрадиционные методы восстановительной терапии.
Асимметрия кровотока по СМА и ПМА может закончиться ишемическим инсультом. В Юсуповской больнице проводят комплексную терапию патологии, в результате которой восстанавливается кровоток и мозговая ткань получает достаточное количество питательных веществ и кислорода. Тяжёлые случаи ишемии в бассейне ПМА обсуждаются на заседании Экспертного Совета с участием профессоров и врачей высшей категории. Ведущие неврологи коллегиально вырабатывают тактику ведения пациентов с нарушением кровообращения вследствие гипоплазии ПМА. Медицинский персонал внимательно относится к пожеланиям пациентов.
Сегменты
Что такое ПМА головного мозга? ПМА расшифровывается в медицине как передняя мозговая артерия. Схема кровоснабжения головного мозга довольно сложная. Кровь поступает в мозг по двум внутренним сонным и двум позвоночным артериям. Сонные артерии формируют каротидный бассейн. Они начинаются в грудной полости: правая от плечеголовного ствола, левая – от дуги аорты. Позвоночные артерии формируют вертебробазилярный бассейн. По ним кровь поступает в сосуды, обеспечивающие питание продолговатого мозга, шейного отдела спинного мозга и мозжечка. В результате слияния позвоночные артерии образуют основную базилярную артерию.
ПМА (передняя мозговая артерия) начинается у места разделения внутренней сонной артерии на концевые ветви. В начале своего пути она отдаёт ряд мелких веточек, которые проникают через переднее продырявленное вещество к базальным ядрам основания большого мозга. На уровне зрительного перекреста передняя мозговая артерия образует анастомоз (соустье) с одноимённой артерией противоположной стороны посредством передней соединительной артерии.
Гипоплазия ПМА
Причиной внезапной закупорки сосуда головного мозга часто является аномальное уменьшение его просвета. Виной тому являются не холестериновые бляшки, а гипоплазия артерии головного мозга – патологическое сужение сосуда. Заболевание наблюдается у 80% пожилых людей. У них к врождённому дефекту прибавляются возрастные изменения сосудов.
Гипоплазия ПМА – что это такое и как проявляется? Гипоплазия ПМА проявляется в недостаточном развитии правой мозговой артерии. Сосуд имеет аномальную форму. При такой патологии может нарушаться строение кровеносных сосудов, питающих внутричерепные структуры. Гипоплазия ПМА – врождённая патология, которая возникает внутриутробно. При гипоплазии ПМА нарушается питание мозжечка, ствола и затылочных долей. В результате патологии возрастает риск образования аневризмы либо развития инсульта. Гипоплазия ПМА – это опасное состояние, которому особое внимание уделяют неврологи Юсуповской больницы и нейрохирурги клиник-партнёров.
Причины, симптомы и лечение
На процесс формирования мозговых артерий, в том числе ПМА, негативно влияют следующие факторы:
Симптомы заболевания и их выраженность зависят от степени недоразвития сосуда, который питает головной мозг. У каждого пациента симптомы могут проявляться по-иному. Некоторые люди узнают о том, что у них гипоплазия ПМА, только во время медицинского осмотра. Часто заболевание протекает бессимптомно.
Гипоплазия ПМА может проявляться следующими симптомами:
Все перечисленные симптомы указывают на недостаточное мозговое кровообращение, поэтому при их возникновении обращайтесь к неврологам Юсуповской больницы. Врачи вначале проведут комплексное обследование, которое включает следующие диагностические процедуры:
Врачи сонологи используют современные ультразвуковые аппараты, совмещающие триплексный сканер и допплеровскую установку. Они позволяют визуализировать экстракраниальный и интракраниальные отделы артерий вертебрально-базилярного бассейна, выявить асимметрию кровотока по СМА и ПМА. Для определения состояния нейронов при ишемии мозга выполняют магнитно-резонансную и компьютерную томографию с помощью аппаратов премиум класса. КТ-ангиографию сосудов головного мозга в Юсуповской больнице делают на современном сканере. С помощью него получают не только пошаговые изображения сосудов головного мозга, но и их трёхмерную модель. Эти изображения могут просматриваю на мониторе компьютера, распечатывают на пленке или переносят на DVD+R диск.
Если симптомы нарушения мозгового кровообращения, вызванные дисплазией ПМА, выражены незначительно, проводят терапию лекарственными средствами, которые расширяют артерии и нормализуют мозговой кровоток. Консервативная терапия помогает снизить интенсивность головных болей и улучшить работу вестибулярного аппарата. При выявлении в аномальном сосуде тромба врач приписывает лекарства для его растворения. Нейрохирурги клиник-партнёров Юсуповской больницы проводят коррекцию патологии ПМА в случаях, когда при медикаментозном лечении отсутствует положительная динамика. Преимущественно при гипоплазии ПМА применяется методика стентирования.
Спазм сосудов головного мозга
Пожилых людей, лиц среднего и мозгового возраста часто беспокоит головная боль, шум и головокружение, повышенная утомляемость, ухудшение памяти, снижение работоспособности. Зачастую пациенты не очень серьезно относятся к таким жалобам. Между тем это могут быть признаки вазоспазма в левых мозговых артериях, СМА (средней мозговой артерии) и ПМА (передней мозговой артерии). Церебральный вазоспазм (сужение просвета артерий основания мозга после субарахноидального кровоизлияния при разрыве мешковидной аневризмы) может вторично вызвать ишемию мозга.
После разрыва аневризмы у пациента наступает временный период улучшения или стабилизации состояния до момента возникновения у него симптоматического вазоспазма. Неврологические симптомы спазма церебральных с четвёртого по четырнадцатый день после первого разрыва аневризмы. Возникшая неврологическая симптоматика соответствует ишемии мозга в специфических артериальных бассейнах. Выраженность церебрального вазоспазма определяет степень вероятности развития ишемии и инфаркта мозга.
Признаки вазоспазма в левых артериях мозга, СМА и ПМА часто возникают у тех пациентов, у которых на ранней магниторезонансной или компьютерной томографии головного мозга определялись слои свернувшейся крови толщиной 1 мм и больше в бороздах мозга или шарообразные сгустки крови размерами больше 5 мм 3 в базальных цистернах.
Локализацию и тяжесть вазоспазма в ПМА и СМА врачи Юсуповской больницы определяют с помощью магниторезонансной или компьютерной томографии. Чтобы прогноз был точным, компьютерную томографию головного мозга проводят в интервале от 24 до 96 ч после субарахноидального кровоизлияния.
Клинически выраженный церебральный вазоспазм проявляется симптоматикой, которая относится к тому или иному бассейну кровоснабжения головного мозга определённой артерии. При вовлечении ствола или основных ветвей средней мозговой артерии (СМА) у пациента развиваются следующие симптомы:
Признаки вазоспазма в левых артериях мозга, СМА и ПМА могут не быть выраженными из-за того, что в головном мозге формируется коллатеральный кровоток через сращения зон смежного мозгового кровоснабжения.
Ишемия вследствие вазоспазма ПМА проявляется абулией. Пациент находится в бодрствующем состоянии, лежит с закрытыми или открытыми глазами, с запаздыванием реагирует на инструкции. Он не может активно вести беседу, но на вопросы отвечает короткими фразами, которые произносит шёпотом, длительно пережёвывает пищу и часто удерживает её между дёснами и щекой. Все очаговые неврологические симптомы в результате церебрального вазоспазма у пациентов могут возникать внезапно, достигая максимальной выраженности в течение нескольких минут, или развиваются на протяжении нескольких дней.
Если ишемии или инфаркту подвергается вся территория мозга в бассейне СМА (средней мозговой артерии), то развивается его отёк, который может привести к повышению внутричерепного давления. Ранняя магниторезонансная или компьютерная томография головного мозга позволяют предсказать неблагоприятный исход, если обнаруживается крупный сгусток крови в сильвиевой цистерне или в просвете сильвиевой щели и второй значительный сгусток в базальной фронтальной щели, расположенной между полушариями мозга. Одновременное присутствие свернувшейся крови в этих областях сочетается с выраженным симптоматическим спазмом СМА и ПМА. В подобной ситуации поверхностные коллатерали в коре головного мозга от ПМА не в состоянии компенсировать ишемию в бассейне СМА.
Если спазм артерий головного мозга возникает на фоне субарахноидального кровоизлияния, медикаментозная профилактика и лечение неэффективно.
Поскольку у пациентов с церебральным вазоспазмом отмечается увеличение объёма крови и отёк паренхимы головного мозга, то даже незначительное увеличение внутричерепного объёма, которое происходит при воздействии вазодилататоров, может усугубить неврологические расстройства. Если у пациента установлен выраженный симптоматический церебральный вазоспазм, неврологи не назначают вазодилататоры.
Все усилия врачей направлены на увеличение мозгового перфузионного давления путём повышения среднего артериального давления. Достигается это увеличением объёма плазмы и назначением вазопрессорных препаратов (фенилэфрина, допамина). Поскольку лечение, направленное на увеличение перфузионного давления, приводит к улучшению картины неврологического статуса у некоторых больных, но высокое артериальное давление сопряжено с риском повторного кровоизлияния, при применении данного метода лечения неврологи Юсуповской больницы определяют давление церебральной перфузии и минутный сердечный выброс, проводят прямое исследование центрального венозного давления. В тяжёлых случаях у пациента измеряют внутричерепное давление и давление заклинивания лёгочной артерии.
Введение осмотического диуретика маннитола при поддержании адекватного внутрисосудистого объёма и среднего артериального давления увеличивает осмолярность сыворотки крови пациента. В тяжёлом случае для снижения внутричерепного давления используют барбитуратную кому.
Как лечить
Тонус церебральных артерий – это напряжение сосудистых стенок, которое поддерживается мышечной стенкой этих сосудов. Он является фактором, определяющим кровоснабжение тканей головного мозга. Благодаря мышечным стенкам церебральных сосудов ткани головного мозга защищаются от недостатка или переизбытка крови. При расстройствах нервной системы или заболеваниях внутренних органов тонус артерий может изменяться. Мышечная стенка артериальных сосудов спазмируется, их просвет уменьшается, как и объём крови, поступающей к нейронам. В результате гипертонуса развивается тканевая гипоксия (клетки головного мозга не получают достаточного количества кислорода и питательных веществ). Гипертонус ПМА, как и других церебральных артерий, вызывает органические и функциональные нарушения в головном мозге.
Патологический гипертонус ПМА возникает вследствие заболеваний внутренних органов, желез и метаболических нарушений. Продолжительный выраженный спазм артерий может привести к острому нарушению мозгового кровообращения (ишемическому инсульту), вследствие которого развиваются необратимые органические изменения тканей, последующая потеря двигательных функций и интеллектуальных возможностей.
К гипертонусу ПМА приводят следующие причины:
Вазоспазм ПМА проявляется следующими симптомами:
Редко в клинической картине вазоспазма ПМА наблюдается синкопальное состояние, однако особо сентиментальные люди даже от счастья могут терять сознание.
Комплексная терапия заболевания направлена на восстановление функции головного мозга и повышение работоспособности организма. Врачи Юсуповской больницы начинают лечение гипертонуса ПМА с терапии той патологии, которая вызвала повышение тонуса мозговых сосудов. Пациентам рекомендуют дозированный режим работы, отдыха, полноценный сон, ароматерапию. Следует сбалансировать питание: уменьшить употребление алкоголя, кофе и содержащих кофеин продуктов, исключить употребление тонизирующих напитков.
Перед сном рекомендуется принять тёплый душ или ванну, выпить чай из плодов шиповника или мяты с добавлением мёда. Медикаментозная терапия заключается стабилизации артериального давления, приёме фитопрепаратов, обладающих седативным эффектом. Для того чтобы пройти диагностику и лечение ишемии, гипоплазии и асимметрии кровотока ПМА головного мозга, записывайтесь на приём к неврологу, позвонив по телефону контакт центра Юсуповской больницы в любое время суток независимо от дня недели.
Как диагностируют и лечат спинальную мышечную атрофию
О спинальной мышечной атрофии (СМА) — тяжелом редком генетическом заболевании — стали активно говорить в обществе и СМИ лишь несколько лет назад, хотя само заболевание, конечно, известно науке давно. Впервые оно было описано в 1891 году австрийским неврологом Г. Верднигом и затем в 1892 году немецким неврологом Й. Гоффманом.
Сегодня оживление вокруг проблематики СМА вызвано тем, что лишь относительно недавно благодаря активному развитию фармацевтической промышленности и генной терапии появились препараты, способные существенно замедлить прогрессирование заболевания. До этого момента болезнь считалась неизлечимой, а постановка диагноза «СМА» была равноценна приговору.
В последние годы о СМА рассказывают пациентские и благотворительные организации, медицинские работники, СМИ, а отдельные люди и фонды собирают средства на покупку дорогостоящих лекарств для таких больных. В результате самое общее представление о СМА имеют и многие обычные люди, далекие от медицины. Например, знают, что оно связано с тяжелой инвалидностью, сильным ограничением подвижности и что цены на спасительные лекарства от СМА исчисляются десятками миллионов рублей.
Что сегодня известно о СМА науке? Почему лечение этой болезни так дорого стоит? Как сегодня живут пациенты с этим диагнозом? Давайте разбираться.
Автор статьи — Кристина Невмержицкая, врач-невролог, заведующая отделением неврологии Областной детской клинической больницы Екатеринбурга, медицинский эксперт благотворительного фонда «Семьи СМА»
Что такое СМА
СМА — это аутосомно-рецессивное нервно-мышечное заболевание, характеризующееся прогрессирующими симптомами вялого паралича и мышечной атрофии. СМА одно из самых распространенных редких (орфанных) заболеваний. Распространенность СМА составляет 1 на 6–10 тыс. новорожденных. Согласно официальным данным, в России сегодня 890 детей со СМА. Каждый год рождается около 200 детей с этим диагнозом [1].
При СМА из-за генетической поломки возникает недостаток особого белка SMN (survival motor neuron). Это провоцирует постепенную гибель α-мотонейронов спинного мозга, которые иннервируют скелетные мышцы и отвечают за их сокращение.
В синтезе белка SMN участвуют два гена — SMN1 и SMN2. Ген SMN1 основной, он кодирует 85% белка. Второй ген SMN2 — оставшиеся 15% белка. Таким образом, если из-за мутации ген SMN1 не работает, единственным источником информации о белке SMN становится ген SMN2. Однако у больных СМА разное количество копий гена SMN2. Чем больше таких копий, кодирующих белок SMN, тем, как правило, легче течение болезни и благоприятнее прогноз. Количество копий гена SMN2 устанавливается путем генетического анализа.
Глобально у всех больных СМА наблюдается прогрессирующая мышечная слабость, ухудшение или постепенная потеря амплитуды движений, нарушения дыхания и глотания. При этом у больных сохраняется интеллект, способность к обучению и выполнению профессиональных навыков.
Как наследуется СМА
СМА — генетическое заболевание с аутосомно-рецессивным типом наследования. Это значит, что родители ребенка со СМА могут быть носителями дефектного гена SMN1, при этом заболевание не проявляется, а сами они могут не подозревать о риске передать его потомству. В случае если оба родителя передадут поврежденный ген ребенку, СМА разовьется у него с вероятностью 25%.
Если же ребенок получит поврежденный ген только от одного родителя, то не будет иметь симптомов заболевания, а так же, как и родители, будет носителем этого дефектного гена. Вероятность этого составляет 50%.
Типы СМА
В настоящее время принято выделять несколько типов спинальной мышечной атрофии на основании возраста появления первых симптомов и максимальных двигательных умений больного. Каждый тип при естественном течении заболевания связан с разной прогнозируемой продолжительностью жизни. По результату генетического анализа тип СМА установить нельзя.
СМА не зря называют коварным заболеванием. Нередко его признаки появляются внезапно, на фоне нормального общего развития, после чего все приобретенные навыки — удержания головы, сидения, ползания, стояния — постепенно теряются.
Классических типов СМА пять. Отдельно выделяют СМА 0 и IV типов [2].
СМА 0
СМА 0 типа нередко объединяют с I типом СМА. Он также, как и I тип, имеет самое тяжелое течение. СМА 0 типа проявляется еще внутриутробно — ребенок начинает менее активно шевелиться. С первых дней жизни у новорожденного наблюдаются резко сниженная спонтанная двигательная активность и мышечная гиподинамия, отсутствие сухожильных рефлексов, возникают проблемы с дыханием и глотанием.
Продолжительность жизни детей с этим типом СМА составляет несколько недель.
СМА I
Самый тяжелый тип СМА. Первые признаки заболевания возникают в возрасте до шести месяцев. Как правило, родители первыми замечают тревожные симптомы: ребенок не держит голову, не переворачивается и не может сидеть без посторонней поддержки. Дети со СМА I типа очень слабые, не могут в полную силу кричать и кашлять, испытывают трудности с принятием пищи, глотанием, дыханием и отхождением мокроты, в результате чего у них высок риск осложненного течения респираторных заболеваний.
Ожидаемая продолжительность жизни таких больных составляет меньше двух лет. Более ⅔ детей со СМА не доживают до двух лет и погибают в результате развития дыхательной недостаточности из-за слабости дыхательной мускулатуры.
СМА II
Данный тип СМА протекает медленнее и впервые проявляется в возрасте от шести до 18 месяцев. Главный признак — ребенок с трудом встает на ноги, в большинстве случаев у него вовсе не получается удерживать вертикальное положение тела. Ходить такие дети не могут. Также наблюдается задержка моторного развития, дрожание рук, сколиоз вследствие слабости мышц и контрактуры суставов. Больным может потребоваться инвалидная коляска. Вкупе с другими приспособлениями — поддержками, упорами — это позволяет зафиксировать оптимальное положение тела пациента.
Ожидаемая продолжительность жизни больных с этим типом СМА — 20–40 лет.
СМА III
Для третьего типа СМА характерно стабильное развитие больных до определенного возраста. Они могут сидеть, стоять и ходить. Затем болезнь проявляет себя — из-за прогрессирующей слабости мышц нижних конечностей походка постепенно становится неустойчивой. В ряде случае пациенты теряют способность ходить.
Продолжительность жизни больных со СМА III типа, как правило, такая же, как у обычных людей.
СМА IV
Этот тип СМА считается самым легким. Он проявляется уже во взрослом возрасте — после 25 лет. У таких больных наблюдаются умеренные двигательные нарушения, мышечная слабость, тремор. В ряде случаев из-за прогрессирования заболевания теряется способность ходить.
Диагностика СМА
Крайне важно установить диагноз как можно раньше, чтобы начать лечение и реабилитацию [3], [4].
Для подтверждения диагноза обычно проводят молекулярно-генетический анализ. Он показывает, имеется ли у больного дефект в гене SMN1, а также число копий гена SMN2. Анализ может быть назначен любым врачом, заподозрившим СМА. Педиатр и невролог может заметить настораживающее отставание развития ребенка от возрастных норм, поэтому родителям важно вовремя проводить все плановые осмотры ребенка и самим наблюдать за его физическим развитием.
При необходимости могут быть назначены и другие исследования, в том числе дополнительный генетический анализ, электромиография, некоторые лабораторные исследования, которые в большей степени служат для исключения похожих заболеваний. После уточнения диагноза требуется осмотр несколькими узкими специалистами для оценки факторов риска развития дыхательной недостаточности, ортопедических проблем, трудностей кормления и откашливания.
Очень важно, чтобы с каждым больным ребенком работала мультидисциплинарная команда специалистов, знающих все аспекты и нюансы лечения и реабилитации больных СМА.
Лечение СМА
Сегодня для лечения СМА в мире применяются три препарата.
Крупнейшие мировые фармацевтические компании параллельно исследуют и разрабатывают лекарства. В том числе оценивается эффективность увеличения доз препаратов, тестируются различные способы введения и комбинации лекарств.
Два из трех разработанных препаратов подходят для лечения всех типов СМА и на всех этапах. Однако чем раньше начинается лечение, тем лучшего эффекта можно достичь. Данная группа лекарств влияет на работу гена SMN2, который, в свою очередь, кодирует белок SMN, отвечающий за выживание нейронов спинного мозга. Препараты позволяют стабилизировать течение заболевания, улучшить двигательные функции больного и приобрести новые моторные навыки.
Третий революционный препарат для лечения СМА у детей — продукт генной терапии. При помощи вирус-вектора препарат доставляет синтетическую функциональную копию гена SMN1 в нейроны спинного мозга. В результате лечения в моторных нейронах, лишенных гена SMN1, восстанавливается продуцирование белка SMN. Дозировка этого лекарства устанавливается индивидуально для каждого пациента в зависимости от веса. Безопасность и эффективность препарата установлены у детей в возрасте до двух лет или с весом до 21 кг. Лекарство применяется однократно — вводится пациенту путем внутривенной инфузии в течение одного часа. Из-за дороговизны разработка стоимость такого лечения достигает 150 млн руб.
На сегодняшний день любая медикаментозная терапия пациентам со СМА должна назначаться специалистами, имеющими достаточный опыт в ее применении.
Жизнь со СМА: как помочь больному
До появления препаратов для лечения СМА больным оказывалась только паллиативная помощь, призванная максимально облегчить симптомы [5].
Теперь речь идет о реабилитации, однако отработанных эффективных методик пока мало. На данный момент с уверенностью можно говорить только об эффективности физической терапии и гидрокинезотерапии.
Огромную роль в реабилитации больного со СМА играют его близкие. Вместе в врачами разных профилей они образуют единую команду, совместными усилиями которой ребенку могут быть обеспечены максимально эффективная системная реабилитация и уход.
Физическая терапия
Из-за общей мышечной слабости больные СМА не могут совершать движения в том же объеме, что здоровые люди. Из-за этого возникает риск развития контрактур суставов, которые со временем могут стать постоянными и ограничивать движения. Лечебная физкультура включает комплексы упражнений по восстановлению гибкости и общих функциональных возможностей. Упражнения подбираются индивидуально для каждого пациента в зависимости от особенностей его здоровья. Например, для полностью лежачих больных занятия ставят целью в том числе увеличение объема и амплитуды активных/пассивных движений в любом сегменте тела и конечностей. У сидячих пациентов — повышение мобильности.
В лечебной физкультуре также применяются различные вспомогательные устройства и приспособления. Например, вертикализатор позволяет улучшить прочность костей и может использоваться в домашних условиях.
Гидрокинезотерапия
Гидрокинезотерапия представляет собой комплекс водных лечебных упражнений, дополняемый подводным массажем и ортопедическими приспособлениями.
Упражнения проходят в специально оснащенном бассейне при оптимальной температуре воды. В целом вода — это дружественная среда для больных СМА, в том числе за счет снятия нагрузки на позвоночник, суставы и сердце. Занятия позволяют укрепить все группы мышц, способствуют восстановлению двигательных функций, повышают общий тонус пациентов и очень нравятся детям.
Где узнать о СМА больше
SMA Europe — европейская пациентская организация, созданная в 2006 году. Она объединяет пациентские и исследовательские организации всей Европы, посвященные СМА.
«Семьи СМА» — российская пациентская организация, часть SMA Europe, созданная в 2015 году. На сайте представлена актуальная информация о СМА для пациентов и их семей, в том числе последние новости о законодательных аспектах и фармацевтическом рынке. Работает горячая линия.
TogetherInSMA— международный сайт, созданный для информирования пациентов со СМА и их семей. Здесь на русском языке можно получить общую информацию о СМА, доступных методах лечения, найти практические руководства по уходу за больными и другие полезные сведения.
Вниманиесма.рф — информационный портал, созданный при поддержке второй по величине в мире фармацевтической компании. Ресурс полностью посвящен симптоматике СМА, в том числе первым тревожным симптомам заболевания.
Узнать о том, как поддержать людей с редкими (орфанными) заболеваниями можно на сайте «Редкое искусство помогать» и в аккаунте @rare_art.
Важно помнить, что ни информация данных ресурсов, ни эта статья не заменяют очную консультацию у медицинского специалиста по любым вопросам, связанным с диагностикой и лечением СМА.