Лактобактерии rhamnosus что это
Lactobacillus rhamnosus (лактобактерии рамнозус)

Lactobacillus rhamnosus являются, наряду с некоторыми другими видами лактобактерий, нормальной микрофлорой кишечника человека.
Lactobacillus rhamnosus в лекарствах, БАДах и продуктах-пробиотиках
Лактобактерии (лактобациллы) рамнозус в лиофилизированном виде применяются в качестве вещества, придающего свойства пробиотика в БАДах и молочных продуктах. Американская гастроэнтерологическая ассоциация отмечает, 
СанПиН 2.3.2.2340-08, утвержденный Постановлением Главного государственного санитарного врача РФ 18 февраля 2008 г. № 13 разрешает использование Lactobacillus rhamnosus в пищевой промышленности.
Штамм Lactobacillus rhamnosus ATCC 53103 (синонимы: Lactobacillus GG и LGG ® ) был выделен из кишечника здорового человека в 1983 и запатентован в 1985 году Шервудом Горбачом (англ. Sherwood Gorbach) и Барри Голдиным (англ. Barry Goldin). Символы «GG» в наименовании штамма взяты от первых букв их фамилий. В своём патенте, а также в позднейших публикациях, Горбач и Голдин отмечают, что данный штамм является устойчивым к воздействию кислоты желудочного сока и желчи и, поэтому, после перорального введения бактерии достигают толстой кишки живыми.
Имеются доказательства, что Lactobacillus rhamnosus GG является самым эффективным пробиотиком в долговременной профилактике развития атопического дерматита у детей самого младшего возраста (Foolad N. etal. JAMA Dermatol. 2013; 149(3): 350-5).
Применение пробиотика Lactobacillus rhamnosus GG снижает продолжительность диареи при гастроэнтеритах у детей. Наибольшая польза отмечалась у европейских пациентов которым LGG назначался в высокой дозе ≥10 10 КОЕ/сутки (Szajewska H. etal. Aliment Pharmacol Ther. 2013; 38(5)).
Штамм Lactobacillus rhamnosus GR-1 был выделен из дистальных отделов уретры здоровых женщин канадскими учеными A.W. Bruce и G. Reid в 1980 году. Этот штамм обладает высокими адгезивными свойствами в отношении вагинальных эпителиоцитов. Штамм Lactobacillus rhamnosus GR-1 обладает способностью продуцировать бактерициноподобные вещества и устойчив к спермицидам. Штамм сохраняют жизнеспособность после прохождения через желудочно-кишечный тракт и ввиду анатомической близости анального отверстия и преддверия влагалища способен успешно колонизировать урогенитальную зону вытесняя при этом патогенную микрофлору.

Штамм Lactobacillus rhamnosus LCR35 является основным пробиотическим компонентом в БАД Линекс Иммуно.
Штамм Lactobacillus rhamnosus LB21 входит в состав продукта Verum (фирма-производитель Norrmejerier).
Lactobacillus rhamnosus в систематике бактерий
Вид Lactobacillus rhamnosus относится к роду Лактобактерии (или Лактобациллы, лат. Lactobacillus), который входит в семейство Lactobacillaceae, порядок Lactobacillales, класс Bacilli, тип Firmicutes, Terrabacteria group, царство Бактерии.
Ранее Lactobacillus rhamnosus классифицировались как подвид вида Lactobacillus casei, но сейчас выделены в самостоятельный вид.
Lactobacillus rhamnosus (лактобактерии рамнозус)

Lactobacillus rhamnosus являются, наряду с некоторыми другими видами лактобактерий, нормальной микрофлорой кишечника человека.
Lactobacillus rhamnosus в лекарствах, БАДах и продуктах-пробиотиках
Лактобактерии (лактобациллы) рамнозус в лиофилизированном виде применяются в качестве вещества, придающего свойства пробиотика в БАДах и молочных продуктах. Американская гастроэнтерологическая ассоциация отмечает, 
СанПиН 2.3.2.2340-08, утвержденный Постановлением Главного государственного санитарного врача РФ 18 февраля 2008 г. № 13 разрешает использование Lactobacillus rhamnosus в пищевой промышленности.
Штамм Lactobacillus rhamnosus ATCC 53103 (синонимы: Lactobacillus GG и LGG ® ) был выделен из кишечника здорового человека в 1983 и запатентован в 1985 году Шервудом Горбачом (англ. Sherwood Gorbach) и Барри Голдиным (англ. Barry Goldin). Символы «GG» в наименовании штамма взяты от первых букв их фамилий. В своём патенте, а также в позднейших публикациях, Горбач и Голдин отмечают, что данный штамм является устойчивым к воздействию кислоты желудочного сока и желчи и, поэтому, после перорального введения бактерии достигают толстой кишки живыми.
Имеются доказательства, что Lactobacillus rhamnosus GG является самым эффективным пробиотиком в долговременной профилактике развития атопического дерматита у детей самого младшего возраста (Foolad N. etal. JAMA Dermatol. 2013; 149(3): 350-5).
Применение пробиотика Lactobacillus rhamnosus GG снижает продолжительность диареи при гастроэнтеритах у детей. Наибольшая польза отмечалась у европейских пациентов которым LGG назначался в высокой дозе ≥10 10 КОЕ/сутки (Szajewska H. etal. Aliment Pharmacol Ther. 2013; 38(5)).
Штамм Lactobacillus rhamnosus GR-1 был выделен из дистальных отделов уретры здоровых женщин канадскими учеными A.W. Bruce и G. Reid в 1980 году. Этот штамм обладает высокими адгезивными свойствами в отношении вагинальных эпителиоцитов. Штамм Lactobacillus rhamnosus GR-1 обладает способностью продуцировать бактерициноподобные вещества и устойчив к спермицидам. Штамм сохраняют жизнеспособность после прохождения через желудочно-кишечный тракт и ввиду анатомической близости анального отверстия и преддверия влагалища способен успешно колонизировать урогенитальную зону вытесняя при этом патогенную микрофлору.

Штамм Lactobacillus rhamnosus LCR35 является основным пробиотическим компонентом в БАД Линекс Иммуно.
Штамм Lactobacillus rhamnosus LB21 входит в состав продукта Verum (фирма-производитель Norrmejerier).
Lactobacillus rhamnosus в систематике бактерий
Вид Lactobacillus rhamnosus относится к роду Лактобактерии (или Лактобациллы, лат. Lactobacillus), который входит в семейство Lactobacillaceae, порядок Lactobacillales, класс Bacilli, тип Firmicutes, Terrabacteria group, царство Бактерии.
Ранее Lactobacillus rhamnosus классифицировались как подвид вида Lactobacillus casei, но сейчас выделены в самостоятельный вид.
Лактобактерии рамнозус-СМ Порошок, саше, 10 шт, 1000 мг, для приема внутрь
Lactobacillus rhamnosus – это естественные обитатели кишечно.
Инструкция
Инструкция
Состав
Мальтодекстрин (носитель), лиофилизированная культура лактобактерий рамнозус (Lactobacillus rhamnosus) Lr-G14.
Содержание лактобактерий (Lactobacillus rhamnosus) в пакете-саше 1 грамм, не менее КОЕ 2х109
Описание
Биологически активная добавка, содержащая живые лактобактерии рамнозус (Lactobacillus rhamnosus) для восполнения бактериальной флоры пищеварительного тракта и сохранения ее нормального состава для детей с рождения и взрослых.
Рекомендуется в качестве добавки к пище как источник пробиотических микроорганизмов способствующих: улучшению работы кишечника, восстановлению баланса микрофлоры кишечника, укреплению иммунитета и ускорению процессов адаптации организма.
Фармакологические свойства
Lactobacillus rhamnosus – это естественные обитатели кишечного тракта, часть нормальной кишечной флоры. Они необходимы для процессов пищеварения и формирования «защитного барьера» организма для поддержки здоровья человека.
Нарушения баланса кишечной микрофлоры у малышей могут проявляться нарушениями стула, аппетита, повышенным газообразованием (коликами).
Причинами нарушения микробного равновесия в кишечнике у детей (дисбактериоз) могут стать отсутствие или прекращение грудного вскармливания, изменения в рационе (введение прикорма), необходимость приема средств, подавляющих нормальную микрофлору. В связи с чем может возникнуть необходимость приема пробиотического комплекса, содержащего полезные пробиотические бактерии.
Пробиотические микроорганизмы Lactobacillus rhamnosus являются представителями нормальной микрофлоры кишечника человека, антагонистами патогенных и условно-патогенных микроорганизмов, оказывают корригирующее действие на микрофлору кишечника, способствуют повышению общей резистентности организма человека.
Способ применения и дозы
Содержимое пакета-саше перед применением следует растворить в достаточном количестве жидкости. Принимать сразу после растворения. Не допускается растворение в горячей жидкости, выше 37 С.
Детям, находящимся на грудном вскармливании, содержимое пакета-саше (1г) перед применением следует растворить в сцеженном грудном молоке, смеси для кормления или другим видом детского питания.
Детям c рождения до 3-х лет, принимать по 1 пакету-саше 1 раз в день.
Детям с 3-х лет и взрослым принимать по 1 пакету-саше 2 раза в день во время еды. Продолжительность приема в среднем – 10-14 дней.
При необходимости продолжительность приема может составлять 30 дней.
Перед применением рекомендуется проконсультироваться с врачом, перед применением БАД детьми необходимо проконсультироваться с врачом-педиатром.
Не содержит белков коровьего молока, лактозу, глютен и сахарозу, поэтому может применяться у лиц, страдающих непереносимостью этих веществ.
Особые указания
Биологически активная добавка (БАД) к пище. Не является лекарством.
Кишечная микробиота и иммунитет: иммуномодулирующие эффекты Lactobacillus rhamnosus GG
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Кишечная микробиота представляет собой совокупность огромного количества микроорганизмов, которые образуют своеобразный симбиоз с организмом человека, где каждый извлекает выгоды для своего существования и оказывает влияние на партнера. Можно уверенно говорить, что нет ни одной функции организма, на которую не влияла бы тем или иным способом кишечная микробиота.
Кишечник является самым большим иммунным органом человеческого организма, при этом эффективность функционирования местного иммунитета зависит от заселения кишечника индигенной микрофлорой. Особое место в процессе формирования и функционирования иммунной системы отводится лактобактериям.
В данном обзоре мы ставили перед собой цель донести наиболее полную информацию о составе и функциях микробиоты кишечника, ее роли в формировании иммунитета и терапевтических возможностях штамма Lactobacillus rhamnosus GG. Установленные механизмы молекулярного действия, детальная структурная и генетическая характеристика, данные рандомизированных исследований и метаанализов, а также огромный опыт эффективного практического использования LGG делают этот штамм средством выбора для профилактики и снижения тяжести целого ряда состояний, обусловленных дисфункцией иммунной системы.
Ключевые слова: микрофлора кишечника, иммунитет, пробиотик, Lactobacillus rhamnosus GG, LGG.
Для цитирования: Оганезова И.А. Кишечная микробиота и иммунитет: иммуномодулирующие эффекты Lactobacillus rhamnosus GG. РМЖ. 2018;9:39-44.
Intestinal microbiota and immunity: immunomodulatory effects of Lactobacillus rhamnosus GG
I.A. Oganezova
North-Western State Medical University named after I. I. Mechnikov, St. Petersburg
Intestinal microbiota is a complex formed by a large number of microorganisms, which make a kind of symbiosis with the human body, where everyone gets benefits for his existence and influences the partner. It can be confidently said, that there are no such functions of the body, which are not effected by the intestinal microbiota in one way or another.
The intestine is the largest immune organ of the human body, while the effectiveness of local immunity depends on the colonization of the intestine by an indigenous microflora. Lactobacilli take a special place in the process of formation and functioning of the immune system.
The aim of this review was to provide the most complete information about the composition and functions of the intestinal microbiota, its role in the formation of immunity and the therapeutic possibilities of Lactobacillus rhamnosus GG. The established mechanisms of molecular action, the detailed structural and genetic characteristics, the data of randomized studies and meta-analyzes, and the great experience of effective practical use of LGG make this strain the means of choice for the prevention and relieving a number of conditions caused by immune system dysfunction.
Key words: intestinal microflora, immunity, probiotic, Lactobacillus rhamnosus GG, LGG.
For citation: Oganezova I.A. Intestinal microbiota and immunity: immunomodulatory effects of Lactobacillus rhamnosus GG //
RMJ. 2018. № 9. P. 39–44.
В обзоре рассмотрена информация о составе и функциях микробиоты кишечника, ее роли в формировании иммунитета и терапевтических возможностях штамма Lactobacillus rhamnosus GG
Состав и функции кишечной микробиоты
Желудочно-кишечный тракт (ЖКТ) представляет собой самый обширный ареал обитания микрофлоры в организме. Применение современных молекулярно-генетических технологий позволило получить достаточно полные представления о числе, генетической неоднородности и сложности бактериальных компонентов микробиоты кишечника. Установлено, что микробиота кишечника человека является эволюционно сложившейся совокупностью микроорганизмов, существующей как сбалансированная микроэкологическая система, в которой симбионтная микрофлора находится в динамическом равновесии, формирует микробные ассоциации, занимающие в ней определенную экологическую нишу, и относится к важнейшим факторам, влияющим на здоровье человека [2].
Значительная изменчивость состава микробиоты между людьми обнаруживается при рассмотрении таксономического уровня видов и штаммов внутри видов. Состав микробиоты каждого человека уникален. В этой экосистеме существуют все известные механизмы и типы взаимоотношений как между бактериями, так и между бактериями и клетками хозяина [3]. Данные некоторых молекулярно-филогенетических исследований свидетельствуют о наличии в человеческом кишечнике от 15 тыс. до 36 тыс. видов бактерий [4].
С позиций современной биологии человек вместе с живущими в его кишечнике генетически совместимыми микро-
организмами представляет собой единый «суперорганизм», обмен веществ которого обеспечивается четко организованной работой ферментов, кодируемых не только
геномом собственно человека, но и геномами всех симбиотических микроорганизмов. Следует подчеркнуть, что совокупность генов всех микроорганизмов человека — метагеном в 100–150 раз многочисленнее генома самого человека [5].
Нормальная микрофлора кишечника подразделяется на индигенную (облигатную) и факультативную (транзиторную). К индигенной относятся микроорганизмы, постоянно входящие в состав нормальной микрофлоры и играющие важную роль в метаболизме организма-хозяина и защите его от возбудителей инфекций. В здоровом кишечнике взрослого человека доминируют два бактериальных типа, на которые приходится более 90% бактериальных клеток: Firmicutes и Bacteroidetes. Микроорганизмы, относящиеся к нормальной микрофлоре кишечника, колонизируют как просвет ЖКТ, так и поверхность слизистой оболочки кишки (СОК), формируя при этом пристеночную (мукозную) и полостную микрофлору. Нормальная микрофлора кишечника на 92–95% состоит из строго анаэробных видов [6].
Основные представители микрофлоры, населяющие различные биотопы ЖКТ, представлены в таблице 1 [7].
Совокупность микроорганизмов и макроорганизм составляют своеобразный симбиоз, где каждый извлекает выгоды для своего существования и оказывает влияние на партнера. Функции кишечной микрофлоры по отношению к макроорганизму реализуются как локально, так и на системном уровне, при этом различные виды бактерий вносят свой вклад в это влияние. По своей роли в поддержании гомеостаза микробиота кишечника не уступает любому жизненно важному органу, поэтому любые нарушения ее состава могут приводить к значительным отклонениям в состоянии здоровья человека [8].
Основные функции кишечной микрофлоры и механизмы их реализации:
Защитная: обеспечение колонизационной резистентности: избирательное подавление факультативной флоры; препятствие адгезии, размножению и инвазии экзогенно поступающих микроорганизмов; продукция лизоцимов, бактериоцинов, Н2О2, антимикробных факторов.
Пищеварительная: продукция ферментов, обеспечивающих гидролиз и всасывание нутриентов.
Метаболическая: регуляция обмена желчных кислот, холестерина, водно-электролитного баланса, состава кишечных газов, поддержание дифференцированных значений рН, детоксикация экзогенных и эндогенных метаболитов.
Синтетическая: синтез витаминов В1, В2, В3, В5, В6, В9, В12, С, К, аминокислот, гормонов, биологически активных веществ, летучих жирных кислот.
Иммуномодулирующая: участие в созревании и функционировании иммунокомпетентных структур кишечника, синтез иммуноглобулинов, цитокинов.
Иммунная система кишечника
Роль кишечной микрофлоры в иммунных реакциях
Влияние пробиотических препаратов на иммунный статус
Иммуномодулирующие эффекты LGG
Терапевтические возможности LGG
Заключение
Только для зарегистрированных пользователей
Пробиотик Lactobacillus rhamnosus GG (LGG®): что мы знаем об эффективности и безопасности?
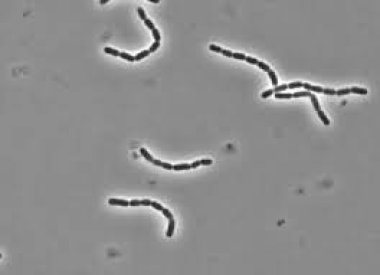
Приводятся современные данные о роли пробиотического штамма Lactobacillus rhamnosus GG (LGG®) в педиатрической практике. Штамм LGG® широко используется как в составе детских молочных смесей, так и в составе ряда лекарственных препаратов. LGG® обладают выс
Current data on the role of probiotic strain Lactobacillus rhamnosus LGG® in pediatric practice are presented. LGG® strain is widely used both as a component of infant formulas and of medical preparations. Lactobacillus LGG® has a high degree of resistance to gastric acid and to bile salts, due to pili, the adhesion to intestinal epithelial cells is realized. LGG® is characterized by an active persistance of colonization of human colonic mucosa. Besides the inhibition of pathogens they participate in intestinal microbiota modulation, support reduction of risk of allergic diseases and provide formation of immunological tolerance.
Лактобациллы L. rhamnosus GG (далее обозначаемые как LGG®) являются наиболее подробно изученными в мировой науке пробиотиками. После углубленного изучения природных лактобацилл штамм был выделен Gorbach и Goldin в 1985 г. и затем подробно исследован [1, 2]. С тех пор штамм был изучен как in vitro, так и in vivo, и сейчас история его изучения насчитывает более 1100 научных публикаций, из которых более 300 — это клинические исследования. Штамм LGG® обладает доказанной клинической эффективностью при целом ряде заболеваний и оказывает положительное действие в отношении иммунной функции и при гастроэнтерологических заболеваниях [3, 4].
Клинические исследования показывают, что LGG® выживают в желудочно-кишечном тракте (ЖКТ) и способны восстановить естественный баланс полезной кишечной микробиоты. LGG® обладают способностью ингибировать патогены in vitro и успешно укрепляют барьерную функцию кишечной слизистой. Более того, LGG® имеют сильное взаимодействие с иммунной системой и оказывают стимулирующее действие на иммунные клетки.
Пробиотики с точки зрения характеристики штаммов
Эффекты пробиотиков, согласно ФАО/ВОЗ (2001), являются штаммоспецифичными и не могут носить «общего характера». Характеристика специфичных свойств каждого штамма основана строго на результатах клинических исследований. Различные штаммы оказывают только присущий им пробиотический эффект. Поэтому необходимо очень четко отслеживать характеристики, свойства и показатели эффективности каждого конкретного штамма (например, именно штамма LGG®, а не просто Lactobacillus rhamnosus).
LGG® выделен из фекального образца здорового взрослого мужчины в 1985 г. Штамм специфически селектирован как обладающий оптимальными характеристиками по своему влиянию на здоровье человека [5].
Эксперты отмечают, что штамм LGG® технологически очень удобен, обладает высокой ферментативной активностью, хорошо выдерживает такой технологический прием, как распылительная сушка, часто используемая в молочной промышленности, в частности, при производстве детских молочных смесей. Кроме того, LGG® не оказывает отрицательного влияния на вкусовые качества продуктов, обладает высокой степенью выживаемости в ЖКТ. Используется в пищевой промышленности с 1990 г. [5], в том числе в составе БАДов, детских молочных смесей и ферментированных молочных продуктов (например, йогуртов) во всем мире.
Критерии идеального пробиотического штамма:
Показатели устойчивости и механизмы действия
LGG® обладает устойчивостью к кислоте и желчи и имеет прекрасные адгезивные свойства в отношении кишечной слизистой.
Два важных фактора защиты организма человека — это кислотная среда желудка и воздействие желчи, которые препятствуют попаданию в организм патогенов. Однако эти же факторы способны погубить полезные пробиотические микроорганизмы. Для своего успешного действия в организме пробиотический штамм должен выживать в условиях воздействия кислоты и желчи. Исследования in vitro показали, что LGG® успешно переносят двухчасовую инкубацию в кислой среде при рН 2,5 (выживаемость 73%) и двухчасовую инкубацию при воздействии желчи (0,3% или 1% — выживаемость 81%) [6]. Такие концентрации соляной кислоты и желчи соответствуют условиям в живом организме и являются физиологичными. Это доказывает наличие устойчивости LGG® к кислой среде желудка и воздействию желчных кислот в двенадцатиперстной кишке.
Способность пробиотического штамма фиксироваться к поверхности интестинальной мукозы важна для транзиторной колонизации. Доказано, что LGG® обладают высокими адгезивными свойствами в составе пристеночной слизи и при непосредственном контакте с эпителиальными клетками. В отличие от других штаммов лактобацилл, LGG® имеют жгутикоподобные волоски на поверхности клетки, называемые «пили», которые важны для фиксации к поверхности слизистой оболочки.
Ингибирование патогенов
Способность ингибировать патогены — это важный механизм, с помощью которого пробиотики обладают способностью уменьшать частоту, тяжесть и продолжительность кишечных инфекций. Существует целый ряд механизмов, благодаря которым пробиотики способны ингибировать патогенные микроорганизмы. К ним относятся:
Модуляция кишечной микробиоты
В толстой кишке человека обитает большое разнообразие микроорганизмов, среди которых лактобациллы занимают важное место в составе сложной экосистемы. Кишечная микробиота выполняет важную роль в поддержании здоровья. Микробиота является метаболически активной и служит защитным механизмом для всего организма. Отклонения в ее составе приводят к разным заболеваниям как организма в целом, так и разных отделов ЖКТ [7]. Существует симбиотическое взаимодействие между кишечной микробиотой и макроорганизмом, поскольку макроорганизм обеспечивает микробное сообщество необходимыми нутриентами, а микробиота выполняет важную роль в созревании ЖКТ, переработке ряда нутриентов и защите от патогенных микробов. Более того, кишечная микробиота является важнейшим иммунологическим органом нашего организма и выполняет ключевую роль в формировании и поддержании иммунной системы. В европейской монографии ILSI «Пробиотики, пребиотики и кишечная микробиота» отмечено, что высокое преобладание бифидобактерий и лактобацилл представляет собой «наиболее здоровую микробную композицию» [8]. В частности, такой постулат основан на том факте, что у детей грудного возраста преобладают бифидобактерии и лактобациллы, которые ферментируют углеводы и вырабатывают органические кислоты, которые лишены токсического потенциала. Активность LGG® сопровождается повышением доли полезных бактерий, что одновременно подавляет рост условно-патогенных бактерий.
Пробиотикам присущи три основных механизма действия. Во-первых, определенные пробиотики обладают способностью подавлять или ликвидировать патогены. Второй механизм заключен в способности определенных пробиотических штаммов укреплять эпителиальную барьерную функцию, модулируя сигнальные пути или укрепляя целостность межклеточных плотных связей. В-третьих, большинство пробиотических штаммов обладает иммуномодулирующими свойствами, оказывая штаммоспецифическое местное и системное действие.
Принимая во внимание комплексный характер каждого из трех механизмов действия, необходимо отметить, что разные штаммы вызывают разные типы ответа в макроорганизме. Поэтому результаты изучения одного штамма Lactobacillus нельзя переносить на другие штаммы. Исследование молекулярных механизмов действия пробиотиков должно учитывать штаммоспецифические свойства. Различные штаммы Lactobacillus имеют различные специфические свойства, экскретируют различные поверхностные молекулы и секретируют белки и метаболиты, напрямую взаимодействующие с организмом хозяина.
Желудочно-кишечный дискомфорт
Периодическое возникновение боли в животе, спазмов, метеоризма, кишечных колик при отсутствии органических причин или обменных нарушений принято называть «кишечным дискомфортом». Обычно эти явления связаны с пищей или с приемом лекарственных препаратов и весьма вариабельны по частоте и степени выраженности. Снижение степени желудочно-кишечного дискомфорта служит показателем улучшения функции ЖКТ и считается «положительным физиологическим эффектом».
В одном исследовании прицельно изучали влияние LGG® на функциональные нарушения ЖКТ и болевой синдром у детей [9]. В двойное плацебо-контролируемое исследование (ПКИ) были включены 104 ребенка (6–16 лет) с функциональной диспепсией (ФД). Синдром раздраженного кишечника или функциональные боли в животе (ФБЖ) оценивались согласно Римским критериям II пересмотра [9]. LGG® (3 × 10 9 КОЕ) или плацебо назначали 2 раза в день в течение 4 недель. Критерием успешности лечения считали исчезновение болевых приступов по окончании курса терапии. В результате такой эффект был достигнут в 25% случаев в группе LGG® и лишь в 9,6% в группе плацебо (р = 0,02).
Избыточный детский плач (excessive crying) у практически здоровых детей совпадает с периодом сразу нескольких процессов созревания, которые происходят в ЖКТ в ответ на массивное нашествие антигенов вследствие микробной колонизации и большого объема (до 1/5 веса тела) потребления пищи. Принципиальные попытки уменьшить плач ребенка основаны на изменении режима питания и попытках модуляции кишечной микробиоты [10].
Результаты исследования с участием 89 детей в возрасте 7–12 недель были основаны на попытке связать воедино состав кишечной микробиоты и беспокойство и продолжительность крика. В двойном слепом ПКИ дети получали LGG® (10 9 КОЕ/день в возрасте 1–30 дней и 2 × 10 9 КОЕ/день в возрасте 31–60 дней), а затем находились на катамнестическом наблюдении весь первый год жизни [11]. Дети, которых относили в группу «избыточного крика», значительно реже встречались в LGG®-группе, чем в группе плацебо. По данным микробиологических исследований, в контрольной группе (без LGG®) значительно чаще в стуле детей определяли Clostridium hydrolyticum, чем в группе, получавшей LGG® (р = 0,05).
Таким образом, назначение LGG® в дозах от 1 × 10 9 до 6 × 10 9 КОЕ/день оказывает положительный эффект при таких нарушениях, как абдоминальная боль и кишечный дискомфорт у детей.
LGG® и формирование иммунитета
Существуют убедительные доказательства того, что некоторые пробиотики положительно влияют на состояние иммунной защиты организма [12]. Одним из таких примеров является их протективное действие в отношении воздействия патогенов, вызывающих заболевания респираторного тракта. Влияние LGG® на патогены дыхательных путей изучалось у детей.
В исследовании с участием 513 здоровых детей, посещающих детский сад, им назначали молочный напиток, содержащий 1–2 × 10 9 КОЕ/день или обычное молоко в течение 5 дней в неделю на протяжении 7 месяцев. Оказалось, что пропуски посещения детского сада по болезни были значительно реже в группе, получавшей LGG® (4,9 против 5,8 дня на ребенка, р = 0,03) [13]. К тому же у детей, получавших LGG®, суммарно была ниже заболеваемость ОРВИ по сравнению с контрольной группой (р = 0.03). Реже встречались и респираторные инфекции, сопровождающиеся инфекциями (отит), и реже возникали показания для назначения антибиотиков [13].
В двойном слепом ПКИ с участием 281 ребенка в возрасте старше 1 года в условиях детского учреждения дети получали 100 мл ферментированного молока с LGG® (1 × 10 9 КОЕ/сутки) или плацебо в течение 3 мес. В группе LGG® значительно реже наблюдались ОРВИ, имеющие продолжительность более 3 дней (р 10 КОЕ), либо плацебо в капсулах ежедневно в течение 2–4 недель до ожидаемого срока родов [17]. После рождения ребенка или кормящая мать, или младенец получали LGG® в течение 6 месяцев. Дети прошли клиническое обследование в возрасте 2 лет. Частота АД в группе, получавшей LGG®, составила 23%, в группе плацебо — 46% (р = 0,006). Далее этот результат был подтвержден авторами, когда детям исполнилось 4 года и 7 лет [18, 19]. При обследовании в 7-летнем возрасте с помощью шкалы регрессии Cox было показано, что риск АД был значительно снижен в группе LGG® по сравнению с контрольной группой (р = 0,027) [19].
Несколько исследований посвящено изучению пробиотиков в плане индукции благоприятного иммунного ответа на пищевые аллергены у детей с атопией.
Изучая формирование толерантности к белкам коровьего молока (БКМ), Berni Canani и соавт. [20] выполнили ПКИ, в котором было показано, что добавление LGG® в состав глубокого гидролизата казеина ускоряет выработку толерантности к БКМ у детей с аллергией к БКМ по сравнению с детьми, которые получали смесь гидролизата без пробиотика.
Результаты проспективного долговременного катамнестического исследования у детей, которые получали или только LGG®, или LGG® в сочетании с другими штаммами, перинатально показали, что дети, получавшие только LGG® или этот штамм в сочетании с другими штаммами, имели более низкий риск аллергических заболеваний (аллергический ринит, экзема, пищевая аллергия или астма) при продолжительном катамнестическом наблюдении [20].
Объединив все данные этих исследований, можно сделать вывод, что LGG® оказывают положительное физиологическое влияние на ответ против аллергенов (например, при АД), что способствует уменьшению риска развития аллергических заболеваний — пищевой аллергии и астмы.
Безопасность
В документе ФАО/ВОЗ «Здоровье и пищевые свойства пробиотиков в продуктах питания, включая сухое молоко, с живыми лактобактериями» безопасность пробиотиков определена следующим образом: «Информация, накопленная до настоящего времени, показывает, что лактобациллы имеют длительную историю использования в качестве пробиотиков без установленного риска для человека, и это является лучшим доказательством их безопасности. Кроме того, не обнаружено патогенных или вирулентных свойств у лактобацилл, бифидобактерий или лактококков».
Штамму LGG® присвоен статус GRAS от Управления по контролю за качеством пищевых продуктов и лекарственных средств (Food and Drug Administration, FDA) — Generally regarded as safe и аналогичный статус безопасности QPS от Европейского агентства по безопасности пищевой продукции (European Food Safety Authority, EFSA).
Cтандарт Codex Alimentarius для ферментированных видов молока разрешает использовать безопасные микроорганизмы в составе ферментированных молочных продуктов — детских кисломолочных смесей (ФAO/ВОЗ 2003, Codex Stan 243–2003).
LGG® считаются самыми безопасными благодаря длительной истории безопасного применения в клинической практике рода Lactobacillus, подвида L. rhamnosus и в особенности конкретного штамма LGG®.
Длительность назначения варьирует от одной недели до одного года. Формы применения разнообразны — от сухих детских молочных смесей до молочных продуктов, а также в виде фармпрепаратов (БАДов) в форме капсул, таблеток и саше или стиков. В большинстве опубликованных работ отсутствуют указания на какие-либо побочные эффекты, связанные с использованием LGG®.
В двух недавних исследованиях обратили внимание на долговременное влияние LGG® у детей [21, 22]. Например, Scalabrin и соавт. [21] оценили данные о безопасности долговременного применения LGG® в первые пять лет жизни, когда дети получали этот пробиотик на первом году жизни в составе детских молочных смесей. В ходе исследования были обследованы 183 ребенка, которые получали смесь с LGG® в течение одного года. Оценивали вес и рост, нервно-психическое развитие, а также наличие аллергических и инфекционных заболеваний за первые 5 лет жизни. Среди этих детей, которым исполнилось 5 лет, отмечены нормальные показатели роста и развития, отсутствие инфекций или аллергических заболеваний, которые могли быть связаны с длительным применением LGG®.
В 2013–2017 гг. Lindelin и соавт. [22] провели проспективное исследование, охватывающее детей, которые получали LGG® как таковой или в сочетании с другими штаммами пробиотиков в период с 1997 по 2012 гг. Авторы не обнаружили различий в показателях роста, развития и неинфекционной заболеваемости между детьми, которые получали пробиотики или плацебо пренатально.
В заключение следует отметить, что существует большое количество продуктов, содержащих LGG®, и миллионы людей используют эти продукты на протяжении более 30 лет. В очень редких случаях встречаются сообщения о побочных эффектах, что свидетельствует о высокой степени безопасности штамма LGG®.
Исключительно высокая технологическая стабильность штамма LGG® позволяет успешно использовать его в производстве сухих детских смесей.
В настоящее время на рынке РФ зарегистрированы три продукта серии Nutrilak Premium ProComfort (Nutrilak Premium Гипоаллергенный, Nutrilak Premium Кисломолочный, Nutrilak Premium Caesarea Бифи), обогащенные LGG®.
LGG® является товарным знаком компании Christian Hansen, Дания.
Литература
* ФГБОУ ДПО РМАНПО МЗ РФ, Москва
** ФГАУ НМИЦ ЗД МЗ РФ, Москва
*** АО «ИНФАПРИМ», Москва
Пробиотик Lactobacillus rhamnosus GG (LGG®): что мы знаем об эффективности и безопасности?/ С. Г. Грибакин, А. Г. Тимофеева, О. А. Боковская
Для цитирования: Лечащий врач № 4/2019; Номера страниц в выпуске: 92-95
Теги: молочная смесь, иммунитет, вскармливание, аллергия.

