Лактожиналь или бифидумбактерин свечи что лучше
Бактериальный вагиноз какая схема лечения?
Здравствуйте, девушка 24 года есть диагноз «бактериальный вагиноз», сдала анализ фемофлор-16, хронические заболевания отсутствуют. подскажите пожалуйста схему лечения по результатам данного анализа. Спасибо
Хронические болезни: Хронические заболевания отсутствуют
На сервисе СпросиВрача доступна консультация гинеколога по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!
Здравствуйте!
1й этап ЭЛЬЖИНА Интравагинально, по 1 вагинальной табл. ежедневно, перед сном 9 дней. Вагинальную таблетку следует вводить глубоко во влагалище в положении лежа на спине, после гигиенической обработки наружных половых органов. Перед введением во влагалище таблетку необходимо подержать в холодной кипяченой воде в течение 20–30 с. После введения таблетки следует лежать в течение 10–15 мин.
Опыт комбинированной терапии бактериального вагиноза
Клинические симптомы бактериального вагиноза состоят в появлении серовато-белых выделений из влагалища с неприятным «рыбным» запахом. Примерно у половины женщин нет клинически выраженных симптомов, они ощущают лишь повышенную влажность в области половых органов. При длительном течении бактериального вагиноза возможно изменение характера выделений, они становятся более густыми, липкими, меняется их цвет, переходя из серовато-белого в желто-зеленый. В ряде случаев можно наблюдать осложнения после гинекологических процедур, после медицинского аборта, вызванные бактериями, главным образом анаэробами, составляющими при бактериальном вагинозе основную часть вагинальной микрофлоры. При беременности возможно восходящее инфицирование околоплодных вод, преждевременное их излитие и развитие хориоамнионита, колонизация плода бактериями и возникновение заболевания плода и новорожденного ребенка. [9,10]
Лечение бактериального вагиноза направлено на устранение анаэробных бактерий и предупреждение восходящего инфицирования внутренних половых органов, а при беременности – восходящего инфицирования околоплодных вод с последствиями такого инфицирования для матери и ребенка. Традиционно для лечения бактериального вагиноза используют лекарственные препараты, подавляющие анаэробные микроорганизмы. В лечении бактериального вагиноза обычно используют метронидазол или клиндамицин. Однако, часто (в 30-40% случаев) такое лечение оказывается неэффективным, не всегда происходит элиминация анаэробных бактерий, последующее восстановление нормальной лактобациллярной микрофлоры влагалища и нормализация клинической картины заболевания. Предложен двухэтапный способ лечения бактериального вагиноза. На первом этапе с помощью нитраимидазолов устраняют анаэробную микрофлору, на втором – восстанавливают нормальную лактобациллярную микрофлору с помощью лактобациллярных препаратов. Однако виды лактобацилл, входящие в состав таких препаратов, не всегда приживаются во влагалище.[5]
Поиск средств, способных создавать и поддерживать условия для жизнедеятельности лактобацилл, оправдан в связи с распространенностью заболевания. В этом плане особого внимания заслуживает препарат «Эпиген интим», содержащий в своем составе активированную глицирризиновую кислоту и ряд дополнительных органических кислот (малеиновую, фумаровую, аскорбиновую, фолиевую), применяется местно в виде спрея и рекомендуется как иммуностимулирующее, противовоспалительное и противовирусное средство. Препарат не оказывает побочного действия, хорошо переносится и может быть применен для комплексной терапии бактериального вагиноза. Положительный опыт применения препарата «Эпиген интим» побудил нас использовать этот препарат в комплексной терапии бактериального вагиноза.
Целью нашего исследования было оценить лечебную эффективность и безопасность препарата «Эпиген интим» спрей 0,1% для местного и наружного применения в комплексной терапии бактериального вагиноза.
Клинические материалы и методы исследования
Исследование проводилось на базе Научно-исследовательского института акушерства и гинекологии им. Д.О. Отта СЗО РАМН и женской консультации №34 Санкт-Петербурга. Исследование было слепым, плацебо-контролируемым, рандомизированным.
Обследовано 90 небеременных женщин в возрасте от 18 до 45 лет, средний возраст – 28,3 года с установленным диагнозом бактериального вагиноза согласно критериям Амселя.
Все пациентки были разделены на три группы. Первая группа, состоящая из 30 человек, получала стандартную терапию в виде препарата «Клиндамицин» 2% вагинальный крем на ночь 3-7 дней в сочетании с использованием препарата «Эпиген интим спрей» 0,1% 2 раза в день 14 дней. Вторая группа (группа сравнения) также состояла из 30 человек и получала стандартную терапию в виде препарата «Клиндамицин» 2% вагинальный крем на ночь 3-7 дней в сочетании с плацебо 2 раза в день 14 дней. Третья (контрольная) группа, состоящая из 30 человек, получала только стандартную терапию в виде препарата «Клиндамицин» 2% вагинальный крем на ночь 3-7 дней. Рандомизация проводилась с помощью таблицы случайных чисел.
Наблюдение за пациентками проводилось во время 4 визитов: до начала терапии, на 14 день от начала терапии, на 30 и на 90 день от начала лечения. Эффективность терапии оценивалась по наличию или отсутствию жалоб со стороны пациенток, по оценке объективных клинических симптомов заболевания, по оценке лабораторных показателей, таких как количество лейкоцитов, соотношение лейкоцитов и эпителия, наличие ключевых клеток, качественный и количественный состав влагалищной микрофлоры при микроскопическом и бактериологическом исследованиях, по наличию лактобацилл в вагинальном отделяемом. Кроме того, проводилась оценка аминового теста и уровня рН. Безопасность и переносимость препарата оценивалась на основании регистрации побочных эффектов, связанных с применением препарата «Эпиген интим».
Результаты
При микробиологическом исследовании отделяемого влагалища получены следующие результаты. При микроскопии вагинальных выделений выявлены единичные лейкоциты (1-3-5 в поле зрения микроскопа, отношение лейкоцитов к эпителию менее чем 1:1), наличие «ключевых клеток», отсутствие лактобацилл. Назначено лечение по схемам, приведенным выше.
При клиническом осмотре женщин врачом на 14 день от начала лечения патологические выделения отмечены у 25% женщин I группы, у 74% женщин II группы и у 57,7% женщин III группы (рис. 2).
На 30 день и на 90 день от начала терапии отмечалась одинаковая тенденция к исчезновению жалоб. Что касается патологических выделений из половых путей, отмеченных врачом, то следует подчеркнуть, что в I группе они были у 30,4% и 21,7% женщин на 30 и 90 день, соответственно. Во II группе патологические выделения были отмечены у 45% и 55,5% женщин, соответственно, в III группе – у 43,8% и 57,1% женщин.
На рис 3 представлено количество пациенток, влагалищные выделения у которых имеют значение рН более, чем 4,5. В первой группе было 73,3% таких женщин, во второй группе – 26,6% и в третьей – 33,3%. На 14, 30 и 90 дни от начала лечения происходило снижение количества женщин с высоким (более 4,5) водородным показателем.
Один из основных признаков бактериального вагиноза – появление ключевых клеток, которые видны при микроскопическом исследовании вагинального отделяемого в виде клеток плоского эпителия с массой бактерий, адгезированных на поверхности. До лечения у всех пациенток были выявлены ключевые клетки. В I группе женщин на 14, 30 и 90 день терапии ключевые клетки не были выявлены ни в одном случае. Динамика наличия ключевых клеток на 14, 30 и 90 день терапии во II группе была следующей: 7,4%, 8,7%, 4,35%, соответственно. В III группе ключевые клетки были выявлены у 15,4% женщин на 14 день и у 4,35% на 30 день (рис. 4).
Микробиологические исследования, проведенные на 14, 30 и 90 день от начала терапии, и их результаты представлены на рис 5 и 6.
Обсуждение
В результате спринцевания, применения противозачаточных средств, содержащих 9-ноноксинол, использования внутриматочных контрацептивов, смены половых партнеров, применения антибиотиков широкого спектра действия уменьшается доля лактобацилл в составе микрофлоры влагалища. Одновременно возрастает доля Gardnerella vaginalis, Mycoplasma hominis, анаэробных бактерий и развивается дисбактериоз влагалища – бактериальный вагиноз [4, 5].
БВ регистрируется у 5-17% практически здоровых женщин и у 30–38% пациенток, предъявляющих жалобы на выделения из половых путей. Эти женщины посещают как женские консультации, так и специализированные клиники для лечения ИППП. БВ достоверно чаще встречается у женщин моложе 25 лет. Данные о заболеваемости БВ широко расходятся вследствие отсутствия единого подхода к критериям диагностики: от изоляции G. vaginalis в ранних исследованиях до обнаружения смешанной микробной флоры при микроскопии в современных работах. Различия в частоте выявления бактериального вагиноза зависит от исследования различных групп женщин как посещающих сеть первичной медицинской службы, так и тех, которые обращаются в кожно-венерологические диспансеры. У части женщин (5-25%) БВ протекает бессимптомно [10, 13, 14], вследствие чего признаки заболевания легко перепутать с нормальными выделениями.
Что касается диагностики бактериального вагиноза, то наиболее часто используются критерии Амселя. В 1983 году R. Amsel и соавторы предложили диагностировать бактериальный вагиноз на основе 4 критериев: наличия специфических жидких гомогенных выделений из влагалища, значения рН вагинальных выделений выше 4,5, положительного аминового теста и наличия ключевых клеток при микроскопическом исследовании вагинальных выделений [6]. Именно на основании этих критериев проводился отбор пациентов для представленного исследования. На сегодняшний день известно еще несколько методов диагностики бактериального вагиноза, описанных Nugent R.P. и соавт., K. Ison и соавт., A. Hallen, Е.Ф. Кира, в наших методических рекомендациях [2-5, 8,11].
При использовании микроскопических методов диагностики бактериального вагиноза необходимо обращать внимание не только на наличие ключевых клеток, но на такой показатель как отношение лейкоцитов к клеткам плоского эпителия, а также на наличие или отсутствие лактобацилл. При физиологическом микробиоценозе влагалища отношение лейкоцитов к эпителию равно 1:1. При бактериальном вагинозе лейкоцитов меньше, чем эпителия, соответственно, это отношение меньше 1 [2-4, 7], что мы использовали в нашем исследовании как один из объективных показателей заболевания.
Для лечения бактериального вагиноза большинство международных руководств, таких как CDC, IUSTI и др. рекомендует использовать исключительно метранидазол в разных дозах и клиндамицин [15]. Наши собственные исследования по использованию клиндамицина в лечении бактериального вагиноза у женщин с сахарным диабетом 1 типа показали хорошие результаты [1]. Поэтому в качестве основного препарата для лечения бактериального вагиноза мы выбрали именно клиндамицин вагинальный крем. Этот препарат назначался всем пациентам с установленным диагнозом.
Большинство современных публикаций свидетельствует о неэффективности противоанаэробной терапии бактериального вагиноза, т.к. она сопровождается более чем в 30% случаев рецидивами. Ряд отечественных и зарубежных исследователей поддерживает идею двухэтапного лечения этого состояния. На первом этапе применяется специфический антибактериальный препарат, а на втором этапе назначаются пробиотики или препараты, способствующие восстановлению нормальной физиологической микрофлоры, в частности, лактобацилл. В вагинальном отделяемом женщин репродуктивного возраста идентифицировано более 150 видов лактобацилл. Поэтому важно подбирать препараты, которые создают условия для размножения собственных эндогенных лактобацилл.
В данном исследовании мы применяли препарат «Эпиген интим», содержащий активированную глицирризиновую кислоту. Исследование было двойным слепым плацебо контролируемым. Рассмотрение динамики изменения использованных в работе показателей позволяет говорить о благоприятном влиянии препарата «Эпиген интим» в комплексном лечении бактериального вагиноза: в более короткий срок прекращается неприятный запах влагалищных выделений, жалобы пациенток на дискомфорт в области влагалища, быстрее снижается значение рН влагалищных выделений и присутствие в них «ключевых» клеток. Микроскопическое и культуральное исследование выявляет значимое увеличение лактобацилл у женщин, которым проведено комбинированное лечение препаратом «Эпиген интим», в сравнении с теми пациентами, которым заменен этот перпарат на плацебо и с теми, которые получали только клиндамицин.
Полученные результаты дают основание рекомендовать препарат «Эпиген интим» для включения его в схемы комплексного лечения бактериального вагиноза как беременных, так и небеременных женщин, т.к. он способствует улучшению микроэкологии влагалища..
Заключение
Проведенное исследование свидетельствует о клинической и микробиологической эффективности препарата «Эпиген интим» спрей для местного и наружного применения в терапии бактериального вагиноза 2 раза в день в течение 10 дней в сравнении с плацебо и с традиционной терапией. Отмечено более быстрое исчезновение жалоб и клинических проявлений заболевания после окончания терапии, а также на 30 и 90 день терапии в группе женщин, которым кроме стандартной терапии был назначен «Эпиген интим» спрей, по сравнению с группой, получавшей плацебо, и с контрольной группой, получавшей только стандартную терапию. У всех женщин основной группы после лечения в выделениях влагалища исчезли ключевые клетки и в составе вагинального микробиоценоза появились лактобациллы. Это свидетельствует о положительном влиянии препарата «Эпиген Интим» спрей для местного и наружного применения на микробиоценоз влагалища, в частности, на размножение лактобацилл, входящих в состав физиологического микробиоценоза каждой женщины.
Таким образом, препарат «Эпиген Интим» спрей для местного и наружного применения может быть включен в комплексную схему терапии бактериального вагиноза.
Данная статья предоставлена специалистом нашей клиники:
Менуховой Юлией Николаевной


Бактериальный вагиноз: место пероральной пробиотической терапии
Общая численность микроорганизмов, заселяющих различные органы человека, достигает порядка 1015, т. е. число микробных клеток примерно на два порядка превышает численность собственных клеток макроорганизма.
Общая численность микроорганизмов, заселяющих различные органы человека, достигает порядка 1015, т. е. число микробных клеток примерно на два порядка превышает численность собственных клеток макроорганизма. Значительная часть (более 60%) микрофлоры заселяет различные отделы желудочно-кишечного тракта, примерно 15% приходится на ротоглотку, на урогенитальный тракт — 11%(из них на вагинальный отдел — 9%), 14% — на кожные покровы. Одновременная эволюция организма хозяина и микроорганизмов благодаря двунаправленному обмену способствовала закреплению взаимовыгодных коллективных взаимодействий. Резидентные микроорганизмы, взаимодействующие с человеком на протяжении тысячелетий, контактируют с толл-подобными рецепторами (toll-like receptors (TLR)) слизистых оболочек пищеварительного тракта. Активация TLR влияет на секрецию цитокинов мукоцитами, воздействуя, таким образом, на дальнейший процессинг и презентацию антигенов бактерий клеткам хозяина, выработку и секрецию иммуноглобулина А, связанного с секреторным компонентом лизоцима, лактоферрина и других биологически активных веществ.
Взаимодействие между физиологической микрофлорой и организмом хозяина происходит на поверхности слизистых оболочек, из которых самой большой по площади является слизистая оболочка кишечника.
Попытки воздействовать на кишечный биоценоз и через него — на здоровье человека имеют долгую историю. Еще И. И. Мечников в 1910 г. предлагал использовать кисломолочные продукты для омоложения и продления жизни.
Сегодня фармацевтический рынок предлагает практическому врачу широкий спектр лекарственных средств, способствующих нормализации микробиоценоза толстой кишки. Все средства, положительно влияющие на состав кишечной микрофлоры, можно разделить на пробиотики, пребиотики и синбиотики.
Пробиотики представляют собой гетерогенную группу непатогенных бактерий. С 30-х годов прошлого столетия ведут отсчет препараты, содержащие лактобактерии и бифидобактерии, так называемые пробиотики. В соответствии с определением рабочей группы ВОЗ к ним относят живые микроорганизмы, которые при применении в адекватных количествах вызывают улучшение здоровья организма-хозяина.
Препараты, входящие в группу пробиотиков, должны соответствовать следующим требованиям:
В ходе международного конгресса гастроэнтерологов (Монреаль, 2005 г.) было дано определение пробиотиков как препаратов на основе кишечных комменсалов, способных осуществлять биологический контроль в организме и обладающих регуляторными, триггерными свойствами. Такой биологический потенциал пробиотиков объясняется многочисленными метаболическими эффектами энтеральной микрофлоры, включая синтез витаминов В и К, короткоцепочечных жирных кислот, инактивацию пищевых канцерогенов, бактериальную ферментацию некоторых лекарственных препаратов, синтез сигнальных молекул и др.
К пробиотикам относят такие препараты, как Линекс, Энтерол, Бактисубтил, Бифидумбактерин, Лактобактерин и др. Пробиотики подразделяются по количеству входящих в состав препарата культур на монокомпонентные (Бифидумбактерин, Энтерол, Бактисубтил и т. д.) и поликомпонентные (Линекс), а также по свойству пробиотической культуры на самоэлиминирующиеся антагонисты (Энтерол, Бактисубтил) и на бифидосодержащие, лактосодержащие и колисодержащие. Например, препарат Линекс относится к поликомпонентным бифидо- и лактосодержащим пробиотикам, так как в его состав входят три микроорганизма — Bifidobacterium infantis, Lactobacillus acidophilus и Enterococcus faecium. Комбинированные пробиотики отличаются большей эффективностью в сравнении с монокомпонентными: лактобактерии и энтерококк преимущественно колонизируют тонкую кишку, а бифидобактерии — толстую, поэтому пробиотические культуры наиболее физиологично поддерживают колонизационную резистентность и способствуют выполнению функций индигенной кишечной микрофлоры.
Пребиотики представляют собой стабилизаторы среды обитания и стимуляторы роста нормальной микрофлоры. В эту группу входят препараты, относящиеся к различным фармакотерапевтическим группам, но обладающие общим свойством — стимулировать рост и развитие нормальной микрофлоры кишечника. К пребиотикам относят лактулозу, глюкозу, протеины, камедь, аминокислоты, витамины и минералы, каолин, пищевые волокна, инулин и олигофруктозу.
Комбинированные средства, сочетающие в себе как про-, так и пребиотический компоненты, относят к синбиотикам (например, Линекс Био).
Действие пероральной пробиотической терапии не сводится к простому заселению кишечника, как это зачастую представляется. Их влияние более сложно и многопланово. Это и конкуренция с патогенной и условно-патогенной микрофлорой; адгезия к слизистой оболочке кишечника и взаимодействие с эпителиоцитами; иммуномодулирующий эффект. Микробные липополисахариды и гликопептиды пробиотической флоры взаимодействуют с TLR с последующей передачей стимулирующего импульса на белок NFkB, вследствие чего последний транспортируется в ядро клетки. Активация NFkB приводит к переключению дифференцировки Th0-лимфоцитов на Thl-путь и стимуляции выработки провоспалительных цитокинов. Пробиотические штаммы лактобактерий (LGG, L. acidophylus), E. faecium, Str. thermophylus воспринимаются TLR и стимулируют ответ хозяина, усиливая выработку Th1 и IL-1, INF-альфа. Они стимулируют фагоцитарную активность нейтрофилов и выработку sIgА. В то же время бифидобактерии оказывают стимулирующее воздействие на Th-reg и, соответственно, выработку TGF-бета, IL-10, способствуя формированию иммунологической толерантности. Этот процесс сопровождается снижением синтеза IgE и усилением синтеза sIgA. Наиболее активно повышают уровень IL-10 В. longum, B. bifidum, B. infantis. Пробиотики, в состав которых входят симбионтные штаммы бактерий, аэробы и анаэробы, вероятно, могут оказывать более многоплановое и мощное иммуномодулирующее действие, чем монокомпонентные препараты.
Иммунорегулирующее действие пробиотиков расширяет возможности их использования и раскрывает широкие перспективы для применения в разных клинических ситуациях. Например, с позиций гастроэнтеролога эффективность пробиотических средств изучается в лечении заболеваний, ассоциированных с инфекцией Helicobacter pylori, воспалительных заболеваний кишечника, диффузных заболеваний печени, а также функциональной патологии кишечника. Мы имеем собственный опыт применения поликомпонентного пробиотика Линекс в лечении пациентов с язвенной болезнью, ассоциированной с инфекцией H. pylori. Эффективность включения Линекса в качестве препарата сопровождения к стандартной эрадикационной терапии тестировалась в открытом когортном проспективном рандомизированном (метод простой рандомизации с помощью конвертов) исследовании с включением 30 пациентов. Полученные нами данные свидетельствуют, что комбинация стандартной антихеликобактерной терапии с пробиотиком существенно снижает частоту развития синдрома кишечной диспепсии посредством протективного действия в отношении кишечного микробиоценоза, повышает приверженность пациентов к лечению и, таким образом, способствуют эрадикации инфекта.
Иммуногенный потенциал пробиотических средств привлекает внимание не только специалистов-гастроэнтерологов, но и врачей других специальностей, являясь отражением необходимости междисциплинарного подхода к восстановлению микроэкологического статуса макроорганизма. Так, проблема лечения и профилактики рецидивирующего бактериального вагиноза все чаще заставляет искать возможности восстановления физиологической микрофлоры влагалища путем нормализации кишечного биотопа для достижения адекватного функционирования местного иммунного ответа слизистых оболочек.
Бактериальный вагиноз — общий инфекционный невоспалительный синдром, связанный с дисбиозом влагалищного биотопа и сопровождающийся чрезмерно высокой концентрацией облигатно- и факультативно-анаэробных условно-патогенных микроорганизмов и резким снижением или отсутствием молочнокислых бактерий в отделяемом влагалища. Трудности в курации пациенток с бактериальным вагинозом определяются нередким сочетанием с папилломавирусной инфекцией (ПВИ) гениталий у женщин и другими инфекциями, передаваемыми половым путем (ИППП). Восстановление микробиоценоза влагалища уменьшает риск ИППП, и способствует улучшению репродуктивного здоровья и качества жизни женщин.
Пероральная терапия пробиотиками в лечении бактериального вагиноза
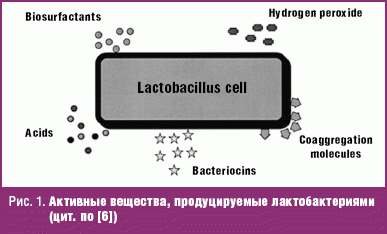
Предпосылкой к разработке схем терапии бактериального вагиноза с включением в антибактериальную терапию приема пробиотических культур послужило появление доказательств об эффективности определенных штаммов пробиотических культур при прямом введении во влагалище или когда они восходят из прямой кишки после перорального приема, а также благодаря их иммуногенному потенциалу. Как минимум для двух штаммов лактобактерий (Lactobacullus rhamnosus GR-1 и L. fermentum RC-1) доказана возможность колонизации влагалища восходящим путем. Основной акцент в отношении лактобактерий сделан в связи с тем, что именно лактобациллы доминируют в микробном пейзаже влагалища. Эти физиологические бактерии продуцируют кислоты, бактериоцины, перекись кислорода, биосульфактанты, препятствуют колонизации патогенной и грибковой флоры (рис. 1).
Результаты проведенных контролируемых исследований подтверждают положительный эффект применения пробиотиков, в том числе и перорально, при бактериальном вагинозе, рецидивирующих инфекциях мочеполового тракта и вульвовагинальном кандидозе у женщин. В 2007 году был опубликован систематизированный обзор, включивший результаты адекватных контролируемых исследований, посвященных оценке эффективности пробиотической терапии в лечении больных бактериальным вагинозом. Результаты клинических исследований с пероральным приемом пробиотиков разнились в зависимости от стартового фона микробиоценоза (не только влагалища, но и кишечника), наличия сопутствующей соматической патологии, а также вида назначенных пробиотических культур. Вместе с тем была отмечена эффективность, статистически достоверно превышающая эффект плацебо, перорального приема культур L. аcidophilus, L. rhamnosus GR-1, L. fermentum RC-14 при условии их приема от 14 дней до 2 месяцев в лечении бактериального вагиноза.
Эффективность пробиотических культур, содержащих лактобактерии, в качестве средств сопровождения к антибактериальной терапии, статистически достоверно выше плацебо и составляет от 60% (р = 0,004) до 88% (р Купить номер с этой статьей в pdf