Легочная гипертензия что это такое у детей
Легочная гипертензия новорожденных
Персистирующая легочная гипертензия новорожденных – это персистирование или возврат к состоянию констрикции артериол легких, из-за чего уменьшается кровоток в легких младенца, и возникает право-левый сброс крови.
Формы легочной гипертензии у новорожденных:
Первичную легочную гипертензию диагностируют у младенцев, которые недавно родились, и у которых нет яркой симптоматики и рентгенологических свидетельств патологии легких. После рождения в скором времени происходит развитие стойкой гипоксемии. Но уровень PaСО 2 в норме или незначительно снижено. Причиной может являться первичное нарушение функции механизмов легочной вазодилятации.
Вторичная легочная гипертензия новорожденного бывает при тяжелых, в основном паренхиматозных, болезнях легких. Это усложняет течение болезни и ухудшает прогноз. Легочная гипертензия у детей часто проходит вместе с синдромом аспирации меконием, респираторным дистресс-синдромом, пневмонией, диафрагмальных грыжах и прочих формах ЛГ. В таких случаях легочная вазоконстрикция имеет связь с гипоксией.
Первичная гипертензия легких у новорожденных встречается в 1-3 случаях из 1 тысячи. Диагноз типичен для переношенных и нормально доношенных детей. При кесаревом сечении ЛГН встречается в 5 раз чаще, чем при родах нормальным путем. Легочная гипертензия у недоношенных бывает редко – недоношенные среди общего количества детей с таким диагнозом составляют всего 15-35%.
Окружающая легочные артериолы гладкая мускулатура развивается только на 28-й неделе и позже – к концу гестации. Потому легочная гипертензия – не так проблема, которая актуальна для рожденных прежде срока детей. структура и функции сосудов легких эмбриона меняются, когда он растат. Обмен газа у плода совершается за счет плаценты, а не за счет легких. Менее 10%-ти смешанной крови, которая вышла из желудочка, циркулирует через легочную сосудистую систему, а большой процент крови из правого желудочка выходит в артериальный проток, попадает в аорту, откуда через восходящую аорту к верхним конечностям и голове.
Что провоцирует / Причины Легочной гипертензии новорожденных:
Персистирующая легочная гипертензия новорожденных возникает во многих случаях по причине перинатальной гипоксии или асфиксии. Часто происходит мекониальное окрашивание околоплодных вод, или же в анамнезе фиксируют меконий в трахее. Гипоксия провоцирует возврат или персистирование выраженной констрикции артериол в легких, что является нормальным у плода.
Среди дополнительных причин выделяют преждевременное закрытие артериального протока или овального отверстия, что вызывает увеличение легочного кровотока у плода. Причиной может быть прием беременной нестероидных противовоспалительных препаратов. Также причина может заключаться в полицитемии – заболевании, при котором происходит нарушение тока крови.
Частая причина болезни – врожденная диафрагмальная грыжа. При этом диагнозе левое легкое очень гипоплазировано, потому большой объем крови идет в правое легкое. Еще одна причина – неонатальный сепсис. Какая бы ни была причина возникновения легочной гипертензии новорожденных, повышенное давление в легочной артерии вызывает аномальное развитие и гипертрофию гладкой мускулатуры стенок легочных артерий малого калибра и артериол, а также право-левый сброс крови через артериальный проток или овальное окно, что приводит к стойкой системной гипоксемии.
Патогенез (что происходит?) во время Легочной гипертензии новорожденных:
Нарушается функция эндотелия – внутренней оболочки сосудов. Начинается избыточная выработка сосудосуживающих веществ, а образование образования сосудорасширяющих веществ наоборот уменьшается. Происходит воспалительный процесс на уровне эндотелия капилляров, развивается тромбоз на определенном участке. В ответ на гипоксию возникает спазм легочных капилляров – снижается содержания кислорода. В патогенезе имеет важное значение избыточное разрастание мышечных компонентов сосудистой стенки легочных капилляров.
Выше описанные изменения становятся причиной сужения просвета сосудов легких. Также увеличивается сосудистое сопротивление и растет давление в системе легочной артерии. Это приводит к тому, что нагрузка на сердце становится значительно больше. Результатом становится сердечная недостаточность у новорожденного.
Симптомы Легочной гипертензии новорожденных:
Основными симптомами являются втяжение податливых мест грудной клетки, тахипноэ, снижение сатурации кислорода, выраженный цианоз. Кислородотерапия при этом эффективных результатов не дает. У младенцев с право-левым шунтом через открытый артериальный поток оксигенация в правой плечевой артерии выше, чем в нисходящей аорте. По этой причине цианоз может быть неодинаков. То есть сатурация кислорода на ногах приблизительно на пять процентов ниже, чем на верхней правой руке.
Диагностика Легочной гипертензии новорожденных:
Легочную гипертензию новорожденных подозревают у малышей, которые родились вовремя или позже назначенного срока, и у которых есть артериальная гипоксемия и/или цианоз. Также в диагностике помогает соответствующий анамнез. У ребенка отсутствует увеличение сатурации кислорода при дыхании 100 % кислородом, что является важным диагностическим признаком.
Методами подтверждения диагноза являются эхокардиография с допплерографией. Они подтверждают повышенное давление в легочной артерии. Также они необходимы для исключения врожденного порока сердца, который можно перепутать с рассматриваемым заболеванием. Рентген показывает, что легочные поля в норме или есть изменения, которые адекватны причине болезни:
Лечение Легочной гипертензии новорожденных:
У детей с диагнозом «персистирующая легочная гипертензия новорожденных» происходит нарушение слуха, задержка в развитии, функциональные нарушения. Терапию кислородом нужно начинать медленно, чтобы болезнь не развивалась далее. Кислород подается при помощи мешка и маски или аппаратной ИВЛ. Высокочастотная осцилляторная вентиляция позволяет расправить и вентилировать легкое, баротравма вместе с этим минимизируетс\.
При вдыхании ребенком оксид азота расслабляет гладкую мускулатуру сосудов, расширяет артериолы легких. Потому кровоток в легких увеличивается, оксигенация улучшается примерно у половины пациентов быстро. Начальная доза составляет 20 ррт, в дальнейшем ее нужно снижать, чтобы поддержать эффект.
При с тяжелой гипоксической дыхательной недостаточности можно применять такой метод как экстракорпоральная мембранная оксигенация. Индекс оксигенации при этой форме болезни выше 35-40, несмотря на максимальную респираторную поддержку. Нужно поддерживать нормальные уровни электролитов, жидкости, кальция, глюкозы. Ребенок должен находиться в помещении с оптимальной температурой. Ему дают антибиотики, пока не получат результаты посева, когда можно будет понять, сепсис этот или нет.
К каким докторам следует обращаться если у Вас Легочная гипертензия новорожденных:
Легочная гипертензия: взгляд детского пульмонолога
Опубликовано в журнале: «ПРАКТИКА ПЕДИАТРА»; июнь; 2016; стр. 10-15.
С.Э. Дьякова, к. м. н., в. н. с. отдела хронических воспалительных и аллергических болезней легких ОСП НИКИ педиатрии им. Ю.Е. Вельтищева
ГБОУ ВПО РНИМУ им.Н.И. Пирогова Минздрава России, г. Москва
Ключевые слова: легочная гипертензия, пульмонология, дети
Keywords: pulmonary hypertension, pulmonology, children
В практике детского пульмонолога пациенты с легочной гипертензией (ЛГ) встречаются относительно нечасто: по статистике, ЛГ имеют примерно 1,9 на 1000 рождающихся ежегодно детей, а распространенность легочной артериальной гипертензии составляет 15 случаев на 1 млн человек [5, 11, 18].
Хронические заболевания легких в 80-90% случаев являются причиной формирования хронического легочного сердца и сопровождаются развитием ЛГ у 30-50% больных. При отсутствии своевременной адекватной диагностики и лечения эта патология может быстро приводить к фатальному исходу. Установлено, что декомпенсированное хроническое легочное сердце в 30-37% случаев служит причиной смерти от недостаточности кровообращения и составляет 12,6% в структуре причин летальности от сердечно-сосудистых заболеваний. Причем многие причины ЛГ у детей значительно отличаются от таковых у взрослых пациентов [3, 5].
Известно, что малый круг кровообращения состоит из сосудистых элементов, которые находятся в анатомической и функциональной взаимосвязи. Разветвленная сеть артериовенозных анастомозов соединяет терминальные артериолы с легочными венами. В норме объем кровотока, минующего капилляры, невелик. Изменения тонуса стенки анастомозов обеспечивает расширение и сужение их просвета вплоть до полного закрытия. При повышении легочного артериального давления анастомозы, обеспечивая кровоток в обход капилляров, ограничивают этим дальнейшее повышение давления и предотвращают перегрузку давлением правого желудочка (ПЖ) [3, 6].
При этом малый круг кровообращения (МКК) осуществляет депонирование крови, обеспечение питанием респираторной ткани легких, реабсорбцию альвеолярной жидкости (дренажная функция) и нейтрализацию эмболов в венозной крови (фильтрационная функция), а также отвечает за транспортировку крови и газообмен.
В зависимости от локализации сопротивления кровотоку различают прекапиллярную, капиллярную и посткапиллярную ЛГ. Прекапиллярная ЛГ характеризуется нарастанием сопротивления в артериальном отделе МКК, что обусловлено падением парциального давления кислорода в альвеолах при обструктивных заболеваниях легких, системных васкулитах и тромбоэмболических осложнениях, а также при ограничении подвижности грудной клетки при кифосколиозе, ожирении и пневмофиброзе. Капиллярная ЛГ возникает при несоответствии объема кровотока и капиллярного русла. При заболеваниях легких эта форма гипертензии часто сочетается с прекапиллярной, поэтому условно объединяется с ней. Посткапиллярная ЛГ развивается при повышении давления в левом предсердии более 20 мм рт. ст. и наблюдается при митральных пороках и левожелудочковой недостаточности. Длительное повышение давления способствует развитию необратимых органических изменений сосудистого русла МКК, которые и становятся причиной стойкой и прогрессирующей ЛГ [3, 6].
Существующие современные международные рекомендации по диагностике и лечению ЛГ, созданные в 2009 году объединенной рабочей группой Европейского кардиологического (ESC) и Европейского респираторного обществ (ERS), одобрены различными авторитетными профессиональными врачебными Ассоциациями и дополнены в 2015 году экспертами Американской кардиологической ассоциации (AHA) и Американского общества специалистов в области торакальной медицины [1, 5, 11, 18, 20].
ЛГ представляет собой патофизиологическое явление, к которому может приводить целый ряд клинических состояний, в частности, она может осложнять большинство сердечно-сосудистых заболеваний и болезней дыхательной системы. Согласно классификации ЛГ 2008 года, выделяют пять основных типов ЛГ:
1. Легочная артериальная гипертензия (включающая два подтипа: веноокклюзивная болезнь легких и/или легочный капиллярный гемангиоматоз и персистирующая ЛГ у новорожденных).
2. ЛГ вследствие патологии левых отделов сердца.
3. ЛГ вследствие болезней легких и/или гипоксии.
4. Хроническая тромбоэмболическая ЛГ и прочие варианты обструкции легочной артерии.
5. ЛГ с неясными и/или многофакторными механизмами.
У детей наиболее часто встречается легочная артериальная гипертензия и ЛГ, ассоциированная с патологией дыхательной системы и/или гипоксией [1, 5].
Среди причин ЛГ, ассоциированной с патологией дыхательной системы и/или гипоксией, основными являются хронические обструктивные заболевания легких; к более редким этиологическим факторам ЛГ этого типа в детском возрасте относятся пороки развития бронхолегочной системы, интерстициальные заболевания легких, легочная патология со смешанными обструктивно-рестриктивными нарушениями, нарушения дыхания во время сна, альвеолярная гиповентиляция, высокогорная легочная гипертензия, легочная гипертензия вследствие хронических тромботических и/или эмболических заболеваний, а также системные заболевания с поражением легких (саркоидоз, гистиоцитоз легочных клеток Лангерганса, лимфангиоматоз, васкулиты).
Принципиально в развитии ЛГ можно выделить три стадии. На первой стадии увеличенное легочное давление является единственной гемодинамической аномалией: больные не имеют отчетливых симптомов заболевания, но может отмечаться одышка при физической нагрузке. На второй стадии при уменьшении сердечного выброса появляется развернутая клиническая симптоматика в виде гипоксемии, одышки, синкопальных состояний, при этом давление в ЛА сохраняется на стабильно высоком уровне. С появлением правожелудочковой недостаточности наступает третья стадия заболевания: несмотря на стабильно высокие значения легочного давления, резко падает сердечный выброс, появляются венозный застой и периферические отеки. Продолжительность каждой стадии может быть различной; течение ЛГ может быть острым и хроническим; быстро, умеренно и медленно прогрессирующим; крайне редко встречаются случаи спонтанного регресса заболевания.
Начальные признаки ЛГ при заболеваниях легких обычно маскируются проявлениями основного заболевания (приступный период бронхиальной астмы, спонтанный пневмоторакс, выраженный плевральный выпот и т. д.). Иначе протекает ЛГ при хронических обструктивных болезнях легких: ЛГ и вызванная ею патология сердца и недостаточность кровообращения занимают первое место среди осложнений этих заболеваний, определяют жизненный прогноз пациентов и эффективность их лечения.
Основной жалобой у детей с ЛГ бывает одышка. Именно поэтому нередко первым специалистом, к кому могут обращаться пациенты с ЛГ, является пульмонолог. В дебюте заболевания одышка возникает только при физической нагрузке, по мере прогрессирования заболевания одышка появляется в покое, иногда сопровождается приступами удушья. Чем выше давление в легочной артерии, тем ярче выражена одышка.
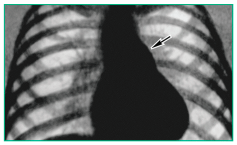
При рентгенографии органов грудной клетки у детей с ЛГ могут быть не только диагностированы заболевания легких, при которых характерна ЛГ (эмфизема легких, пневмосклероз, туберкулез, саркоидоз, пороки легких и т. д.), но и выявлены патогномоничные признаки ЛГ, такие как расширение корней легких, усиление легочного рисунка, общее или неравномерное повышение прозрачности легочных полей, интерстициальный отек, выбухание дуги ЛА по левому контуру, увеличение коэффициента Мура (процентное отношение поперечника дуги ЛА к половине диаметра грудной клетки на уровне диафрагмы (норма до 30%)), расширение нисходящей ветви правой ЛА (рис.). При этом индекс Мура и ширина правой ЛА коррелируют с высотой давления в ЛА и могут быть использованы в качестве критериев наличия и выраженности ЛГ. На ранних стадиях ЛГ до развития дилатации ПЖ размеры сердца могут не изменяться; по мере нарастания ЛГ и увеличения ПЖ на рентгенограмме грудной клетки в боковой проекции ретростернальное пространство выполняется тенью ПЖ. Еще большей информационной ценностью для верификации диагноза обладает компьютерная томография легких [1, 4, 6].
Рисунок
Повышение прозрачности легочной ткани, усиление легочного рисунка и выбухание дуги легочной артерии у ребенка 12 лет с ЛГ
При электрокардиографии ЛГ можно заподозрить по наличию признаков перегрузки и гипертрофии правых отделов сердца: отклонение электрической оси сердца вправо, перегрузка правого предсердия и правого желудочка, отрицательный зубец Т в грудных отведениях, транзиторная блокада правой ножки пучка Гиса [1, 3, 6].
Тем не менее, электрокардиография и рентгенография дают возможность лишь косвенно судить о наличии ЛГ. В течение длительного времени единственным методом исследования, позволявшим оценивать состояние правых отделов сердца, получать характеристики внутрисердечного кровотока и определять давление в правых отделах сердца и ЛА, была катетеризация правых отделов сердца и ЛА, которая на сегодняшний день продолжает использоваться для исключения кардиальных причин ЛГ (врожденные пороки сердца), определения основных параметров легочной и центральной гемодинамики, а также для подбора эффективных вазодилататоров. Однако, в силу инвазивности и высоких рисков осложнений, эта методика не может быть рекомендована для динамического наблюдения детей с ЛГ [11, 18].
Достоверно установлено, что показатели легочной гемодинамики при проведении ЭхоКГ сопоставимы с данными, полученными при катетеризации ЛА. В связи с этим всем младенцам с бронхолегочной дисплазией в анамнезе рекомендовано проведение эхокардиографического скрининга для исключения формирования ЛГ. При обследовании детей с ЛГ с помощью ЭхоКГ рекомендуется проведение теста с физической нагрузкой, который позволяет уточнять степень функциональных нарушений.
Немаловажным для дифференциальной диагностики ЛГ является определение газового состава крови, в частности, определение насыщения ее кислородом: снижение этого показателя наблюдается при сбросе крови справа налево, а также при ЛГ, сочетающейся с дыхательной недостаточностью (хронические обструктивные заболевания легких, массивная тромбоэмболия легочной артерии и т. д.) [1, 5, 11].
Исследование функции легких позволяет выявить вид и степень выраженности вентиляционных нарушений (обструктивные, рестриктивные смешанные). В целях дифференциальной диагностики, наряду со спирометрией, целесообразно проведение бодиплетизмографии и оценки диффузионной способности легких. У детей старше 6 лет для контроля переносимости нагрузок должна использоваться проба с 6-минутной ходьбой. Если ребенок относится к группе риска нарушений дыхания во сне, то в план его обследования должна включаться полисомнография.
Для верификации диагноза ЛГ в детской практике редко прибегают к открытой биопсии легких с последующим морфометрическим исследованием мелких сосудов, поскольку она сопряжена со значительными рисками и не обладает высокой информативностью в связи с неравномерным поражением сосудов легких.
Таким образом, диагностика ЛГ у детей предполагает проведение комплексного обследования с целью установления диагноза, оценки клинического класса и типа ЛГ, уровня давления в ЛА и оценки функционального и гемодинамического статуса пациентов с определением стадии заболевания.
У детей с хроническими бронхолегочными заболеваниями необходимо регулярное проведение комплексного кардиологического обследования (ЭКГ, ЭхоКГ) с целью диагностики патологии легочной гемодинамики и предупреждения формирования легочного сердца. Раннее выявление ЛГ позволяет начать своевременное лечение и предупредить развитие сердечной декомпенсации.
Основные подходы к лечению детей с ЛГ включают в себя ежедневные физические нагрузки по переносимости, что способствует улучшению качества жизни и уменьшению клинической симптоматики [16], а также профилактику инфекционных заболеваний (вакцинирование от гриппа и пневмококковой инфекции), исключение активного и пассивного курения. Наибольшее внимание должно быть уделено лечению основного заболевания, ликвидации гипоксии, снижению давления в малом круге кровообращения, профилактике дистрофической гипоксии миокарда и лечению правожелудочковой недостаточности [7].
Хотя гипоксия не является единственным этиологическим фактором ЛГ, однако развивающаяся гипоксемия у больных с хронической бронхолегочной патологией обусловливает необходимость применения кислорода в качестве терапевтического средства [21].
Тем не менее, специфической терапии ЛГ при хронической бронхолегочной патологии не разработано. В любом случае решение о назначении специфической терапии ЛГ у детей должно приниматься коллегиально, с учетом возрастных особенностей, тяжести течения и быстроты прогрессирования заболевания. В лечении больных с бронхиальной обструкцией, осложненной ЛГ, применение адреналина, норадреналина, эфедрина требует особой осторожности, так как они, помимо бронходилатирующего действия, вызывают гипертензивные реакции в малом круге кровообращения.
При неэффективности медикаментозного лечения проводится трансплантация легкого; в большинстве случаев для снижения давления в легочной артерии достаточно пересадки одного легкого. Двухлетняя выживаемость при трансплантации легкого составляет 60%, однако в отдаленные сроки у 50% больных развивается облитерирующий бронхиолит (проявление хронической реакции отторжения). На конечных стадиях высокой легочной гипертензии, особенно при сочетании с врожденными пороками сердца или кардиомиопатией, показана легочно-сердечная трансплантация; на начальных стадиях заболевания даже успешно выполненная операция не увеличивает продолжительность жизни таких больных [7].
Наибольшая эффективность лечения ЛГ у детей достигается в случае, если оно начато в ранний период болезни с применением средств, повышающих реактивность организма (лечебная физкультура, массаж, использование климатических факторов, иммуномодуляторов).
Комплексное лечение детей с ЛГ проводится непрерывно с соблюдением преемственности между стационаром, поликлиникой и санаторием-профилакторием; важность этого принципа вытекает из особенностей течения хронических бронхолегочных заболеваний, для которых и в фазе ремиссии необходима постоянная поддерживающая терапия.
Лечение легочной гипертензии у детей
Под легочной гипертензией (ЛГ) понимают состояние, при котором среднее давление в легочной артерии превышает 25 мм рт. ст. [1].
Под легочной гипертензией (ЛГ) понимают состояние, при котором среднее давление в легочной артерии превышает 25 мм рт. ст. [1].
Повышение давления в малом круге кровообращения у детей представляет собой частое явление и наблюдается при многих заболеваниях сердечно-сосудистой системы и аппарата внешнего дыхания. Распространенность легочной артериальной гипертензии составляет 15 случаев на 1 миллион человек [2]. Хронические заболевания легких в 80–90% случаев являются причиной формирования хронического легочного сердца и сопровождаются развитием ЛГ у 30–50% больных [3].
Современная классификация ЛГ была утверждена в 2008 г. на V Всемирном симпозиуме по легочной гипертензии, который состоялся в г. Дана-Пойнт (Калифорния, США) [4].
Классификация легочной гипертензии (2008 г.)
1. Легочная артериальная гипертензия:
1.1. Идиопатическая (первичная).
1.2. Наследственная.
1.2.1. Ген BMPR2.
1.2.2. Ген ALK1, эндоглин (с или без наследственной геморрагической телеангиоэктазии).
1.2.3. Неизвестной этиологии.
1.3. Связанная с лекарственными и токсическими воздействиями.
1.4. Ассоциированная с:
1.4.1. Cистемными заболеваниями соединительной ткани.
1.4.2. ВИЧ-инфекцией.
1.4.3. Портальной гипертензией.
1.4.4. Врожденными пороками сердца (системно-легочные шунты).
1.4.5. Шистосомозом.
1.4.6. Хронической гемолитической анемией.
1.5. Персистирующая легочная гипертензия новорожденных.
1. Легочная вено-окклюзионная болезнь и/или легочный капиллярный гемангиоматоз.
2. Легочная гипертензия, ассоциированная с поражениями левых отделов сердца:
2.1. Систолическая дисфункция.
2.2. Диастолическая дисфункция.
2.3. Поражения клапанного аппарата сердца.
3. Легочная гипертензия, ассоциированная с патологией дыхательной системы и/или гипоксией.
3.1. Хронические обструктивные заболевания легких.
3.2. Интерстициальные заболевания легких.
3.3. Легочная патология со смешанными обструктино-рестриктивными нарушениями.
3.4. Нарушения дыхания во время сна.
3.5. Альвеолярная гиповентиляция.
3.6. Высокогорная легочная гипертензия.
3.7. Пороки развития.
4. Легочная гипертензия вследствие хронических тромботических и/или эмболических заболеваний.
5. Смешанные формы.
5.1. Гематологические заболевания: миелопролиферативные заболевания, спленэктомия.
5.2. Системные заболевания: саркоидоз, гистиоцитоз легочных клеток Лангерганса, лимфангиоматоз, нейрофиброматоз, васкулиты.
5.3. Метаболические расстройства: с нарушением обмена гликогена, болезнь Гаучера, патология щитовидной железы.
5.4. Другие: опухолевая обструкция, фиброзирующий медиастинит, хроническая почечная недостаточность.
У детей наиболее часто встречается легочная артериальная гипертензия и ЛГ, ассоциированная с патологией дыхательной системы и/или гипоксией.
Тактика лечения ЛГ оперирует терминами доказательной медицины, такими как класс рекомендаций и уровень доказательности, а также учитывает функциональный класс тяжести заболевания (табл. 1, табл. 2).
Для характеристики тяжести ЛГ используется функциональная классификация Нью-Йоркской ассоциации сердца (табл. 3) [5].
Ключевые принципы терапии повышенного давления в малом круге кровообращения были сформулированы экспертами международных кардиологических и пульмонологических сообществ в 2003 и 2008 гг. в рамках Всемирных симпозиумов по легочной гипертензии и утверждены в качестве базисных практических рекомендаций как в Европе, так и в США. Согласно данным рекомендациям у детей возможно использовать терапевтический алгоритм, аналогичный применяемому у взрослых (класс рекомендаций IIа, уровень доказательности С) [1].
Целесообразна госпитализация пациентов в специализированные клинические центры. Детям с ЛГ необходим постоянный, динамичный контроль проводимого лечения и его коррекция при недостаточной эффективности. Основные цели при ведении пациентов с ЛГ — уменьшение симптоматики, улучшение качества жизни и повышение выживаемости.
Для всех без исключения больных ЛГ актуальны общие рекомендации, соблюдение которых позволяет уменьшить риск возможного ухудшения течения заболевания вследствие определенных обстоятельств и внешних факторов (табл. 4).
Больным ЛГ следует поддерживать адекватное состояние скелетной мускулатуры, выполняя ежедневные дозированные физические нагрузки, не вызывающие жалоб, что способствует улучшению качества жизни и уменьшению клинической симптоматики [6].
Профилактика инфекционных заболеваний является крайне важной задачей для больных ЛГ [7]. Следует рекомендовать пациентам вакцинирование от гриппа и пневмококковой инфекции.
Беременность и роды связаны с повышенным риском ухудшения течения заболевания и смертности у этой категории больных [8]. Всем пациенткам с ЛГ репродуктивного возраста должны быть рекомендованы соответствующие методы контрацепции.
На сегодняшний день детально разработаны подходы к лечению легочной артериальной гипертензии, являющейся наиболее изученной патологией по сравнению с другими вариантами заболевания и имеющей специфические подходы к базисной терапии (рис.) [1].
В лечении легочной артериальной гипертензии используют:
В табл. 5 представлена неспецифическая терапия ЛГ.
Кислород. При снижении парциального давления кислорода менее 60 мм рт. ст. необходимы сеансы кислородотерапии [9].
Дигоксин. Изменившиеся за последние 10–15 лет представления о механизме действия и эффективности сердечных гликозидов привели к пересмотру тактики и ограничению их показаний при лечении ЛГ. Сердечные гликозиды могут назначаться в редких случаях мерцательной аритмии у больных ЛГ для урежения желудочкового ритма. Вопрос о длительной поддерживающей терапии сердечными гликозидами, скорее всего, должен решаться отрицательно.
Диуретики. При наличии признаков застоя крови в большом круге кровообращения (периферические отеки, асцит) показана терапия диуретиками и ограничение потребления соли и жидкости. Положительный эффект лечения диуретиками у больных с ЛГ основан на уменьшении объемной перегрузки правого желудочка и периферического венозного застоя.
Антикоагулянты. Использование антикоагулянтов в педиатрии является спорным, так как отсутствуют исследования у детей, подтверждающие их эффективность и безопасность. Вместе с тем доказано наличие нарушений в системе гемостаза при ЛГ [10]. Многочисленными исследованиями продемонстрировано, что назначение антикоагулянтов улучшало прогноз у пациентов с высокой ЛГ.
Единственным широко используемым препаратом остается непрямой антикоагулянт варфарин, преимуществом которого является возможность перорального приема. Вместе с тем при использовании варфарина могут возникнуть определенные затруднения из-за необходимости постоянного контроля за уровнем протромбина в крови, а также вероятности массивных кровотечений per diapedezem при передозировке препарата. При приеме варфарина необходимо поддерживать международное нормализованное отношение на уровне 1,5–2,5. Как альтернативу варфарину при его непереносимости или повышенном риске кровотечений следует рассматривать применение стандартного гепарина. Гепарин также не лишен недостатков, что сдерживает его широкое использование при ЛГ. Это и необходимость частого подкожного введения (до 4 раз/сут) с постоянным контролем за его действием, а также возможность развития серьезных побочных реакций, таких как кровотечение, тромбоцитопения, остеопороз. В последние годы успешно внедряется в практику новый класс антикоагулянтных препаратов — низкомолекулярные гепарины. Одними из наиболее доступных из этой группы являются надропарин кальция (Фраксипарин), эноксапарин (Клексан) и далтепарин (Фрагмин).
Вазодилятаторы. Препаратами первого ряда в лечении ЛГ считаются блокаторы кальциевых каналов. Это простой и дешевый подход к длительной терапии ЛГ.
Блокаторы кальциевых каналов могут использоваться только у тех больных, у которых был выявлен положительный ответ на острый вазореактивный тест.
Ранее считалось, что до 40% детей с ЛГ являются так называемыми «ответчиками» при проведении теста. Однако в настоящее время установлено, что положительный ответ на острый вазореактивный тест отмечается только у 10–15% детей с ЛГ, и при этом лишь примерно у половины из них блокаторы кальциевых каналов оказывают клинически значимый гемодинамический эффект [11].
Не следует применять препараты этого ряда эмпирически в отсутствие данных о вазореактивности. При отрицательном вазореактивном тесте возможны выраженная системная гипотония, обмороки, правожелудочковая недостаточность.
При выборе блокатора кальциевых каналов следует учитывать частоту сердечных сокращений. При брадикардии назначается нифедипин или амлодипин, при тахикардии дилтиазем. Рекомендуется начинать с малых доз и постепенно повышать до максимально переносимых (под контролем системного АД и вероятных побочных эффектов).
В ситуации, когда в течение 2–3 месяцев отсутствует адекватный положительный эффект, который определяется как I функциональный класс по ВОЗ или II функциональный класс по ВОЗ с улучшением легочной гемодинамики, необходимо перейти к назначению так называемой специфической терапии ЛГ.
Таким образом, пациенты с ЛГ, которым не показано лечение блокаторами кальциевых каналов или у которых применение этих препаратов не было успешным, могут получить преимущества от других методов фармакотерапии.
Простагландины и их аналоги. Простаноиды — мощные вазодилятаторы с целым спектром дополнительных эффектов (антиагрегационным, антипролиферативным, цитопротективным). Благодаря этому простаноиды не только успешно снижают давление в легочной артерии, но и предотвращают (замедляют) ремоделирование легочных сосудов, препятствуют тромбообразованию в них. Доказано, что длительное использование внутривенных инъекций эпопростенола улучшает гемодинамику, функциональные возможности и выживаемость у пациентов с идиопатической легочной гипертензией и является предпочтительной терапией у многих тяжелых больных (прежде всего, при IV функциональном классе), хотя постоянное введение этого препарата остается неудобным в рутинной практике, а само лечение эпопростенолом довольно дорогостоящее.
В педиатрии доказана эффективность длительной терапии эпопростенолом в/в [12]. Доза препарата титруется в зависимости от клинического эффекта, субъективного и объективного. Начальная доза 2–4 нг/кг/мин, лечебная доза в диапазоне 20–40 нг/кг/мин. Учитывая необходимость постоянных медленных инфузий, постановки внутривенного катетера и ухода за ним, а также высокую степень индивидуализации дозировок в зависимости от массы тела пациента и переносимости препарата, практику введения эпопростенола рекомендовано ограничить теми центрами, в которых есть достаточный опыт использования этого препарата и системного наблюдения за получающими его пациентами. Трепростинил применяется при III и IV функциональном классе ЛГ.
Трепронистил для подкожного введения слишком болезненен при инъекции. В настоящее время также изучаются перспективы применения трепростинила в пероральной и ингаляционной формах. Илопрост является первым простаноидом, рекомендованным для лечения легочной гипертензии в виде аэрозоля для ингаляционного применения. Доза илопроста составляет 2,5–5 мкг/ингаляцию. В последние годы появляются сообщения о его эффективности в педиатрии [13]. Однако режим дозирования 6–12 раз в день вызывает затруднения у детей раннего возраста. Помимо ингаляционной, илопрост существует в пероральной и внутривенной формах. Влияние илопроста на долгосрочный прогноз остается еще недостаточно изученным. Берапрост — первый пероральный простаноид, доказавший свою эффективность в лечении ЛГ. Однако эффект берапроста недолговременный и при его приеме наблюдается много побочных эффектов. В настоящее время исследования берапроста в Европе и США прекращены.
Отмечено, что дети нуждаются в более высоких дозах простаноидов, чем взрослые, у них чаще развивается толерантность к препаратам, что требует постоянного контроля и коррекции дозы.
Ингибиторы фосфодиэстеразы-5. В настоящее время в лечении пациентов с ЛГ в качестве одних из наиболее перспективных препаратов могут рассматриваться силденафил и тадалафил. Исследования с силденафилом продолжаются очень активно, становятся все более масштабными и собирают все больше новых данных о перспективах монотерапии этим препаратом и его использования в комбинации с другими средствами для лечения легочной гипертензии. На данный момент FDA США одобрило применение силденафила в дозе 20 мг 3 раза в день перорально у взрослых с легочной артериальной гипертензией. В Европе утверждены аналогичные дозировки, однако долгосрочный эффект наблюдается при их повышении до 40–80 мг 3 раза в день [1].
Антагонисты эндотелиновых рецепторов являются наиболее изученными и приоритетными в лечении легочной гипертензии у детей.
Бозентан — пероральный антагонист рецепторов эндотелина А и В и первая молекула этого класса препаратов, которая была синтезирована и, следовательно, наиболее изучена. Препарат полностью блокирует нежелательные эффекты эндотелина при легочной гипертензии. Бозентан существенно замедляет темпы прогрессирования заболевания, способствует улучшению клинического течения ЛГ [14]. Показана высокая выживаемость пациентов с ЛГ, получавших бозентан [15].
По результатам последних исследований бозентан рекомендован в лечении ЛГ II функционального класса в США и Европе у детей с 2 лет, что делает его единственным разрешенным в педиатрии препаратом. В РФ бозентан используется в лечении легочной артериальной гипертензии у детей с 3-летнего возраста. Необходимо отметить, что бозентан — единственный зарегистрированный препарат для специфической терапии легочной артериальной гипертензии, имеющийся в данный момент на территории России. Детям бозентан назначают с учетом массы тела (табл. 6).
В терапии легочной артериальной гипертензии также возможно использование антагонистов эндотелиновых рецепторов ситаксентана и амбрисентана [1].
Вероятно, имеет смысл использовать комбинацию разных препаратов, учитывая различные точки приложения и возможность воздействовать на разные звенья патогенеза ЛГ, однако этот вопрос пока еще только изучается. Некоторые пилотные исследования уже подтверждают целесообразность такой тактики, и изучение эффективности и безопасности различных комбинаций лекарственных препаратов при легочной гипертензии проводится очень активно. Одной из наиболее сложных проблем при этом представляется суммирование побочных эффектов препаратов, которые, как правило, достаточно агрессивны для организма и в комбинации часто обусловливают неблагоприятный профиль безопасности. Пока что небольшие плацебо-контролируемые исследования демонстрировали перспективность комбинирования илопроста и бозентана, а также силденафила и эпопростенола.
Комплексное лечение ЛГ при хронических бронхолегочных заболеваниях у детей должно включать:
Наибольшая эффективность лечения достигается в случае, если оно начато в ранний период болезни с обязательным исключением курения у подростков, в том числе пассивного, и применением средств, повышающих реактивность организма (лечебная физкультура, массаж, использование климатических факторов, иммуномодуляторов).
Лечение проводится непрерывно с соблюдением преемственности между стационаром, поликлиникой и санаторием-профилакторием; важность этого принципа вытекает из особенностей течения хронических бронхолегочных заболеваний, для которых и в фазе ремиссии необходима постоянная поддерживающая терапия.
В лечении больных с бронхиальной обструкцией, осложненной ЛГ, применение адреналина, норадреналина, эфедрина требует особой осторожности, так как они, помимо бронходилятирующего действия, вызывают гипертензивные реакции в малом круге кровообращения.
Хотя гипоксия не является единственным этиологическим фактором ЛГ, однако развивающаяся гипоксемия у больных с хронической бронхолегочной патологией обусловливает необходимость применения кислорода в качестве терапевтического средства [16].
Специфической терапии ЛГ при хронической бронхолегочной патологии не разработано [1].
Часто используется медикаментозная терапия, направленная на снижение тонуса резистивных сосудов и включающая применение сосудорасширяющих средств различных групп [17, 18].
Терапия блокаторами кальциевых каналов имеет ряд ограничений и возможна не у всех больных. Следует помнить о возможности развития таких нежелательных эффектов, как усиление гипоксемии из-за увеличения перфузии плохо вентилируемых участков легких, системная гипотензия и тахикардия. Согласно последним данным группы экспертов ВОЗ при длительном применении обычных вазодилятаторов у пациентов с хронической бронхолегочной патологией и ЛГ обнаруживается их недостаточная эффективность.
В последние годы формируется представление, что применение ингибиторов АПФ целесообразно в лечении ЛГ при хронических бронхолегочных заболеваниях [19, 20]. Действие ингибиторов АПФ не ограничивается блокадой превращения ангиотензина I в активное прессорное вещество ангиотензин II. Другим их эффектом, также непосредственно связанным с инактивацией АПФ, является предупреждение деградации брадикинина, вызывающего релаксацию гладких мышц сосудов и способствующего высвобождению зависимого от эндотелия релаксирующего фактора — оксида азота. Кроме того, под влиянием ингибиторов АПФ снижается синтез других сосудосуживающих веществ (норадреналина, эндотелина-1). В последние годы выявлено положительное влияние ингибиторов АПФ на функциональное состояние эндотелия [21, 22].
Простаноиды, ингибиторы фосфодиэстеразы 5-го типа и антагонисты эндотелиновых рецепторов пока не нашли широкого применения в лечении хронического легочного сердца. Существуют лишь единичные исследования, показывающие эффективность специфической терапии ЛГ при хронической бронхолегочной патологии [23, 24]. Тем не менее, данная группа препаратов, на наш взгляд, имеет широкие перспективы в педиатрии.
При наличии признаков застоя крови в большом круге кровообращения (периферические отеки, асцит) показана терапия диуретиками и ограничение потребления соли и жидкости.
Назначение сердечных гликозидов не показано, за исключением упорно прогрессирующей недостаточности кровообращения, когда они применяются по витальным показаниям. В остальных случаях вероятность развития побочных эффектов значительно превышает минимальное положительное действие препарата.
Профилактика гипоксической дистрофии миокарда предусматривает применение средств, улучшающих питание миокарда.
Хирургические методы лечения легочной гипертензии
Межпредсердное шунтирование. Замечено, что открытое овальное окно у больных с высокой ЛГ улучшает прогноз заболевания и увеличивает продолжительность жизни. Данные клинические наблюдения подтверждаются в эксперименте путем хирургической атриосептостомии [25].
Трансплантация легкого. Трансплантация легкого проводится при неэффективности медикаментозного лечения. В большинстве случаев для снижения давления в легочной артерии достаточно пересадки одного легкого. Двухлетняя выживаемость при трансплантации легкого составляет 60%. В отдаленные сроки у 50% больных развивается облитерирующий бронхиолит (проявление хронической реакции отторжения).
Легочно-сердечная трансплантация. Проведение операции оправдано на конечных стадиях высокой легочной гипертензии, особенно при сочетании с врожденными пороками сердца или кардиомиопатиями. На начальных стадиях заболевания даже успешно выполненная операция не увеличивает продолжительность жизни таких больных. ЃЎ
Литература
Л. И. Агапитов, кандидат медицинских наук
Московский НИИ педиатрии и детской хирургии Росмедтехнологий, Москва