Левофлоксацин или ципрофлоксацин что эффективнее при пневмонии
Почему азитромицин остается препаратом выбора при внебольничных инфекциях нижних дыхательных путей
Инфекционно-воспалительные заболевания дыхательных путей занимают первое место в структуре инфекционной патологии. Пневмония является наиболее частой инфекционной причиной смерти в мире.
Инфекционно-воспалительные заболевания дыхательных путей занимают первое место в структуре инфекционной патологии. Пневмония является наиболее частой инфекционной причиной смерти в мире. В России ежегодно около 1,5 млн человек переносят пневмонию. В связи с этим остается актуальной проблема рационального выбора антибактериального средства для лечения инфекций нижних дыхательных путей. Выбор препарата для антибактериальной терапии должен основываться на его спектре действия, охватывающем выделенный или предполагаемый возбудитель, чувствительный к данному антибиотику, фармакокинетических свойствах антибактериального средства, обеспечивающих его проникновение в терапевтической концентрации в соответствующие ткани, клетки и жидкости организма, данных о безопасности антибиотика (побочных эффектах, противопоказаниях и возможном нежелательном взаимодействии с другими лекарствами), характеристиках лекарственной формы, способе введения и режиме дозирования, обеспечивающих высокий комплаенс терапии, фармакоэкономических аспектах лечения [4, 6, 8].
Инфекции нижних дыхательных путей и принципы выбора антибиотика
При неспецифических внебольничных инфекциях выбор антибактериального препарата в большинстве случаев основывается на статистических данных о наиболее частых их возбудителях, а также сведениях о подтвержденной в контролируемых клинических исследованиях эффективности тех или иных антибиотиков при инфекциях известной этиологии. Вынужденно эмпирический подход к лечению связан с отсутствием возможности микробиологического исследования в амбулаторных лечебных учреждениях, длительностью бактериологической идентификации возбудителя и определения его чувствительности к антибиотикам (3–5 дней, а в случае «атипичных» патогенов и больше), невозможностью в ряде случаев получить биологический материал для посева или бактериоскопии (например, около 30% больных пневмониями имеют непродуктивный кашель, что не позволяет исследовать мокроту), трудностями в разграничении истинных возбудителей и сапрофитов (обычно микроорганизмов ротоглотки, попадающих в исследуемый материал). Сложности выбора лекарственного средства в амбулаторных условиях определяются также отсутствием полноценного наблюдения за течением заболевания и, следовательно, своевременной коррекции лечения при его неэффективности. Антибиотики по-разному проникают в различные ткани и биологические жидкости. Лишь некоторые из них хорошо проникают в клетку (макролиды, тетрациклины, фторхинолоны, в меньшей степени — клиндамицин и сульфаниламиды). Поэтому, даже если препарат in vitro проявляет высокую активность в отношении данного возбудителя, но не достигает в месте его локализации уровня, превышающего минимальную подавляющую концентрацию (МПК) для данного микроорганизма, клинического эффекта он не окажет, хотя микробная резистентность к нему будет вырабатываться. Не менее важным аспектом антибактериальной терапии является ее безопасность, особенно для амбулаторного больного, лишенного повседневного медицинского наблюдения. В амбулаторных условиях следует отдавать предпочтение пероральному приему антибиотиков. В педиатрической практике имеют значение органолептические свойства препарата. Для повышения исполняемости пациентом врачебных назначений режим дозирования антибиотика должен быть максимально простым, т. е. предпочтительнее препараты с минимальной кратностью приема и коротким курсом лечения.
Возбудители неспецифических внебольничных инфекций нижних дыхательных путей
Острые респираторные вирусные инфекции (ОРВИ), протекающие с синдромом бронхита, в ряде случаев, чаще в детском возрасте, могут осложняться присоединением бактериальной флоры с развитием острого бронхита. Возбудителями острого бактериального бронхита в детском возрасте являются пневмококк, микоплазма или хламидия, реже гемофильная палочка, моракселла или стафилококк. Острый бактериальный бронхиолит у детей вызывают моракселла, микоплазма и возбудитель коклюша. Острый гнойный трахеобронхит у взрослых в 50% случаев вызывает гемофильная палочка, в остальных случаях пневмококк, реже моракселла (5–8% случаев) или внутриклеточные микроорганизмы (5% случаев).
Среди бактериальных возбудителей обострений хронического бронхита главную роль играют Haеmophilus influenzae (30–70% случаев), Streptococcus pneumoniae и Moraxella catarrhalis. Для курильщиков наиболее характерна ассоциация H. influenzae и M. catarrhalis. В отягощенных клинических ситуациях (возраст старше 65 лет, многолетнее течение болезни — более 10 лет, частые обострения — более 4 раз в год, сопутствующие заболевания, выраженные нарушения бронхиальной проходимости — объем форсированного выдоха за первую секунду (ОФВ1)
С. В. Лукьянов, доктор медицинских наук, профессор ФГУ «Консультативно-методический центр лицензирования» Росздравнадзора, Москва
Антибиотики нового поколения: за и против
Антибиотики – это вещества биологического или полусинтетического происхождения. Применяются в лечебной практике для борьбы с болезнетворными микробами, вирусами. До появления этих медпрепаратов статус неизлечимых болезней был у брюшного тифа, дизентерии, пневмонии, туберкулеза. Сегодня лечение заболеваний инфекционного характера возможно с применением 1-6 поколения антибиотиков.
На этот момент фармакологическая индустрия выпускает более 2000 разновидностей лекарственных средств подобного типа. Медики описали действие около 600 позиций, а во врачебной практике используются порядка 120-160 препаратов.
Важно! При любом заболевании принимать антибиотики рекомендуется после консультации с врачом. В противном случае может развиться антибиотикорезистентность (снижение чувствительности патогенных микроорганизмов к антибактериальным средствам).
Классификация антибиотиков
Все антибактериальные средства можно разделить на 5 категорий по характеристикам и спектру применения. Рассмотрим эту классификацию подробнее:
Спектр действия
Различают антибактериальные средства:
По составу
Антибактериальные препараты делят на 6 групп:
Поколения препаратов. У передовых антимикробных препаратов насчитывается уже шесть генераций. Например, пенициллин был первым средством природного происхождения, тогда как третья или шестая генерация – это уже улучшенная версия, которая включает в состав сильнейшие ингибиторы. Зависимость прямая: чем новее генерация, тем эффективнее воздействие препаратов на патогенную микрофлору.
По способу приема. Пероральные – принимают через рот. Это различные сиропы, таблетки, растворимые капсулы, суспензии. Парентеральные – вводятся внутривенно или внутримышечно. Они быстрее дают эффект, чем пероральные лекарства. Ректальные препараты вводятся в прямую кишку.
Важно! Принимать антибиотики допускается только после консультации с врачом, иначе разовьется антибиотикорезистентность.
Антибактериальные средства нового поколения
Отличие последних генераций антибиотиков от их ранних версий в более совершенной формуле действующего вещества. Активные компоненты точечно устраняют только патологические реакции в клетке. Например, кишечные антибиотики нового поколения не нарушают микрофлору ЖКТ. При этом они борются с целой «армией» возбудителей инфекций.
Новейшие антибактериальные препараты делятся на пять групп:
Рассмотрим несколько известных противомикробных средств импортного и российского производства.
Амоксициллин – импортный противомикробный препарат из группы пенициллинов. Используется во врачебной практике для лечения бактериальной инфекции. Эффективен при кишечных инфекциях, гайморите, ангине, болезни Лайма, дизентерии, сепсисе.
Авелокс – медпрепарат последней генерации из группы фторхинолонов. Отличается сильнейшим воздействием на бактериальные и атипичные возбудители. Не вредит почкам и ЖКТ. Используется при острых, хронических заболеваниях.
Цефалоспорины – антибиотики третьего поколения. К этой группе относят Цефтибутен, Цефтриаксон и другие. Используются для лечения пиелонефрита, пневмонии. В целом это безопасные средства с малым количеством побочных действий. Однако их нужно принимать только после консультации с врачом. Медпрепаратов много, а какой именно выбрать – порекомендует специалист.
Дорипрекс – импортный противомикробный препарат синтетического происхождения. Показал хорошие результаты при лечении пневмонии, запущенных интраабдоминальных инфекций, пиелонефритах.
Инваз – антибактериальное средство из группы карбапенемов. Выпускается в ампулах для парентерального способа применения. Показывает быстрый эффект при лечении бактериальных расстройств кожи, мягких тканей, инфекциях мочевыводящих путей, пневмонии, септицемиях.
Аугметин – полусинтетический пенициллин третьей генерации с добавлением усиливающих ингибиторов. Педиатрами признается лучшим комплексным медпрепаратом для лечения детских гайморита, бронхита, тонзиллита и других инфекций дыхательных путей.
Цефамандол – антибактериальное средство российского производства. Относится к группе цефалоспоринов третьего поколения. Используется для лечения кишечных инфекций, возбудителей инфекций половых органов. Как противомикробное средство обширного диапазона воздействия применяется при простудных заболеваниях.
Лучшие антибактериальные препараты широкого диапазона действия
Противомикробные средства новой генерации обычно синтезируют из природного сырья и стабилизируют в лабораториях. Это помогает усилить эффект лекарства на патогенную микрофлору.
Какие препараты самые сильные? Врачи относят к таким антибактериальные средства широкого спектра воздействия. Приведем ниже краткий список препаратов по названиям:
Резюме
Мы рассмотрели российские и импортные антибиотики широкого спектра действия, кратко описали классификацию препаратов. Ответим на вопрос: какие антибактериальные средства выбрать?
Важно понимать, противомикробные лекарства для обширного применения обладают токсичностью, поэтому негативно влияют на микрофлору. Кроме того, бактерии мутируют, а значит препараты теряют свою эффективность. Поэтому антибактериальные средства с новейшей структурой будут в приоритете, чем их ранние аналоги.
Самолечение антибиотиками опасно для здоровья. При инфекционном заболевании первым делом нужно обратиться к врачу. Специалист установит причину болезни и назначит эффективные антибактериальные средства. Самолечение «наугад» приводит к развитию антибиотикорезистентности.
Клиническая фармакология левофлоксацина
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В настоящее время фторхинолоны (ФХ) рассматриваются, как важная группа химиотерапевтических препаратов в пределах класса хинолонов – ингибиторов ДНК–гиразы, характеризующихся высокой клинической эффективностью (в том числе при оральном применении), широкими показаниями к применению и составляют серьезную альтернативу другим антибиотикам широкого спектра. Создано более 15 препаратов группы ФХ, несколько новых активных соединений проходят клиническое исследование с целью получения более эффективных препаратов в отношении грамположительных микроорганизмов, микобактерий, анаэробов, атипичных возбудителей. Важной задачей является также разработка препаратов с минимальным риском побочных эффектов и высокой клинической эффективностью.
Среди ФХ в настоящее время выделяются две группы препаратов: ранние или старые (норфлоксацин, ципрофлоксацин, офлоксацин, пефлоксацин, ломефлоксацин и др.) и новые или поздние (левофлоксацин, спарфлоксацин, гатифлоксацин, гемифлоксацин и др.).
Офлоксацин применяется уже более 15 лет, обладает высокой эффективностью, хорошей переносимостью, низким уровнем побочных эффектов и отсутствием значимого межлекарственного взаимодействия. С точки зрения стереохимии офлоксацин представляет собой рацемическую смесь двух оптически активных изомеров: левовращающего (L–изомер, L–офлоксацин) и правовращающего (D–изомер, D–офлоксацин).
Левовращающий изомер офлоксацина – L–офлоксацин в настоящее время известен, как левофлоксацин (ЛФ). Препарат был разработан в конце 1980–х годов в Японии и был предложен для применения после многоцентровых клинических испытаний, проведенных в Европе, Америке, странах Азии [8]. В России левофлоксацин зарегистрирован и разрешен для применения в 2000 г. под торговым названием Таваник (оральная и парентеральная формы).
Левофлоксацин в 8–128 раз активнее, чем D–офлоксацин. В химической структуре ЛФ существенную роль играют две основные группы: 4–метил–пиперазинильная, обусловливающая усиление всасывания при приеме препарата внутрь, повышение его активности в отношении грамотрицательных бактерий, удлинение периода полувыведения, и оксазиновое кольцо, обусловливающее расширение спектра активности в отношении грамположительных бактерий, а также удлинение периода полувыведения. Левофлоксацин характеризуется в 2 раза большей активностью, чем офлоксацин, и, следовательно, не уступает в активности ципрофлоксацину.
Левофлоксацин обладает уникальной, почти 100% биоэквивалентностью при оральном применении. Фармакокинетический профиль ЛФ аналогичен таковому у офлоксацина. Период полувыведения составляет 4–8 часов, то есть больше, чем у ципрофлоксацина, Тmax – 1,5 часа (как у ципрофлоксацина и офлоксацина), Сmax – 5,1 мг/л (то есть в 4 раза больше, чем у ципрофлоксацина), что практически соответствует Сmax при парентеральном введении в эквивалентной дозе. Левофлоксацин почти в 10 раз лучше растворяется, чем офлоксацин [6].
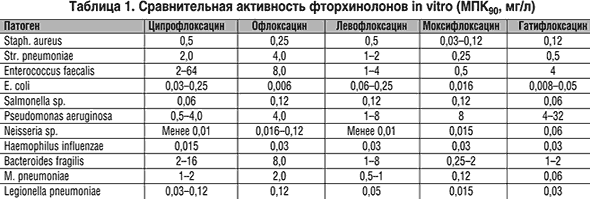
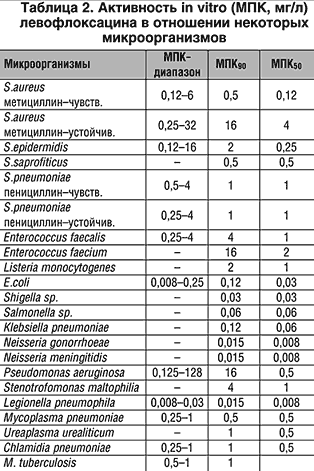
Левофлоксацин, как и другие ФХ, обладает бактерицидным типом действия и широким антимикробным спектром. ФХ активны в отношении большинства энтеробактерий, грамотрицательных бацилл (гемофильной палочки, включая b –лактамазoпродуцирующие штаммы) и грамотрицательных кокков (гоннококка, менинигококка, моракселлы, включая b –лактамазопродуцирующие штаммы), а также синегнойной палочки. Ранние ФХ (ципрофлоксацин, офлоксацин) имеют некоторую активность в отношении стафилококков и еще меньшую – против стрептококков и энтерококков, в отличие от новых ФХ, включая левофлоксацин, высокоактивных в отношении золотистого стафилококка (за исключением метициллиноустойчивых штаммов), коагулазонегативных стафилококков, стрептококков, включая пневмококк (табл. 1, 2). Диапазон МПК ЛФ в отношении стафилококков составляет 0,06–64 мг/л (при МПК90 0,25–16 мг/л), в отношении пневмококков диапазон МПК составляет 0,25–0,2 мг/л. Антипневмококковая активность не зависит от степени чувствительности к пенициллину. Левофлоксацин несколько менее активен в отношении энтерококков, хотя в отношении некоторых штаммов величины МПК составляют 0,5–1 мг/л. Препарат высокоактивен в отношении Listeria monocitogenes, Сorinеbacterium diphtheriae. Внутриклеточные возбудители (хламидии, микоплазмы, легионеллы) восприимчивы ко всем ФХ. Некоторые новые ФХ активны в отношении анаэробов, ЛФ – частично [13–18]. Особый интерес представляет активность ЛФ в отношении микобактерий. Изучается активность ЛФ в отношении риккетсий, бартонелл и некоторых других микроорганизмов [19].
В прошлом десятилетии в США была отмечена резистентность к фторхинолонам следующих патогенов: MRSA, энтерококки, Pseudomonas sp. В последующие годы докладывалось о росте резистентности сальмонелл, шигелл, Acinetobacter sp., Campilоbacter sp. и гонококка. Селекция штаммов золотистого стафилококка, устойчивых к ЛФ, наблюдается значительно реже, чем к ципрофлоксацину [1, 25–28]. Известны данные резистентности пневмококков к ФХ. Один из наиболее низких уровней устойчивости пневмококка отмечен к ЛФ (в целом 0,5% в 1997–2000 гг. в США и Канаде). Формирование резистентности к левофлоксацину возможно, однако в настоящее время устойчивость к препарату развивается наиболее медленно и не является перекрестной с другими антибиотиками [12].
В прошлом десятилетии в США была отмечена резистентность к фторхинолонам следующих патогенов: MRSA, энтерококки, В последующие годы докладывалось о росте резистентности сальмонелл, шигелл, и гонококка. Селекция штаммов золотистого стафилококка, устойчивых к ЛФ, наблюдается значительно реже, чем к ципрофлоксацину [1, 25–28]. Известны данные резистентности пневмококков к ФХ. Один из наиболее низких уровней устойчивости пневмококка отмечен к ЛФ (в целом 0,5% в 1997–2000 гг. в США и Канаде). Формирование резистентности к левофлоксацину возможно, однако в настоящее время [12].
Левофлоксацин имеет некоторые фармакокинетические преимущества перед другими ФХ. Это определяется устойчивостью молекулы к трансформации и метаболизму в организме больного. Левофлоксацин, как и ципрофлоксацин, гатифлоксацин, тровафлоксацин и офлоксацин, существует в оральной и в парентеральной формах и может использоваться при ступенчатой терапии, в отличие от других ФХ, доступных лишь в оральной форме.
Длительный Т1/2 позволяет назначать ЛФ один раз в день, что повышает комплаентность пациентов [18]. Оральная биодоступность ЛФ достигает 100% и не зависит от приема пищи, что также делает его удобным для применения. Выведение большинства ФХ происходит двойным путем (через почки и печень) [47]. В противоположность им ЛФ выводится преимущественно через почки (90%), что требует коррекции его дозы при тяжелой почечной недостаточности. Однако отсутствие метаболизма ферментами системы цитохрома р450 обусловливают отсутствие взаимодействия с варфарином и теофиллином и других значимых лекарственных взаимодействий [41]. В клинико–фармакологическом исследовании взаимного влияния при одновременном назначении ЛФ с нестероидными противовоспалительными, антидиабетическими, антиаритмическими средствами I и III класса, теофиллином, варфарином, циклоспорином и циметидином не отмечено (Simpson I., 1999).
Левофлоксацин подвергается метаболизму всего на 5%. Около 35% ЛФ связывается с белками сыворотки крови, и поэтому препарат хорошо распределяется в тканях [29]. Следует подчеркнуть, что ФХ, включая ЛФ, отлично проникают в различные ткани, создавая высокие концентрации в почках, простате, женских половых органах, желчи, органах ЖКТ, бронхиальном секрете [9], альвеолярных макрофагах, легочной паренхиме, костях, а также в цереброспинальной жидкости, поэтому эти препараты могут широко применяться при инфекциях практически любой локализации. Кроме того, хорошее внутриклеточное проникновение обеспечивает их активность в отношении атипичных патогенов.
Клиническая эффективность ЛФ при однократном назначении 250–500 мг/сут – существенное достоинство препарата, однако при генерализованных инфекционных процессах, протекающих в тяжелой форме, ЛФ назначается дважды [10–11].
Побочные эффекты и переносимость
Побочные эффекты левофлоксацина и других ФХ известны по данным европейских и других международных исследований. В Европе исследованию подверглись более чем 5000 пациентов, в мире во время испытаний было проведено приблизительно 130 млн. назначений ЛФ.
Левофлоксацин проявил себя, как наиболее безопасный ФХ с низким уровнем гепатотоксичности (1/650000). Левофлоксацин, наряду с офлоксацином и моксифлоксацином, более безопасен в отношении патологического влияния на ЦНС. Кардиоваскулярное негативное воздействие ЛФ наблюдалось значительно реже, чем при использовании других ФХ (1/15 млн. назначений, у спарфлоксацина – в 1–3% случаев). Диарея, тошнота и рвота – наиболее частые побочные эффекты, связанные с ЛФ, однако они встречаются гораздо реже, чем у других ФХ. Частота побочных эффектов ЛФ и других ФХ представлена в табл. 3 [43–44].
Показано, что увеличение дозы ЛФ до 1000 мг/сут не приводит к росту числа побочных эффектов, а их вероятность не зависит от возраста пациента [42].
В целом уровень побочных реакций, связанных с ЛФ, наиболее низкий среди ФХ, а переносимость ЛФ может быть расценена, как очень хорошая [48].
Левофлоксацин при инфекциях нижних дыхательных путей
Внебольничная пневмония – одно из наиболее распространенных заболеваний с серьезным прогнозом. Заболеваемость пневмонией в Европе колеблется от 2 до 15 случаев на 1000 человек в год. По данным А.Г. Чучалина, распространенность пневмоний среди взрослого населения России составляет 5–8 на 1000 человек [52]. В США ежегодно регистрируется 2–3 млн. случаев внебольничной пневмонии, по поводу которых совершается около 10 млн. врачебных визитов в год [49]. По данным ЦНИИОИЗ МЗ РФ, ежегодно в России переносят пневмонию более 1,5 млн. взрослых.
Общая летальность при пневмонии составляет около 20–30 случаев на 100 тыс. человек в год. Смертность среди амбулаторных больных с низкой степенью риска не более 1%, а у больных, госпитализированных с пневмонией – до 14% (у критических больных до 30–40%) (Fine et al. 1999).
Пневмококк остается наиболее частым возбудителем внебольничных пневмоний – 30,5% (20–60%). В молодых и средних возрастных группах часто встречаются Mycoplasma pneumoniae (5–50%) и Chlamydia pneumoniae (5–15%). В старших возрастных группах эти возбудители встречаются реже (1–3%). Легионелла – редкий возбудитель пневмонии (4,8%), однако она вызывает до 10% случаев тяжелых пневмоний. Легионеллезная пневмония занимает второе место по летальности после пневмококковой. H. influenzae чаще вызывает пневмонию у курильщиков или на фоне хронического бронхита (3–10%) и, по некоторым данным, в России занимает второе место в этиологии тяжелых пневмоний. Представители семейства Enterobacteriaceae (E.coli, K.pneumoniae) встречаются у пациентов с факторами риска (сахарный диабет, недостаточность кровообращения и др.) в 3–10% случаев. Moraxella сatarrhalis выделяется в 0,5% случаев Сравнительно редко выделяют Str. pyogenes, Chl. psittaci, Coxiella burnetii и др. При тяжелой пневмонии относительно большую долю среди бактериальных агентов занимает золотистый стафилококк, вероятность его обнаружения возрастает с возрастом или после перенесенного гриппа (3–10%), при этом уровень летальности может достигать 50%. В 50% случаев выделить возбудитель не удается, а в 2–5% случаев выявляется микст–инфекция.
На протяжении последних лет во всем мире наблюдается стремительный рост резистентности возбудителей пневмонии к антибактериальным препаратам [1–3, 12]. Значительно увеличилась доля пневмоний, вызываемых штаммами пневмококка, устойчивыми к пенициллину (до 51,4%) и цефалоспоринам, а также к макролидам (к эритромицину до 45,9%), тетрациклинам и ко–тримоксазолу. При этом в некоторых регионах резистентность к макролидам превалирует над устойчивостью к пенициллину. В некоторых странах частота устойчивости пневмококков к пенициллину может достигать 60%. Масштабных исследований резистентности пневмококков к пенициллину в нашей стране не проводилось. По данным локальных исследований в Москве, частота устойчивых штаммов составляет 2%, штаммов с промежуточной чувствительностью – около 20%. Устойчивость пневмококков к пенициллину связана не с продукцией b –лактамаз, а с модификацией мишени антибиотика в микробной клетке – пенициллин–связывающих белков, поэтому ингибитор–защищенные пенициллины в отношении этих пневмококков также неактивны. Устойчивость пневмококков к пенициллину обычно cопровождается устойчивостью к цефалоспоринам I–II поколений, макролидам, тетрациклинам, ко–тримоксазолу.
Проблема устойчивости пневмококка к антибиотикам в России пока не столь актуальна, как на Западе, однако следует помнить, что резистентность штаммов варьирует в каждом регионе. Факторами риска для развития резистентности являются пожилой и детский возраст, сопутствующие заболевания, предшествующая антибиотикотерапия, пребывание в домах ухода.
Резистентность гемофильной палочки к пенициллинам достигает 10%, растет ее резистентность к новым макролидам.
Антибактериальная терапия пневмоний, в подавляющем большинстве случаев эмпирическая, требует применения препаратов с широким спектром действия. При выборе способа лечения учитывают степень тяжести заболевания и факторы риска. Эмпирическая терапия всегда должна охватывать пневмококк, необходимо рассматривать применение антибиотиков, активных в отношении микоплазмы и легионеллы, во время эпидемии гриппа – S. aureus, а у пожилых больных – Enterobacteriaceae. Общепринято при тяжелой внебольничной пневмонии начинать лечение комбинацией антибиотиков, состоящей из макролида и средства, активного в отношении грамотрицательных энтеробактерий, например цефалоспорина. Кроме того, современные руководства рекомендуют применять новейшие ФХ для лечения внебольничных пневмоний, требующих госпитализации.
Фторхинолоны обладают широким спектром антимикробной активности. Эти препараты проявляют природную активность в отношении практически всех потенциальных возбудителей внебольничной пневмонии. Однако применение ранних ФХ (ципрофлоксацин, офлоксацин, пефлоксацин) при внебольничной пневмонии было ограничено из–за их слабой природной активности в отношении основного возбудителя пневмонии – S. pneumoniae. Значения минимальных подавляющих концентраций (МПК) ранних ФХ в отношении пневмококка составляют от 4 до 8 мкг/мл, а их концентрация в бронхолегочной ткани значительно ниже, что недостаточно для успешной терапии. Описаны случаи, когда терапия ФХ при пневмококковой пневмонии не приносила успеха. По другим данным, возможно создание высокой тканевой концентрации этих препаратов, достаточной для адекватной противопневмококковой активности. Это подтверждается клинико–бактериологической эффективностью ципрофлоксацина при лечении пневмоний и других инфекций нижних дыхательных путей, не уступающей стандартной терапии b –лактамными антибиотиками. Доказанная эффективность ФХ при инфекции нижних дыхательных путей позволяет определить их место при лечении внебольничной пневмонии. У больных моложе 65 лет, не курящих, без серьезных хронических заболеваний возбудителем внебольничной пневмонии в 80% случаев является пневмококк и другие стрептококки, реже атипичные микроорганизмы. Фторхинолоны у этой категории больных являются альтернативой для лечения среднетяжелой и тяжелой пневмонии, например, при аллергии на пенициллины. У больных старше 65 лет, злостных курильщиков, страдающих серьезными хроническими соматическими заболеваниями, алкоголизмом возбудителями пневмонии являются преимущественно грамотрицательные патогены, а именно H. influenzae, M. сatarrhalis, Klebsiella spp., в трети случаев пневмококк, часто атипичные патогены. Фторхинолоны являются препаратами выбора у данной категории больных, особенно при амбулаторном лечении, поскольку могут назначаться в оральной форме при среднетяжелом течении заболевании с однократным приемом в сутки, что повышает комплаентность пожилых пациентов [45]. При лечении пневмоний, требующих госпитализации, преимуществом ФХ является возможность использования ступенчатой терапии, что существенно улучшает фармакоэкономические аспекты лечения [13, 16].
На фоне роста устойчивости ключевых возбудителей респираторных инфекций к антибиотикам (в частности, распространение штаммов S.pneumoniae, резистентных к пенициллину и макролидам) особое положение приобретают новые или так называемые респираторные фторхинолоны (левофлоксацин, моксифлоксацин, гатифлоксацин). Новые ФХ обладают повышенной, в сравнении с классическими фторхинолонами (офлоксацином, ципрофлоксацином), активностью в отношении S.pneumoniae. Необходимо также подчеркнуть, что высокая антипневмококковая активность новых ФХ наблюдается независимо от чувствительности пневмококка к пенициллину и/или к макролидам [13]. Так же очевидно превосходство новых ФХ и в отношении атипичных возбудителей (M.pneumoniae, C. pneumoniae, L.pneumophila). И, наконец, эти антибиотики «унаследовали» высокую активность классических ФХ против H.influenzae и M.catarrhalis. Не вызывает сомнений, что новые ФХ являются приемлемой альтернативой макролидам, амоксициллину/клавуланату и пероральным цефалоспоринам в лечении внебольничной пневмонии. К очевидным достоинствам новых ФХ следует добавить возможность приема один раз в сутки и использование их в рамках ступенчатой терапии [16].
В проведенных к настоящему времени исследованиях, включавших в т.ч. и больных с тяжелым и (или) прогностически неблагоприятным течением заболевания, были получены убедительные свидетельства превосходящей или, по меньшей мере, сопоставимой клинической и микробиологической эффективности монотерапии ЛФ по сравнению с традиционным комбинированным лечением (цефалоспорины + макролиды). Это обстоятельство, а также прекрасный профиль безопасности, подтвержденный многолетней практикой широкого клинического применения, и очевидные экономические преимущества монотерапии объясняют присутствие ЛФ в современных схемах лечения внебольничной пневмонии. Левофлоксацин занимает видное место в современных схемах лечения взрослых пациентов с внебольничной пневмонией, не подлежащих госпитализации (Frias J., 1998; Bartlett J.G., 2000), а также в условиях стационара (Frias J., 2000; Mandell L.A., 1997)
При внебольничной пневмонии клиническая эффективность ЛФ превосходила эффективность терапии цефтриаксоном, цефуроксимом (в т.ч. в сочетании с эритромицином или доксициклином) и составила 96 и 90%, бактериологическая эффективность – 98 и 85% соответственно; различия были статистически достоверны (File T.M.,1997).
По данным I. Нarding (2001), левофлоксацин был более эффективным при лечении внегоспитальной пневмонии, чем кларитромицин, бензилпенициллин, цефтриаксон, амоксициллин/клавулановая кислота.
В ходе рандомизированного, двойного слепого, мультицентрового исследования у 518 больных внебольничной пневмонией проводился сравнительный анализ клинической эффективности применения ЛФ и амоксициллина/клавуланата. Клиническая эффективность при приеме 500 мг ЛФ 1 раз в сутки составила 95,2%, при приеме ЛФ по 500 мг 2 раза в сутки – 93,8%, а при приеме амоксициллина/клавуланата по 625 мг 3 раза в сутки – 95,3% [55].
В многоцентровом открытом рандомизированном исследовании сравнивалась эффективность ЛФ и цефтриаксона в комбинации с эритромицином у больных внебольничной пневмонией с высоким риском неблагоприятного исхода. 132 больным, получавшим ЛФ, препарат изначально вводился внутривенно (500 мг 1 раз в сутки), затем перорально в той же дозе в течение 7–14 дней. В группе сравнения 137 пациентов получали внутривенно или внутримышечно цефтриаксон (1–2 г 1 раз в сутки) и внутривенно эритромицин (500 мг 4 раза в сутки) с последующим переходом на пероральный прием амоксицилина/клавуланата (875 мг 2 раза в сутки) совместно с кларитромицином (500 мг 2 раза в сутки). Клиническая эффективность в 1 группе была 89,5%, во 2 группе – 83,1%. Таким образом, монотерапия ЛФ не уступает по эффективности традиционному комбинированному лечению у больных с высокой вероятностью летального исхода.
В ходе другого мультицентрового рандомизированного исследования [14] у 456 больных внебольничной пневмонией (1 группа – 226 пациентов получали левофлоксацин, 2 группа 230 пациентов получали цефтриаксон и/или цефуроксим аксетил) была изучена клиническая и микробиологическая эффективность ЛФ, вводимого внутривенно (500 мг 1 раз в сутки) и/или перорально (500 мг 1 раз в сутки), в сравнении с цефтриаксоном, вводимым внутривенно (1,0–2,0 г 1–2 раза в сутки) и/или цефуроксимом аксетилом, вводимым перорально (500 мг 2 раза в сутки). Помимо этого, исходя из конкретной клинической ситуации, 22% больных второй группы назначался эритромицин перорально (1 г 4 раза в сутки). Клиническая и микробиологическая эффективность монотерапии ЛФ оказалась достоверно выше традиционной схемы лечения. Так клинический успех у пациентов 1 группы составил 96%, у пациентов 2 группы – 90%, а частота эрадикации возбудителя у микробиологически обследованных пациентов – 98% и 85%, соответственно.
Роль и место ЛФ в рамках ступенчатой терапии внебольничной пневмонии в сравнении с традиционной терапией были изучены в рамках масштабного канадского исследования (CAPITAL Study), включавшего 1743 больных [56]. Для решения вопроса о месте лечения и способе введения лекарственного средства использовалась шкала M.J. Fine et al., 1997. Если итоговая оценка пациента не превышала 90 баллов, то лечение проводилось в домашних условиях с назначением ЛФ (500 мг 1 раз/сутки, внутрь) в течение 10 дней. Если же итоговая оценка составляла 91 и более баллов, то больного госпитализировали и первоначально ЛФ (500 мг 1 раз/сут) вводили внутривенно. По достижении стабильного состояния (способность проглатывать пищу, отрицательные результаты посевов крови, температура тела 38,0°C, частота дыхания b –лактамными антибиотиками, а также кларитромицином. В данном исследовании проводилось определение чувствительности к исследуемым антибиотикам с использованием МПК и был выявлен высокий уровень резистентности основных возбудителей пневмонии (пневмококка, гемофильной палочки, моракселлы) к b –лактамам, рост резистентности атипичных патогенов к макролидам и, в противоположность этому, низкий уровень резистентности к ЛФ. Частые случаи возникновения аллергических реакций на b –лактамы в сравнении с ЛФ и хорошая переносимость последнего также показали его преимущество. Во втором исследовании рассматривался вопрос об оптимальной антибактериальной терапии при внебольничной пневмонии у пациентов с различными сопутствующими состояниями (ХНЗЛ, диабет, хроническая сердечная недостаточность, алкоголизм, нахождение в домах престарелых, работа на животноводческих фермах и т.д.). В результате среди всех ФХ для ведения внебольничной пневмонии был рекомендован только левофлоксацин.
В следующем исследовании изучалась замена левофлоксацином других ФХ при пневмонии и инфекциях другой локализации. Производилось микробиологическое исследование, клиническая и фармакоэкономическая оценки. В результате замена более дорогим препаратом (левофлоксацином) более дешевых (офлоксацина, ципрофлоксацина) оказалась более выгодной.
Хронический бронхит в фазе обострения
Согласно результатам исследования C.A. DeAbate (1997), клиническая и бактериологическая эффективность ЛФ при приеме в дозе 500 мг 1 раз в сутки в течение 5–7 дней сопоставима с 7–10–дневным приемом цефуроксима в дозе 250 мг 2 раза в сутки. Клиническая эффективность составила 94,5 и 92,6%, бактериологическая – 97,4 и 92,6%, соответственно.
Согласно данным M.P. Habib (1998), клиническая и бактериологическая эффективность однократного приема 500 мг ЛФ в течение 5–7 дней сопоставима с 7–10–дневным приемом цефаклора в дозе 250 мг 3 раза в сутки. Клиническая эффективность составила 91,6 и 85%, бактериологическая – 94,2 и 86,5%, соответственно [21].
В этиологии нозокомиальной пневмонии преобладает грамотрицательная флора (Klebsiella sp., P. mirabilis, E. coli, H. influensae, P. aeruginosa). Из грамположительной флоры встречаются S. aureus, реже пневмококки, часто полирезистентные штаммы. Фторхинолоны давно успешно используются при лечении данной патологии. Учитывая антимикробный спектр ЛФ, назначение его при нозокомиальной пневмонии может быть вполне оправдано. Однако при предполагаемой или при подтвержденной инфекции P. аeruginosa требуется комбинированная антибактериальная терапия обычно с антисинегнойными b –лактамными антибиотиками для предупреждения развития резистентности.
Опыт применения левофлоксацина убедительно доказывает, что это высокоэффективный препарат, сопоставимый по степени эффективности с другими новыми фторхинолонами. Практически в равной степени левофлоксацин эффективен в отношении как грамположительной, так и грамотрицательной аэробной флоры, а также обладает высокой активностью в отношении атипичных возбудителей. Левофлоксацин имеет практически идеальные фармакокинетические параметры и две лекарственные формы, оральную и парентеральную, что позволяет максимально оптимизировать дозы и схемы терапии и применять его в рамках супенчатой терапии. Высокая бактерицидная активность левофлоксацина в сочетании с высокими значениями максимальных концентраций, хорошим проникновением в ткани, показателями AUC обеспечивает максимальный терапевтический эффект.
Среди других препаратов группы ФХ левофлоксацин обладает наилучшей переносимостью с низким уровнем побочных эффектов.
В настоящее время левофлоксацин с успехом применяется в основном при инфекциях нижних дыхательных путей. Однако, учитывая широкий антимикробный спектр, оптимальные фармакокинетические параметры, хорошую переносимость, левофлоксацин может применяться при инфекциях практически любой локализации (синуситы, инфекции мочевыводящих путей, кожи и мягких тканей, малого таза, интраабдоминальные инфекции, тяжелые генерализованные инфекции, кишечные инфекции, инфекции, передающиеся половым путем, и др.).
Формирование резистентности к левофлоксацину возможно, однако в настоящее время устойчивость к препарату развивается наиболее медленно и не является перекрестной с другими антибиотиками.
Наряду с высокой клинической эффективностью левофлоксацин несомненно обладает фармакоэкономическими преимуществами, что актуально в условиях современной системы здравоохранения.
1. Tenover FC, Hughes JM. The challenges of emerging infectious diseases: Development and spread of multiple–resistans bacterial pathogens. JAMA 1996;275:300–304.
2. Report pf the ASM Task Force on Antibiotic Resistance. American society for microbiology. Antimicrob agent chemother 1995; 39(sappl); 2–23.
3. Rockefeller University Workshop. Special Report. Multiple–resistans bacterial pathogens. N Engl J Med 1994;330:1247–1251.
4. Bartlett JG, Breiman RF, Mandell LA, File TM Jr. Guidelines from the infections Diseases Sosiety of America. Community– acquired pneumonia in adults: guidelines for management. Clin infect Dis 1998;;811–838.
5. Niederman MS, Bass JB Jr, Campbell GD, et al. Guidelines for the initial management of adults with community– acquired pneumonia: Diagnosis, assessment of severity, initial antimicrobial therapy.; 1993;14181426.
6. Davis R, Bryson HM, Levofloxacin: a review of its antibacterial activity, farmacokinetics and therapeutic efficasy. Drags 1994;47;677–700.
7. Cunha BA, Community– acquired pneumonia cost–effective antimicrobial therapy. Postgrad Med 1996;99:109–122.
8. Hayakawa Y, Furuhama K, Takayama S, Osada Y, Levofloxacin a new quinolone antibacterial agent. Arzneim Forsch Drag Res 1992;42:363–364.
9. Nacamori Y, Miyashita Y, Nacatu K, Levofloxacin; Penetration into sputum and once–daily treatment of respiratory tract infection. Drags 1995;49(sappl 2):418–419.
10. Shishido H, Furukawa K, Nagai H, Kawakami K, Kono H, Oral levofloxacin 500mg and 300mg daily doses in difficult–to–treat respiratory infections. Drags 1995;49(sappl 2):433–435.
11. Kawai T, Clinical evaluation of levofloxacin 200mg 3 times daily in the treatment of bacterial lower respiratory tract infections. Drags 1995(sappl 2):416–417.
12. Klugman KP, Capper T, Levofloxacin in vitro activity and sinergistic activity in combination with other antibacterials against antibioticresistans S. Pneumonia, and selections of resistans mutants. 1995:87.
13. Marcus A, Isert D, Klesel N, Selbert C Killing activity of levofloxacin and ciprofloxacin against S. pneumonia in vitro and vivo. 1995:90.
14. File TM, Segreti J, Dunbar L et al. A multicenter, randomized study comparing the efficacy and safety IV and/or oral levofloxacin versus ceftriaxon and/or cafuroxim axetil in treatment of adults with community– acquired pneumonia. Antimicrob Agent Chemother 1997;41:1965–1972.
15. Sydnor TA, Scheld WM, Gwaltney JM. A noncomparative study to evaluate the safety and efficasy of levofloxacin in the treatment of acute bacterial sinusitis in adults. 1995.
16. File TM Fluoroquinolones and respiratory tract infections. Infect Dis Clin Pract. 19979Sappl 2):559–566.
17. Chein SC, Rogge MC, Gisclon LG, et al. Pharmokinetic profil of levofloxacin following once–daily 500mg oral or IV doses. Antimicrob Agent Chemother 1997;47:2256–2260.
18. Niederman MS, McCombs JS, Unger AN, et al. The cost of treating community– acquired pneumonia. Clin Ther. 1998;20:820–837.
19. Isaacson DM, Fernandes JA, Frosco M et al. Levofloxacin: a review of its antibacterial activity. 1996;1:391–439.
20. Cooper I, Isbell DJ, Kruszinsky JA et al. Comparative in vitro activity of L–ofloxacin and FK037 to other agents against 10,040 fresh clinical isolates. Int J Antimicrob Agents. 1996;6:201–211.
21. DeAbate CA, Russel M, McElvaine P et al. Safety and efficasy of levofloxacin versus cefuroxime axetil in acute bacterial exacerbation of chronic bronhitis. Respir Care.1997;42:206–13.
22. Biedenbah DJ, Jones RN. The comparative antimicrobial activity of levofloxacin tested against 350 clinical isolates streptococci. Diagn Microbiol Infect Dis. 1996;25:47–51.
23. Hazlet TK, Hu TW. Assotiation between formulary strategies and hospital drag expenditures. Am J Hosp Pharm 1992;49:2207–10.
24. Guay DRP, Sequential antimicrobial therapy; a realistic approach to cost conteinment? Pharmacoeconomics 1993;3:341–4.
25. Acar JF, Goldstain FW. Trends in bacterial resistense to fluoroquinolones. Clin Infect Dis1997;24:567–73.
26. Segreti J, Goots TD, Goodman LJ et al. High–level quinolone resistense in clinical isolates of Campilobacter jejuni. J Infect Dis 1992;165:667–70.
27. Smith SM, Eng RHK, Bais P, Fan–Haward P, Texon–Tuman F. Epidemiology of ciprofloxacin resistence among patient with meticillin–resistant S. aureus. J Antimicrob Chemother 1990;26:567–72.
28. Selman LJ, Mayfield DC, Thornsberry C et al. Risc factors associated with antimicrobial resistance among Str. Pneumonia in the USA.2000.
30. Gwailtneiy JM Jr Acute community–asqued sinusitis. Clin Infect Dis 1996;23:1209–25.
31. Bartlett JG, Dowell SF, Mandell LA, File TM Jr, Musher DM, Fine AM. Practice guidelines for the management of community–asqued pneumonia in adults. Clin Infect Dis 2000; 31:1209–25
32. Grossman RF. The role of the fluoriquinolones in respiratory infections. J Antimicrob Chemother 1997;40(sapplA):59062
33. Hooton TM, Stamm WE. Diagnosis and treatment of uncomlicated urinary tract infetions. Infect Dis Clin North Am 1997;11:551–81.
34. Bergeron MG. Treatment of pyelonephritit in adults. Med Clin North AM 1995;79:619–49.
35. Nickel JC. Practical approach to the management of prostatitis. Techniques Urol 1995;1:162–7.
36. Karchmer AW. Use of quinolones in skin and skin structure and other infections. 2000.
37. Ortho–McNeil Pharmaceutical. Levofloxacin tablets–injection package insert. Raritan, NJ;2000.
38. Hamer DH, Gorbach SL. Use of the quinolones for treatment and prophilaxis of bacterial gastrointestinal infections. In Andriole VT, ed. The quinolones 3rd ed. San Diego: Academic Press, 2000:303–23.
39. Weigelt J, Brasel K, Faro S. Use of quinolones in surgery and obstetrics and genicology. JN: Andriole VT, ed. The quinolones, 3rd ed. San Diego:Academic Press, 2000:285–301.
40. Levison ME, Bush LM. Peritonitis and other intra–abdominal infections.1995.
41. Guay DRP. Implications of quinolones pharmacocinetic drag interactions. Hosp Pharm 1997; 32:677–90.
42. Fish DN. Fluoroquinolones adverse effects and drag interactions. Pharmacotherapy 2002;21(10pt2);2535–72.
43. Lipsky BA, Baker CA. Fluoroquinolones toxiticy prophil; a review focusing on newer agents. Clin Infect Dis 1999;28:352–64.
44. Jones RN, Pfaller MA. Bacterial resistance: a worldwide problem. Diagn Microbiol Infect Dis 1998;31:379–88.
45. Guay DRP. Quinolones. Antimicrobial therapy in the elderly patient. New York/ 1994: 237–310.
46. Падейская Е. Н., Яковлев В.П. Антимикробные препараты группы фторхинолонов в клинической практике. М.: Логата, 1998.–351с.
47. Яковлев В.П., Литовченко К.В. Левофлоксацин–новый препарат группы фторхинолонов.// Инфекция и антимикробная терапия, 2001; 3 (5): 132–140.
48. Экономическая оценка эффективности лекарственной терапии (фармакоэкономический анализ). Под ред. проф. Воробьева П.А.// Ньюдиамед, М. – 2000.
49. Навашин С.М., Чучалин А.Г., Белоусов Ю.Б. и др. Антибактериальная терапия пневмоний у взрослых. Учебно–методическое пособие для врачей. М. – 1998.
50. Синопальников А.И., Дуганов В.К. Левофлоксацин: ступенчатая терапия внебольничной пневмонии у взрослых // Русский медицинский журнал. 2001. № 15. с. 3–10.
51. Стандарты (протоколы) диагностики и лечения больных с неспецифическими заболеваниями легких (Приложение к приказу № 300 Минздрава России). М. 1999. Универсум Паблишинг. 47 с.
52. Чучалин А.Г. Болезни органов дыхания. Медицинская газета. – 2000. № 43. С. 8–9.
53. Яковлев С.В. Новое поколение фторхинолонов – новые возможности лечения внебольничных инфекций дыхательных путей // Антибиотики и химиотерапия. 2001. Т. 46. № 6. С. 38–42