Левоцетиризин или дезлоратадин что лучше
Антигистаминные препараты: как сделать правильный выбор
В России распространенность аллергии, по результатам эпидемиологических исследований ГНЦ Института иммунологии, колеблется от 17,5 до 30%. Клинические формы заболеваний аллергического генеза чрезвычайно многообразны. Но, какой бы не была маска аллергии, пациент ждет от терапевта, педиатра, оториноларинголога, дерматолога или аллерголога помощи в снятии симптомов и адекватной терапии, которая улучшит его качество жизни. Современные антигистаминные препараты IIб поколения – левоцетиризин, R-энантиомер цетиризина, ‒ влияют на гистаминзависимую стадию аллергических реакций, снижают проницаемость сосудов и миграцию эозинофилов, ограничивая высвобождения медиаторов воспаления.
Аллергические заболевания в последние десятилетия стали реальной глобальной проблемой человечества. И их распространенность продолжает расти, уже не напоминая, а крича о проблемах окружающей среды и современного образа жизни людей (особенно в больших городах).
С чертами эпидемии
Распространенность аллергии сегодня действительно приобретает черты эпидемии. И это не преувеличение: по данным скрининговых эпидемиологических исследований, распространенность аллергопатологий среди взрослого населения составляет почти 30% и практически 50% – среди детей 1 (в их структуре: 20‒40% – аллергический ринит (АР), 7‒10% — бронхиальная астма (БА), различные аллергодерматозы – до 40% детского и около 10% взрослого населения 2‒4 ). То есть каждый третий
Левоцетиризин: современные аспекты применения при аллергических заболеваниях с точки зрения доказательной медицины
Разработка стратегий терапевтических вмешательств при ряде аллергических заболеваний исторически связана с выявлением роли гистамина в механизме развития главных симптомов аллергии. Существуют разные подходы к подавлению активности гистамина в организме. Так, например, кортикостероиды, циклоспорин А, пувотерапия подавляют высвобождение гистамина из тучных клеток; блокаторы гистаминовых рецепторов, антилейкотриеновые препараты, доксепин предотвращают действие гистамина на клетки-мишени.
Поиск препаратов с антигистаминным эффектом, начатый в сороковые годы XX века, продолжается до настоящего времени, и исследовательский интерес сфокусирован на полифункциональных характеристиках препаратов нового поколения, которые объединяют в себе антигистаминную, противоаллергическую и противовоспалительную активность.
Гистамин обладает широким спектром биологической активности и действует через активацию клеточных поверхностных рецепторов, сопряженных с G-белками (GPCR, от англ. — G-protein coupled receptor). Эти молекулярные структуры организованы в виде извивающегося наподобие серпантинной ленты белка, семь раз пересекающего клеточную мембрану. Наружная часть ленты служит «антенной», улавливающей химические сигналы, которые поступают к клетке, а внутренняя — запускает клеточный ответ, начинающийся с активации G-белка. В отличие от остальных видов поверхностных клеточных рецепторов GPCR универсален. С ними связываются и нейромедиаторы, всего в несколько раз превосходящие по массе атом углерода, и более крупные белки.
GPCR участвуют почти во всех жизненно важных процессах, протекающих в организме. Лекарственные вещества, мишенью которых являются GPCR, либо связываются с активным центром, имитируя действие сигнальной молекулы, либо блокируют активный центр, преграждая доступ к нему этой молекулы.
Из всех известных в настоящее время четырех типов рецепторов гистамина (Н1-, Н2-, Н3-, Н4-рецепторы), принадлежащих к группе GPCR, особый интерес для аллергологии представляют Н1-рецепторы. Именно Н1-рецепторы, преобладающие в коже и на гладкомышечных клетках, ответственны за развитие ранней и поздней (отсроченной) фазы аллергического ответа.
Расшифровка механизмов взаимодействия лекарств с гистаминовыми рецепторами позволила уточнить терминологические формулировки в отношении антигистаминных препаратов и обозначить их как «обратные агонисты». Обратные агонисты Н1-гистаминовых рецепторов являются патогенетически оправданными средствами для лечения большинства аллергических заболеваний.
В настоящем обзоре, посвященном левоцетиризину, будут использоваться привычные термины («антагонист Н1-гистаминорецепторов») наряду с современным толкованием препарата как «обратного агониста».
Большинство Н1-антигистаминных препаратов представляют собой вещества, осуществляющие основное фармакологическое действие за счет активных метаболитов, образующихся после серии трансформаций исходного лекарственного препарата. Безусловным преимуществом в связи с этим обладают новые средства, полученные на основе фармакологически активных метаболитов: весь лекарственный препарат в этом случае является действующим началом, лишенным многих побочных эффектов своего предшественника [1].
Первым антигистаминным препаратом второго поколения (ко второму поколению относятся все неседативные антигистамины), крайне незначительно подвергающимся метаболизму, был цетиризин. Препарат с доказанной эффективностью и безопасностью, он в настоящее время широко используется для лечения и профилактики аллергических заболеваний у взрослых и детей [2]. С 2005 года на фармацевтическом рынке России присутствует левовращающий оптический изомер цетиризина, селективный обратный агонист Н1-рецепторов — левоцетиризин (Ксизал) в таблетированной форме, а с 2008 года — в виде капель.
Фармакодинамика и фармакокинетика левоцетиризина достаточно хорошо изучены [3, 4].
Левоцетиризин быстро всасывается в кишечнике, достигая максимальной концентрации в плазме через 0,5–1 час после приема. Биодоступность препарата близка к 100% — это значит, что препарат почти полностью попадает в системный кровоток (около 100% относительно исходной дозы препарата). Из кишечника левоцетиризин транпортируется в печень, а оттуда поступает в кровоток. Т. к. левоцетиризин — это конечный метаболит, он не проходит печеночный метаболизм, чтобы стать активным. Левоцетиризин не взаимодействует с цитохромом печени P450, поэтому у него нет конкурентного лекарственного взаимодействия. Это дает возможность сочетать его с антибиотиками, противогрибковыми и другими препаратами и применять у пациентов с патологией печени. Левоцетиризин не обладает кардиотоксическим действием.
В связи с низким объемом распределения (0,4 л/кг), препарат обнаруживается в тканях только там, где это необходимо, а именно на клеточной мембране, и не проникает внутрь клетки. Левоцетиризин выводится с мочой в неизменном виде на 86% и фекалиями — 13%. Перечисленные параметры свидетельствуют об оптимальном фармакокинетическом профиле левоцетиризина [5, 6].
Селективность
Отличительным свойством антигистаминовых препаратов второго поколения является сродство к гистаминовым рецепторам и избирательность подавления их активности. При аллергической реакции через Н1-гистаминовые рецепторы реализуются такие патофизиологические и клинические эффекты, как зуд, вазодилятация, экссудация, эритема, гиперемия, стимуляция кашлевых рецепторов и вагусных афферентных волокон, секреция гистамина, экспрессия молекул межклеточной адгезии, а через Н4-рецепторы –зуд, продукция цитокинов, эйкозаноидов, хемотаксис лейкоцитов и дендритных клеток [6].
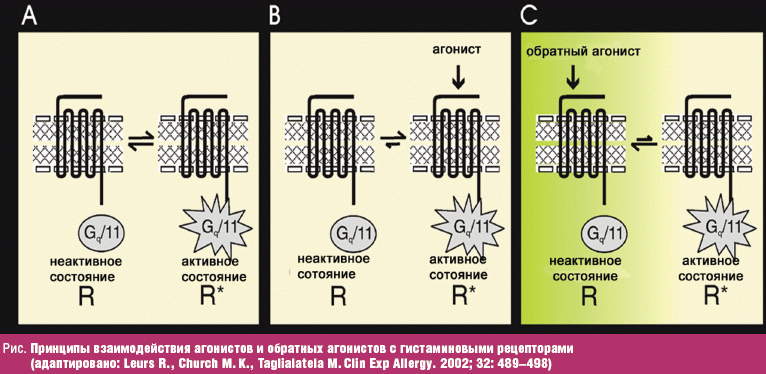
Н1-рецептор присутствует на клеточных мембранах в двух конформациях — активной и неактивной, между которыми в норме поддерживается равновесие (рис. A, B, C).
Рис. Принципы взаимодействия агонистов и обратных агонистов с гистаминовыми рецепторами (адаптировано: Leurs R., Church M. K., Taglialatela M. Clin Exp Allergy. 2002; 32: 489–498)
Даже при отсутствии гистамина рецептор проявляет базальную активность («конститутивная рецепторная активность» — рис., A). Гистамин, связываясь с рецептором, «закрепляет» его в форме активной конформации; активная конформация начинает преобладать над неактивной (рис., B). Все седативные и неседативные гистаминоблокаторы, являясь обратными агонистами, «закрепляют» рецептор в неактивной форме (рис., С). Поэтому они могут снижать базальную деятельность рецептора, независимо от того, повышен в данный момент выброс гистамина в межклеточное пространство или нет. В результате базальной и стимулированной гистамином активности Н1-рецептора повышается активность внутриклеточного фактора транскрипции ряда провоспалительных цитокинов и молекул адгезии (ядерного фактора NF-kB). Так, гистамин при взаимодействии с гистаминовым рецептором I типа повышает активность фактора NF-kB в 8 раз, а антигистаминные препараты снижают базальную активность фактора NF-kB и блокируют реакцию на контакт с гистамином [1, 8].
Степень смещения равновесия в сторону неактивной конформации зависит от природы обратного агониста. Чем выше сродство Н1-антигистаминных препаратов к Н1-рецептору, тем сильнее выражено их подавляющее действие на зависимое от активации NF-kB образование провоспалительных медиаторов и на клинические проявления, с ними связанные.
Еще одна важная характеристика взаимодействия обратного агониста с рецептором — это занятость рецепторов. Через 4 и 24 часа после приема левоцетиризина занятость составила 90% и 57%, для фексофенадина — 95% и 24%, для дезлоратадина — 71% и 43%. Наивысшая занятость рецепторов обеспечивает лучший терапевтический эффект [1].
Избирательность левоцетиризина в отношении Н1-гистаминовых рецепторов в два раза выше по сравнению с цетиризином, а также в 600 раз выше, чем к другим рецепторам и ионным каналам, близким по структуре (Н2-, Н3-, альфа- и бета-адренорецепторам, 5-НТ1А и 5-НТ2, дофамина D2, аденозина А1 и мускариновым рецепторам), в связи с чем его антихолинэргическое и антисеротониновое действие сводится к минимуму [7].
Выраженная способность левоцетиризина тормозить спонтанную и стимулированную гистамином активность NF-kB объясняет его угнетающее действие на секрецию медиаторов аллергического воспаления [9, 10, 11]. Этим объясняется лечебное действие — уменьшение заложенности носа, благоприятное влияние на течение бронхиальной астмы, зудящих дерматозов, крапивницы и др. [12, 13, 14].
Левоцетиризин в программах фармакотерапии аллергического ринита и конъюнктивита
Антигистаминные препараты рекомендуются в качестве лекарств первого выбора у больных аллергическим ринитом [15]. Их назначают с целью купирования эффекта гистамина, провоцирующего основные симптомы заболевания: зуд, чихание и ринорею. Проведено множество клинических испытаний антигистаминных препаратов, где отмечено их выраженное позитивное влияние на тяжесть течения ринита и качество жизни пациентов [16]. За последние несколько лет в контролируемых исследованиях левоцетиризина был подтвержден высокий терапевтический эффект и безопасность этого препарата [17, 18].
Курсы лечения у взрослых и детей, больных аллергическим ринитом, продолжались 2, 4, 8 недель и 6 месяцев. Во всех испытаниях продемонстрировано достоверное снижение интенсивности симптомов воспаления как верхних, так и нижних дыхательных путей по сравнению с группой плацебо. Курс лечения левоцетиризином кроме основного, антигистаминного эффекта, оказывал благоприятное влияние на общее состояние и самочувствие пациентов: эмоциональный статус, болевой синдром и физическую активность, которые сохранялись и после отмены препарата [19].
Клиническая эффективность левоцетиризина продемонстрирована у больных с круглогодичными и сезонными ринитами [20, 21]. В открытом многоцентровом исследовании с участием 397 врачей общей практики из Бельгии и 1290 пациентов с сезонным аллергическим ринитом (САР), которые пришли на консультацию к доктору с жалобами на неэффективность предыдущей антигистаминовой терапии или на побочные эффекты такой терапии, лечение левоцетиризином 5 мг однократно в течение 4 недель продемонстрировало преимущества назначенного лечения [22].
С появлением новой классификации ринитов (интермиттирующий и персистирующий) продолжено изучение оптимальных доз, влияние на глазные симптомы, оценку качества жизни на фоне фармакотерапии в этих группах пациентов [23, 24]. К таким исследованиям относится XPERT (Xyzal® persistent rhinitis trial), которое проводилось в 5 странах Европы: Бельгии, Франции, Германии, Италии, Испании и включало 551 пациента с персистирующим аллергическим ринитом с сенсибилизацией к пыльце трав и домашней пыли. Пациенты рандомизированы на две группы: 273 получали плацебо, 278 — левоцетиризин. Было установлено, что левоцетиризин обладает высокой клинической эффективностью, улучшает качество жизни и снижает стоимость длительного лечения персистирующего аллергического ринита [25].
Левоцетиризин в дозе 5 мг продемонстрировал высокую эффективность и безопасность при лечении пациентов с персистирующим аллергическим ринитом в отношении всех симптомов данного заболевания, включая назальные и глазные симптомы при хорошей переносимости лечения [23, 26].
Терапевтический эффект антигистаминного препарата левоцетиризина (Ксизал) у больных аллергическим персистирующим ринитом не только на назальные, но и глазные симптомы подтвержден в российском многоцентровом открытом несравнительном исследовании [27].
Левоцетиризин подавлял существенно проявления аллергии у больных с разным спектром сенсибилизации (аллергия к клещам домашней пыли, пыльце растений), а при сравнительных исследованиях с другими антигистаминами демонстрировал ряд преимуществ [28].
В двойном слепом перекрестном исследовании у 39 пациентов с аллергией к клещам домашней пыли проводили провокационный тест с аллергеном, после чего пациенты принимали 5 мг левоцетиризина, или 10 мг лоратадина, или плацебо. Существенное улучшение отмечено у 83,8% пациентов, получавших левоцетиризин, и у 66,7% получавших лоратадин [29, 30].
При контролируемом контакте пациентов с аллергеном (пыльцой луговых трав) было показано, что левоцетиризин и фексофенадин имели одинаковое время начала действия — через 1 ч после приема и оба препарата были значительно эффективнее, чем плацебо. Через 24 ч после приема препарата появлялась достоверная разница в эффективности препаратов, что говорит о большей продолжительности действия левоцетиризина по сравнению с фексофенадином [29].
При сравнении быстроты наступления и продолжительности действия левоцетиризина и дезлоратадина в двойном слепом плацебо-контролируемом исследовании 373 пациента с аллергией к пыльце амброзии получали левоцетиризин 5 мг в сутки, или дезлоратадин 5 мг в сутки, или плацебо и наблюдались в течение 2 дней контролируемого контакта с пыльцой амброзии. Самооценка симптомов проводилась каждые полчаса. Среднее время начала действия составило у дезлоратадина 3 ч, в то время как у левоцетиризина — 1 ч. Оба препарата были эффективнее, чем плацебо, а левоцетиризин эффективнее дезлоратадина для купирования симптомов аллергического риноконъюнктивита [31, 32].
Оба препарата также достоверно уменьшали заложенность носа, причем в первые сутки приема данный эффект у левоцетиризина был более выражен, чем у дезлоратадина. Через 24 ч после приема первой дозы препарата выраженность симптомов была достоверно ниже в группе левоцетиризина, что говорит о большей продолжительности действия препарата по сравнению с дезлоратадином.
Во всех исследованиях у больных с ринитами доказана безопасность использования левоцетиризина: в долгосрочном наблюдении в течение 6 месяцев не было выявлено никаких серьезных побочных и нежелательных эффектов [33]. Установлены безопасность и эффективность пероральных антигистаминных средств у детей. Их можно назначать даже маленьким детям [34].
В отличие от анализа клинической эффективности и безопасности левоцетиризина в литературе реже обсуждаются фармакоэкономические аспекты. В одном двойном слепом, плацебо-контролируемом длительном исследовании была установлена эффективность затрат на лечение левоцетиризином у больных с персистирующим аллергическим ринитом [15].
Таким образом, можно отметить, что уровень рекомендаций по использованию левоцетиризина в терапии пациентов с аллергическими ринитами можно отнести к категории А, поскольку они базируются на большом количестве рандомизированных, двойных слепых, плацебо-контролируемых клинических исследований [15, 19]. Высокая эффективность применения препарата в стандартных терапевтических дозах (5 мг однократно в сутки) установлена в разных возрастных группах, в том числе у детей дошкольного и школьного возраста, пожилых людей. Продолжительные наблюдения (в течение полугода лечения, 26 недель и более), достаточное количество пациентов (размеры выборок более 300–500 человек) показали, что длительная (годы) терапия левоцетиризином безопасна [15, 23, 25, 34].
Назальная гиперреактивность и неспецифические триггеры
Полный список литературы находится в редакции
Обзор антигистаминных средств первого и второго поколений, рациональный подход к использованию в клинической практике
Исторически сложилось так, что под термином «антигистаминные препараты» понимают средства, блокирующие Н1-гистаминовые рецепторы, а лекарства, воздействующие на Н2-гистаминовые рецепторы (циметидин, ранитидин, фамотидин и др.), называют Н2-гистаминоблокат
Исторически сложилось так, что под термином «антигистаминные препараты» понимают средства, блокирующие Н1-гистаминовые рецепторы, а лекарства, воздействующие на Н2-гистаминовые рецепторы (циметидин, ранитидин, фамотидин и др.), называют Н2-гистаминоблокаторами. Первые используются для лечения аллергических заболеваний, вторые применяются в качестве антисекреторных средств.
Гистамин, этот важнейший медиатор различных физиологических и патологических процессов в организме, был химически синтезирован в 1907 году. Впоследствии его выделили из тканей животных и человека (Windaus A., Vogt W.). Еще позднее были определены его функции: желудочная секреция, нейромедиаторная функция в ЦНС, аллергические реакции, воспаление и др. Спустя почти 20 лет, в 1936 году, были созданы первые вещества, обладающие антигистаминной активностью (Bovet D., Staub A.). И уже в 60-е годы доказана гетерогенность рецепторов в организме к гистамину и выделены три их подтипа: Н1, Н2 и Н3, различающиеся по строению, локализации и физиологическим эффектам, возникающим при их активации и блокаде. С этого времени начинается активный период синтеза и клинического тестирования разнообразных антигистаминных препаратов.
Многочисленные исследования показали что гистамин, воздействуя на рецепторы респираторной системы, глаз и кожи, вызывает характерные симптомы аллергии, а антигистаминные препараты, селективно блокирующие Н1-тип рецепторов, способны их предотвращать и купировать.
Большинство используемых антигистаминных средств обладает рядом специфических фармакологических свойств, характеризующих их как отдельную группу. Сюда относятся следующие эффекты: противозудный, противоотечный, антиспастический, антихолинергический, антисеротониновый, седативный и местноанестезирующий, а также предупреждение гистамининдуцированного бронхоспазма. Некоторые из них обусловлены не гистаминовой блокадой, а особенностями структуры.
Антигистаминные препараты блокируют действие гистамина на Н1-рецепторы по механизму конкурентного ингибирования, причем их сродство к этим рецепторам значительно ниже, чем у гистамина. Поэтому данные лекарственные средства не способны вытеснить гистамин, связанный с рецептором, они только блокируют незанятые или высвобождаемые рецепторы. Соответственно, Н1-блокаторы наиболее эффективны для предупреждения аллергических реакций немедленного типа, а в случае развившейся реакции предупреждают выброс новых порций гистамина.
По своему химическому строению большинство из них относятся к растворимым в жирах аминам, которые обладают сходной структурой. Ядро (R1) представлено ароматической и/или гетероциклической группой и связано при помощи молекулы азота, кислорода или углерода (Х) с аминогруппой. Ядро определяет выраженность антигистаминной активности и некоторые из свойств вещества. Зная его состав, можно предсказать силу препарата и его эффекты, например способность проникать через гематоэнцефалический барьер.
Существует несколько классификаций антигистаминных препаратов, хотя ни одна из них не является общепринятой. Согласно одной из наиболее популярных классификаций, антигистаминные препараты по времени создания подразделяют на препараты первого и второго поколения. Препараты первого поколения принято также называть седативными (по доминирующему побочному эффекту), в отличие от неседативных препаратов второй генерации. В настоящее время принято выделять и третье поколение: к нему относятся принципиально новые средства — активные метаболиты, обнаруживающие, помимо наивысшей антигистаминной активности, отсутствие седативного эффекта и характерного для препаратов второго поколения кардиотоксического действия (см. табл.).
Кроме того, по химическому строению (в зависимости от Х-связи) антигистаминные препараты подразделяют на несколько групп (этаноламины, этилендиамины, алкиламины, производные альфакарболина, хинуклидина, фенотиазина, пиперазина и пиперидина).
Антигистаминные препараты первого поколения (седативные). Все они хорошо растворяются в жирах и, помимо Н1-гистаминовых, блокируют также холинергические, мускариновые и серотониновые рецепторы. Являясь конкурентными блокаторами, они обратимо связываются с Н1-рецепторами, что обусловливает использование довольно высоких доз. Для них наиболее характерны следующие фармакологические свойства.
Более того, многие качества, о которых шла речь, позволили занять «старым» антигистаминным средствам свою нишу в области лечения некоторых патологий (мигрень, нарушения сна, экстрапирамидные расстройства, тревога, укачивание и др.), не связанных с аллергией. Немало антигистаминных препаратов первого поколения входит в состав комбинированных препаратов, применяющихся при простуде, как успокаивающие, снотворные и другие компоненты.
Наиболее часто используются хлоропирамин, дифенгидрамин, клемастин, ципрогептадин, прометазин, фенкарол и гидроксизин.
Хлоропирамин (Супрастин) — один из самых широко применяемых седативных антигистаминных препаратов. Обладает значительной антигистаминной активностью, периферическим антихолинергическим и умеренным спазмолитическим действием. Эффективен в большинстве случаев для лечения сезонного и круглогодичного аллергического риноконъюнктивита, отека Квинке, крапивницы, атопического дерматита, экземы, зуда различной этиологии; в парентеральной форме — для лечения острых аллергических состояний, требующих неотложной помощи. Предусматривает широкий диапазон используемых терапевтических доз. Не накапливается в сыворотке крови, поэтому не вызывает передозировку при длительном применении. Для Супрастина характерно быстрое наступление эффекта и кратковременность (в том числе и побочного) действия. При этом хлоропирамин может комбинироваться с неседативными Н1-блокаторами с целью увеличения продолжительности противоаллергического действия. Супрастин в настоящее время является одним из самых продаваемых антигистаминных препаратов в России. Это объективно связано с доказанной высокой эффективностью, управляемостью его клинического эффекта, наличием различных лекарственных форм, в том числе и инъекционных, и невысокой стоимостью.
Дифенгидрамин (Димедрол), — один из первых синтезированных Н1-блокаторов. Он обладает достаточно высокой антигистаминной активностью и снижает выраженность аллергических и псевдоаллергических реакций. За счет существенного холинолитического эффекта имеет противокашлевое, противорвотное действие и в то же время вызывает сухость слизистых, задержку мочеиспускания. Вследствие липофильности Димедрол дает выраженную седатацию и может использоваться как снотворное. Оказывает значительный местноанестезирующий эффект, вследствие чего иногда применяется как альтернатива при непереносимости новокаина и лидокаина. Димедрол представлен в различных лекарственных формах, в том числе и для парентерального применения, что определило его широкое использование в неотложной терапии. Однако значительный спектр побочных эффектов, непредсказуемость последствий и воздействия на ЦНС требуют повышенного внимания при его применении и по возможности использования альтернативных средств.
Клемастин (Тавегил) — высокоэффективный антигистаминный препарат, сходный по действию с дифенгидрамином. Обладает высокой антихолинергической активностью, однако в меньшей степени проникает через гематоэнцефалический барьер, чем и обусловлена невысокая частота наблюдения седативного эффекта — до 10%. Также существует в инъекционной форме, которая может использоваться как дополнительное средство при анафилактическом шоке и ангионевротическом отеке, для профилактики и лечения аллергических и псевдоаллергических реакций. Однако известна гиперчувствительность к клемастину и другим антигистаминным средствам, обладающим сходной с ним химической структурой.
Диметенден (Фенистил) — наиболее близок к антигистаминным препаратам второго поколения, от препаратов первого поколения отличается значительно меньшей выраженностью седативного и мускаринового эффекта, высокой противоаллергической активностью и длительностью действия.
Таким образом, антигистаминные средства первого поколения, влияющие как на Н1-, так и на другие рецепторы (серотониновые, центральные и периферические холинорецепторы, aльфа-адренорецепторы), обладают различными эффектами, что определило их применение при множестве состояний. Но выраженность побочных действий не позволяет рассматривать их как препараты первого выбора при лечении аллергических заболеваний. Опыт, накопленный при их применении, позволил разработать препараты однонаправленного действия — второе поколение антигистаминных средств.
Антигистаминные препараты второго поколения (неседативные). В отличие от предыдущего поколения они почти не обладают седативным и холинолитическим эффектами, а отличаются избирательностью действия на Н1-рецепторы. Однако для них в разной степени отмечен кардиотоксический эффект.
Наиболее общими для них являются следующие свойства.
Ниже представлены антигистаминные средства второй генерации с наиболее характерными для них свойствами.
Лоратадин (Кларитин) — один из самых покупаемых препаратов второго поколения, что вполне объяснимо и логично. Его антигистаминная активность выше, чем у астемизола и терфенадина, вследствие большей прочности связывания с периферическими Н1-рецепторами. Препарат лишен седативного эффекта и не потенцирует действие алкоголя. Кроме того, лоратадин практически не взаимодействует с другими лекарственными средствами и не обладает кардиотоксическим действием.
Нижеследующие антигистаминные средства относятся к препаратам местного действия и предназначены для купирования локальных проявлений аллергии.
Азеластин (Аллергодил) — высокоэффективное средство для лечения аллергического ринита и конъюнктивита. Применяемый в виде назального спрея и глазных капель азеластин практически лишен системного действия.
Цетиризин (Зиртек) — высокоселективный антагонист периферических Н1-рецепторов. Является активным метаболитом гидроксизина, обладающим гораздо менее выраженным седативным действием. Цетиризин почти не метаболизируется в организме, и скорость его выведения зависит от функции почек. Характерной его особенностью является высокая способность проникновения в кожу и, соответственно, эффективность при кожных проявлениях аллергии. Цетиризин ни в эксперименте, ни в клинике не показал какого-либо аритмогенного влияния на сердце.
Выводы
Итак, в арсенале врача имеется достаточное количество антигистаминных препаратов с различными свойствами. При этом необходимо помнить, что они обеспечивают лишь симптоматическое облегчение при аллергии. Кроме того, в зависимости от конкретной ситуации можно использовать как различные препараты, так и многообразные их формы. Для врача также важно помнить о безопасности антигистаминных средств.
К недостаткам большинства антигистаминных препаратов 1-го поколения относится феномен тахифилаксии (привыкание), требующий смены препарата каждые 7–10 дней, хотя, к примеру, для диметиндена (Фенистил) и клемастина (Тавегил) показана эффективность в течение 20 дней без развития тахифилаксии (Kirchhoff C. H. et al., 2003; Koers J. et al., 1999).
Продолжительность действия от 4–6 часов для дифенгидрамина, 6–8 часов у диметиндена, до 12 (а в некоторых случаях и 24) часов у клемастина, поэтому препараты назначаются 2–3 раза в сутки.
Несмотря на вышеперечисленные недостатки, антигистаминные препараты 1-го поколения занимают прочные позиции в аллергологической практике, особенно в педиатрии и гериатрии (Лусс Л. В., 2009). Наличие инъекционных форм данных лекарственных средств делает их незаменимыми в острых и неотложных ситуациях. Дополнительный антихолинергический эффект хлоропирамина значительно уменьшает зуд и кожные высыпания при атопическом дерматите у детей; снижает объем назальной секреции и купирование чихания при ОРВИ. Терапевтический эффект антигистаминных препаратов 1-го поколения при чихании и кашле в значительной мере может быть обусловлен блокадой Н1- и мускариновых рецепторов. Ципрогептадин и клемастин наряду с антигистаминовым действием обладают выраженной антисеротониновой активностью. Диментиден (Фенистил) дополнительно угнетает действие других медиаторов аллергии, в частности кининов. Более того, установлена более низкая стоимость антигистаминных средств 1-го поколения по сравнению с препаратами 2-го поколения.
Указывается эффективность пероральных антигистаминных препаратов 1-го поколения, не рекомендуется их использование в комбинации с оральными деконгестантами у детей.
Следовательно, преимуществами антигистаминных препаратов 1-го поколения являются: длительный опыт (в течение 70 лет) применения, хорошая изученность, возможность дозированного применения их у детей грудного возраста (для диметиндена), незаменимость при острых аллергических реакциях на пищевые продукты, лекарственные препараты, укусы насекомых, при проведении премедикации, в хирургической практике.
Особенностями анигистаминных препаратов 2-го поколения является высокое сродство (аффинность) к Н1-рецепторам, длительность действия (до 24 часов), низкая проходимость через гематоэнцефалический барьер в терапевтических дозах, отсутствие инактивации препарата пищей, отсутствие тахифилаксии. Практически данные препараты не подвергаются метаболизму в организме. Не вызывают развитие седативного эффекта, однако у некоторых пациентов может наблюдаться сонливость при их использовании.
Преимущества антигистаминных препаратов 2-го поколения заключается в следующем:
Антигистаминные препараты 2-го поколения характеризуются противоаллергическим и противовоспалительным действием. Описаны определенные антиаллергические эффекты, однако их клиническое значение остается неясным.
Длительная (годы) терапия пероральными антигистаминными средствами как первого, так и второго поколения безопасна. Некоторые, но не все препараты этой группы подвергаются метаболизму в печени под действием системы цитохрома Р450 и могут взаимодействовать с другими лекарственными веществами. Установлена безопасность и эффективность пероральных антигистаминных средств у детей. Их можно назначать даже маленьким детям.
Таким образом, имея столь широкий круг антигистаминных препаратов, врач имеет возможность выбирать лекарственное средство в зависимости от возраста пациента, конкретной клинической ситуации, диагноза. Антигистаминные препараты 1-го и 2-го поколения остаются неотъемлемой частью комплексного лечения аллергических заболеваний у взрослых и детей.
Литература
О. Б. Полосьянц, кандидат медицинских наук
ГКБ № 50, Москва
Контактная информация об авторе для переписки: 127206, Россия, Москва, ул. Вучетича, д. 217
.gif)