Лимфопролиферативного заболевания что это
Диагностика и мониторинг лимфопролиферативных заболеваний
Лейкопения – это снижение количества лейкоцитов в единице объема крови.
Лейкопения может появиться как следствие различных заболеваний, в том числе и онкологических.
Лейкоциты – это клетки, имеющие важное значение для иммунной системы человека; белые кровяные тельца выполняют защитную функцию для организма от вирусов, бактерий и прочих агентов, способных причинить вред человеку и вызвать заболевания.
Норма содержания лейкоцитов в крови: от 4 до 9 х 109 клеток/ 1л. Если выявлено их снижение, то это может быть сигналом о подозрении на лейкопению.
ФОРМЫ ЛИМФОПРОЛИФЕРАТИВНЫХ ЗАБОЛЕВАНИЙ:
Существуют различные виды лейкоцитов, обычно происходит снижение не всех, а только нескольких видов.
Причины возникновения лейкопении
ОСНОВНЫМИ ПРИЧИНАМИ ДАННОГО ЗАБОЛЕВАНИЯ ЯВЛЯЮТСЯ:
Опасность, которую несет лейкопения
Лейкоциты – это часть иммунной системы. Белые кровяные тельца атакуют чужеродные агенты, попадающие в организм, но при снижении лейкоцитов, иммунитет человека падает, защитные силы ослабевают. Организм становится более подвержен инфекционным заболеваниям.
Диагностика лимфопролиферативных заболеваний
Заболевание определяется с помощью общего анализа крови.Происходит подсчет содержания количества лейкоцитов в крови и соотношение различных видов лейкоцитов (лимфоциты, эозинофилы, базофилы, нейтрофилы, моноциты) в процентах.
Симптоматика при лейкопении может отсутствовать, особенно легкой степени заболевания. Первым симптомом может быть возникновение различных инфекций. У некоторых онкобольных наблюдается лихорадка, вызванная либо инфицированием, либо как реакция организма на прием химиопрепаратов, либо лихорадка имеет опухолевую причину.
ПОСКОЛЬКУ ЛЕЙКОПЕНИЯ ВЫЗЫВАЕТ НАРУШЕНИЕ ПРОЦЕССА КРОВЕТВОРЕНИЯ, ТО ВОЗМОЖНЫ СЛЕДУЮЩИЕ СИМПТОМЫ:
Лечение лимфопролиферативных заболеваний
Пациент, проходящий курс химиотерапии, должен находиться под постоянным наблюдением онколога, контролирующего уровень лейкоцитов в крови.
ПАЦИЕНТУ, КОТОРОМУ ДИАГНОСТИРОВАНО ДАННОЕ ЗАБОЛЕВАНИЕ СЛЕДУЕТ:
Пациент, у которого наблюдается ярко выраженная симптоматика заболевания помещается в изолированную палату, а медицинский персонал, с которым больной имеет контакт, обязательно должен соблюдать все санитарные правила антисептики. Пациент может быть направлен в гематологическую клинику, специализирующуюся только на заболеваниях крови.
Больному вводят лекарственные препараты, стимулирующие образование лейкоцитов, дополнительно могут быть назначены витаминно-минеральные комплексы для поддержания организма.
Аутоиммунный лимфопролиферативный синдром
Аутоиммунный лимфопролиферативный синдром – группа генетически обусловленных заболеваний, которые возникают по причине наследственных или соматических мутаций в генах, отвечающих за различные этапы FAS-обусловленного апоптоза. Симптоматика может быть вариабельной и наиболее часто включает в себя лимфаденопатию, спленомегалию и разнообразные аутоиммунные поражения системы крови, печени, щитовидной железы. Диагностика аутоиммунного лимфопролиферативного синдрома производится на основании результатов общего и биохимического анализов крови, биопсии лимфатических узлов, генетических исследований. Специфического лечения заболевания в настоящий момент нет, применяют комбинации иммунносупрессивной и цитотоксической терапии.
Общие сведения
Аутоиммунный лимфопролиферативный синдром (АЛС, ALPS, синдром Канале-Смит) – группа иммунодефицитных состояний, характеризующихся аутоиммунными цитопениями, лимфаденопатией, спленомегалией. Первые данные о заболевании стали поступать в 1968-м году, после чего вскоре началось бурное изучение патологии. Изначально АЛС был отнесен к первичным иммунодефицитам, однако со временем были обнаружены формы синдрома, обусловленные соматическими мутациями в детском и подростковом организме.
Данные о встречаемости у разных исследователей довольно сильно различаются, на сегодняшний момент описано более 500 случаев различных форм аутоиммунного лимфопролиферативного синдрома. Наследственные формы заболевания передаются по аутосомно-доминантному типу, при этом в развитии врожденных форм также довольно велика роль спонтанных мутаций. Среди больных с одинаковой частотой встречаются как мальчики, так и девочки.
Причины
Выяснено, что причиной любого типа АЛС является нарушение FAS-опосредованного апоптоза лимфоцитов. При образовании Т-лимфоцитов те линии, которые способны атаковать собственные ткани, уничтожаются за счет активизации рецепторов CD-95 (Fas-рецепторов) на поверхности их мембраны. Активация CD-95, относящегося к группе рецепторов фактора некроза опухолей, запускает многостадийную реакцию с участием каспаз, которая оканчивается апоптозом клетки.
При аутоиммунном лимфопролиферативном синдроме генетические мутации приводят к блоку этого процесса на определенном этапе, из-за чего устранения потенциально опасных клонов Т-лимфоцитов не происходит, и они начинают накапливаться в лимфатических узлах. Кроме того, создаются условия для аутоиммунного поражения органов и тканей.
Наиболее часто встречаются наследственные и спонтанные мутации в гене TNFRSF6, который кодирует собственно Fas-рецептор. При этом нарушение структуры белка (особенно домена, отвечающего за взаимодействие с FADD-молекулой) приводит к тому, что он становится неспособным выполнять свои рецепторные функции и активизировать апоптоз. Возможны и соматические мутации в гене FAS, которые в полной мере проявляют себя в позднем детском или подростковом периоде, и поэтому их относят к отдельной группе АЛС.
Второй по распространенности вариант аутоиммунного лимфопролиферативного синдрома обусловлен мутацией в гене CASP10, кодирующем цистин-аспарагин кислотную протеазу (каспаза-10). Этот белок играет ключевую роль в передаче сигнала об апоптозе с клеточной мембраны в ядро клетки. К этому же варианту относят и мутации гена CASP8.
Третьим по распространенности является аутоиммунный лимфопролиферативный синдром, который вызван мутацией в гене FASLG, кодирующем Fas-лиганд или рецептор CD-178. Он играет вспомогательную роль в распознавании факторов, стимулирующих апоптоз, и участвует в передаче сигнала в клетку.
Некоторые формы АЛС обусловлены мутацией гена NRAS, который кодирует «малый G-белок», принимающий участие в качестве вторичного мессенджера в передаче сигналов с мембраны в клетку, в том числе и ядро. Примерно в трети случаев аутоиммунного лимфопролиферативного синдрома врачам-иммунологам не удается установить непосредственную причину заболевания.
Классификация аутоиммунного лимфопролиферативного синдрома
При помощи методов современной генетики удалось выявить шесть основных форм АЛС:
ALPS 1A – вызвана мутацией гена TNFRSF6, расположенного на 10-й хромосоме, чаще всего имеет врожденный характер, наследуется по аутосомно-доминантному типу. По статистике, более 40% АЛС относятся именно к этой разновидности.
ALPS 1В – обусловлена мутацией гена FASLG, также довольно часто приводит к врожденному аутоиммунному лимфопролиферативному синдрому. К этому типу относят около 10% от всех клинических случаев АЛС.
ALPS 1m – ее причиной являются соматические мутации в гене FAS, возникающие в детском или подростковом возрасте и поэтому приводящие к поздним формам АЛС. При этом повреждение гена должно произойти в полипотентной клетке-предшественнице, которая способна дать начало многим линиям лимфоцитов. При этой форме наиболее часто возникает внезапная самопроизвольная ремиссия заболевания.
ALPS 2 – вызвана мутацией в генах CASP10 и, по некоторым данным, CASP8, которые кодируют белки-каспазы, передающие сигнал об апоптозе от рецептора к ядру клетки. Эта форма аутоиммунного лифопролиферативного синдрома составляет примерно 25% от всех случаев заболевания, может быть как врожденной, так и проявиться в более старшем возрасте.
ALPS 3 – мутация какого гена и характер ее наследования при этой форме неизвестны. Особенностью такого варианта АЛС является нарушение не только FAS-, но и IL2-опосредованного апоптоза, а также более тяжелый характер течения.
ALPS 4 – обусловлена мутацией гена NRAS, также кодирующего белки-передатчики внутриклеточного сигнала. Данный тип аутоиммунного лимфопролиферативного синдрома характеризуется более доброкачественным течением и умеренной выраженностью симптомов.
Симптомы аутоиммунного лимфопролиферативного синдрома
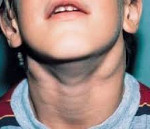
Симптомы АЛС довольно вариабельны из-за большого количества мутаций, которые могут приводить к такому состоянию. Начало заболевания можно заметить уже на 15-й день после рождения (при врожденных формах), в детском или подростковом возрасте в случае соматических мутаций в генах FAS, CASP10 или NRAS. Обычно первым проявлением заболевания является лимфаденопатия – подмышечные, паховые или шейные лимфатические узлы увеличиваются в размерах, но при этом безболезненны и не спаяны с окружающими тканями. Регистрируется спленомегалия, в некоторых случаях она сопровождается увеличением печени (гепатоспленомегалия).
Аутоиммунные проявления АЛС регистрируются обычно через некоторое время после лимфаденопатии и увеличения селезенки. В основном это поражения кровяных ростков – тромбоцитопения, гемолитическая анемия, приводящая к желтухе, изредка нейтропения. Помимо крови, аутоиммунному поражению могут подвергаться органы ЖКТ (возникают гастрит, панкреатит, колит, аутоиммунный гепатит). На коже могут проявляться признаки васкулита, делая клинику аутоиммунного лимфопролиферативного синдрома схожей с таковой при системной красной волчанке. Кроме того, могут возникать аутоиммунные формы тиреоидита, гломерулонефрита, поражаться суставы, ткани глаза (иридоциклит, увеит). Нередки поражения центральной нервной системы – эпилептические припадки, миелиты, мозжечковая атаксия.
Выраженность симптомов и их количество может значительно варьироваться у каждого конкретного больного. Кроме того, при аутоиммунном лимфопролиферативном синдроме в десятки раз возрастает риск развития злокачественных опухолей, так как опухолевые клоны лимфоцитов также устраняются посредством апоптоза.
Примерно в 20% случаев АЛС приводит к неходжкинским лимфомам (лимфома Беркитта, фолликулярная лимфома), описаны и другие онкологические заболевания. Из-за этого проявления АЛС могут быть ошибочно определены как следствие опухолевой инфильтрации лимфоидной ткани. Среди других осложнений аутоиммунного лимфопролиферативного синдрома наиболее часто встречается травматический разрыв селезенки, сепсис и другие инфекционные поражения.
Диагностика
Диагностика АЛС производится на основании осмотра, а также лабораторных, иммунологических и генетических исследований. При осмотре выявляют увеличение более чем трех групп лимфатических узлов, спленомегалию, увеличение печени. Анализ крови может показывать уменьшение количества некоторых клеток (анемию, тромбоцитопению), у части больных определяется высокая (до 30%) эозинофилия. Проба Кумбса положительная, в биохимическом анализе крови определяется выраженная гипергаммаглобулинемия.
Одним из высокочувствительных методов иммунологической диагностики аутоиммунного лимфопролиферативного синдрома является проточная иммуноцитофлюориметрия, проводимая с целью выявления количества лимфоцитов с атипичным набором рецепторов (CD3+CD4-CD8-). При АЛС количество таких клеток превышает 1% от всех лимфоцитов. В биоптате лимфатических узлов определяется фолликулярная гиперплазия, результатом гистологического исследования селезенки служит лимфоидная гиперплазия.
Врачом-генетиком может быть произведено секвенирование гена FAS с целью выявления мутаций, ставших причиной аутоиммунного лимфопролиферативного синдрома. С учетом значительной величины этого гена для ускорения и удешевления процедуры поиск может быть произведен лишь в отдельных экзонах гена FAS, в которых наиболее часто обнаруживаются нарушения – эти участки называют «горячими точками». Таким образом, при помощи генетической диагностики можно определить АЛС только 1А, 1В и 1m типов. Методики определения остальных форм АЛС генетическими методами на сегодняшний день не разработаны. Изучение наследственного анамнеза в ряде случаев будет неэффективно из-за значительной доли форм заболевания, вызванных соматическими мутациями.
Лечение аутоиммунного лимфопролиферативного синдрома
Этиотропное лечение аутоиммунного лимфопролиферативного синдрома не разработано, патогенетическая терапия сводится к применению иммуносупрессивных и цитотоксических средств. В качестве средств, подавляющих аутоиммунную активность, наиболее часто используют кортикостероиды (преднизолон, дексаметазон). К специфическим препаратам, ограничивающим скорость пролиферации лимфоцитов, относят микофенолата мофетил, сиролимус. Также при аутоиммунном лимфопролиферативном синдроме активно применяются традиционные цитотоксические средства – метотрексат, циклоспорин А и другие.
При значительном увеличении селезенки или отсутствии эффекта от консервативного лечения прибегают к спленэктомии. Пересадка костного мозга и использование стволовых клеток в долгосрочной перспективе давали только временный эффект. При значительно выраженных гематологических нарушениях применяют гемотрансфузии, введение эритроцитарной или тромбоцитарной массы. Больному следует избегать физических нагрузок, использовать высоковитаминную диету.
Прогноз
Прогноз заболевания, ввиду высокой вариабельности и выраженности симптомов, неопределенный или неблагоприятный. У большей части больных проявления заболевания постепенно нарастают, со временем приводя к летальной анемии, тромбоцитопении, билиарному циррозу печени. Также важную роль в прогнозе играют нарушения иммунитета, так как нередко причиной смерти выступают сепсис и другие инфекционные поражения. В прогнозе аутоиммунного лимфопролиферативного синдрома следует учитывать и повышенный риск онкологических заболеваний, примерно пятая часть больных умирает от различных типов лимфом. В некоторых случаях возникает спонтанная и длительная ремиссия патологии.
Лимфома
Лимфома – это злокачественное заболевание, которое характеризуется поражением лимфатических узлов и внутренних органов, в которых скапливаются «опухолевые» лимфоциты.
Акции
Запись на консультацию со скидкой 10%.
Онкоконсилиум может потребоваться как при лечении в «СМ-Клиника», так и пациентам других медицинских учреждений с целью получения альтернативного мнения.
«СМ-Клиника» предоставляет своим пациентам предоперационное обследование со скидкой до 72%!
Консультация врача-хирурга по поводу операции бесплатно!
Содержание статьи:
Лимфома (lymphoma) – злокачественная опухоль клеток иммунитета.При ней лимфоциты увеличиваются до гигантских размеров, бесконтрольно делятся и поражают лимфатическую систему: лимфоузлы, костный мозг, вилочковую железу.
От других онкологических заболеваний лимфома отличается диссеминацией по всему организму: с током лимфы переродившиесязлокачественныеклетки попадают во внутренние органы и критически нарушают их работу. Болезнь долго течет бессимптомно, а когда начинает проявляться, то часто весь организм уже поражен.
Большинстволимфомхарактеризуетсяпрогрессирующим течением и высокой злокачественностью с метастазированием. Тем не менее при раннем их выявлении благоприятный прогноз достигает
Статистические данные о лимфомах:
Виды лимфом
Различают две основные группы заболевания – лимфому Ходжкина и неходжкинские лимфомы. Они развиваются из разного типа клеток, отличаются характером течения и по-разному реагируют на терапию.
Неходжкинские лимфомы (НХЛ)поражают не только В-, но и Т-лимфоциты. Всего выделено 30 подтипов.Большинство из них менее агрессивно, но и труднее лечится.
Классификация неходжкинских лимфом в соответствии с 4-й редакцией ВОЗ 2008 года:
По характеру поражения и патогенезу все лимфомы делятся на 3 основные группы:
Для каждого вида лимфом существует особая схема лечения.
Стадии лимфом
В зависимости от распространенности опухоли определяют стадию патологического процесса. В соответствии с международной классификацией AnnArborвыделяют 4 стадии заболевания:
Каждую стадию дополнительно маркируют титрами А и Б. Титр А указывает на отсутствие ключевых симптомов – лихорадки, сильной ночной потливости и резкого снижения веса. Титр Б указывает, что такие проявления есть.
Причины возникновения лимфом
Единого причинного фактора развития заболевания не выделено. На данный момент ученые считают, что патпроцесс запускается комплексом причин. К ним относят:
Симптомы
Помимо основных симптомов – лихорадки, сильной ночной потливости и резкого снижения веса – для патологии характерны:
Иногда возможен кожный зуд. При поражениях опухолью грудной клетки возможны затрудненное дыхание, одышка и кашель. При локализации новообразования в брюшной полости наблюдают расстройства пищеварения, тошноту, рвоту, распирающие боли в животе и нижней части спины. При поражении костного мозга больные жалуются на боли в костях.Если в патологию вовлечены лицевые и черепные структуры, есть жалобы на головные боли и распирающие боли в лице и шее.
Диагностика лимфом
Диагноз ставят по результатам микроскопического исследования биоптата – образца лимфоидной ткани. По результатам дифференциальной биопсии определяют тип опухоли.
Методы лечения
Наиболее распространенные методы лечения лимфом:
Они применяются как в виде отдельных курсов, так и в комплексе. Выбор лечебной схемы зависит от вида опухоли и общего состояния больного.
Лечебная тактика
Индолентные лимфомы могут не требовать лечения, а только наблюдения онкогематолога. Терапия показана при первых признакахпрогрессированияпатпроцесса. При локализованныхопухоляхдостаточнорадиотерапевтического облучения пораженных структур. При генерализованных формах показана химиотерапия.
При агрессивном течении заболевания одна из наиболее эффективных лечебных схем – химиотерапия по протоколу СНОР в сочетании с иммунотерапевтическимипрепаратами из группы моноклональных антител. При высокоагрессивных видах опухолей может быть назначена высокодозная химиотерапия в сочетании с трансплантацией кроветорных стволовых клеток.
Лечение отдельных типов лимфом
Радиотерапия – излучение высокой мощности – в качестве самостоятельного лечения ЛГМ может быть оправдана в отдельных случаях – когда в процесс вовлечена одна, максимум две группы лимфатических узлов. Чаще ее назначают в комплексе с химиотерапией. На поздних стадиях заболевания метод показан в качестве паллиативного лечения.
Биологические препараты – моноклональные антитела – при лечении лимфомы применяют для активизации иммунной системы. Лучевую терапию проводят регионарно, в области вовлеченных в онкологический процесс лимфоузлов.
В некоторых случаях при лечении ЛГМ оправдано удаление селезенки. Если увеличенные лимфатические узлы сдавливают соседние органы,может быть показано их иссечение.
При рецидивах заболевания, а также с целью уничтожения раковых клеток, на которые не действуют стандартные дозировки лучевой и химиотерапии, назначают высокие терапевтические дозы, разрушающие вместе с опухолью ткани костного мозга. После такого курса показана трансплантация органа. Взятые заранее собственные либо донорские стволовые клетки формируют новую иммунную систему.
Хорошие результаты в лечении НХЛ демонстрирует также комбинация лучевой и химиотерапии. В некоторых случаях успешно применяют инновационную техникулюмбально-пункционного введения противоопухолевых антител.
НХЛ с агрессивным течением плохо поддаются лечению. Наиболее эффективный метод борьбы с этим заболеванием – пересадка костного мозга.
Прогнозы
Прогноз для пациентов с лимфомами зависит от стадии процесса, возраста и состояния больного, а также от результатов терапии. При лимфоме Ходжкина пациенты молодого возраста на ранних стадиях,как правило, полностью выздоравливают. У 8 из 10 удается добиться устойчивой ремиссии. Пятилетняя выживаемость при 1-й стадии составляет 95%, при 4-й – 65%.
При НХЛ селезенки, лимфоузлов и слизистых средняя пятилетняя выживаемость – порядка 70%. При НХЛ ЖКТ, слюнных желез, глазных орбит средняя пятилетняя выживаемость – около 60%. Менее благоприятный прогноз у агрессивных НХЛ молочных желез, яичников, ЦНС и костей – пятилетняя выживаемость в среднем меньше 30%.
Клинические рекомендации после лечения лимфом и профилактика
Избегайте факторов риска – интоксикаций и контакта с канцерогенами. Вакцинируйтесь, а если заболели инфекционной болезнью – не занимайтесь самолечением.
При первых признаках лимфомы обращайтесь к врачу. Ежегодно проходите профилактические медосмотры, придерживайтесь правильного питания и старайтесь вести здоровый образ жизни.
Источники:
Что такое лимфома? Причины возникновения, диагностику и методы лечения разберем в статье доктора Михайличенко В. Ю., хирурга со стажем в 20 лет.
Определение болезни. Причины заболевания
Лимфомы — это заболевания, для которых характерен первичный локальный злокачественный опухолевый рост, исходящий преимущественно из внекостномозговой лимфоидной ткани. В отличие от лейкозов с первичным поражением костного мозга и лейкемическими нарушениями периферической крови, лимфомы возникают в лимфатических узлах и проникают в окружающие ткани. При этом в костном мозге долгое время опухолевые клетки не образуются.
Краткое содержание статьи — в видео:
Лимфомы подразделяются на две большие группы:
Ходжкинские лимфомы встречаются в 40 % случаев, а неходжкинские — в 60 %. Единственный достоверный дифференциальный признак ходжкинских лимфом в отличие от неходжкинских — морфологическое исследование, при котором находят специфические для болезни Ходжкина клетки Березовского — Штернберга — Рида. В дальнейшем для уточнения диагноза проводят иммуногистохимическое исследование.
В структуре онкологических заболеваний Российской Федерации лимфома Ходжкина занимает 9-10 место. Мужчины болеют чаще женщин, городские жители — чаще сельских.
Отмечено два пика заболеваемость лимфомой Ходжкина у взрослых:
Вероятно, первый пик связан с увеличением пролиферативного потенциала клеток (способностью к делению), а второй пик — с ослаблением иммунного контроля.
Причины появления лимфом до конца не изучены, существуют особенности течения заболевания у детей и на фоне иммунодефицита (например, ВИЧ).
Симптомы лимфомы
Первые симптомы заболевания:
Первые признаки заболевания совпадают с клинической картиной ОРВИ или ОРЗ.
В течение нескольких недель происходят следующие изменения:
Как правило, увеличенные лимфатические узлы воспалительного характера болезненные при пальпации, плотно-эластичные, часто спаянные с гиперемированной кожей. Напротив, лимфоузлы при лимфоме плотные и абсолютно безболезненные.
При онкологическом заболевании увеличенный лимфатический узел может быть проявлением метастаза. Учитывая, что лимфатический узел является фильтром, который «вылавливает» инфекцию или опухолевые клетки, его увеличение сигнализирует о присутствии патологии и требует внимательного отношения со стороны больного. Изначально может увеличиваться один лимфатический узел и группа регионарных, но может и присутствовать и генерализованное увеличение лимфатических узлов.
Обширное разрастание опухоли в забрюшинном пространстве и брыжейке кишки приводит к кишечной непроходимости, отсутствию мочи с развитием гидронефроза. Соответственно локализация опухолевых клеток в селезёнке приведёт к увеличению селезёнки в размерах и боли в левом подреберье за счёт перерастяжения капсулы селезёнки.
Патогенез лимфомы
Патогенез лимфомы Ходжкина и неходжкинских лимфом различаются. При лимфоме Ходжкина лимфоидное новообразование появляется в одном лимфатическом узле или в цепочке лимфоузлов и изначально распространяется в пределах смежных лимфатических узлов. Неходжкинские лимфомы, как правило, возникают вне узлов и распространяются непредсказуемо.
Патогенез лимфомы Ходжкина
Выдвигаются различные теории происхождения лимфомы Ходжкина, основные из них:
Патогенез неходжкинской лимфомы
Доказанной теории возникновения НХЛ нет. Отмечается повышенное число заболевших среди следующих пациентов:
Таким образом, лимфомы возникают после сильной встряски иммунной системы с последующим её дисбалансом в виде бласттрансформации. При бласттрансформации по неизвестным причинам не происходит трансформация клеток во взрослый фенотип. Это приводит к большому неконтролируемому образованию бластов, что и является началом опухолевого роста.
Классификация и стадии развития лимфомы
Стадия I. Характеризуется поражением опухолевыми клетками лимфатических узлов одного региона (регионарное поражение). Допускается поражение одного лимфатического узла из другой регионарной группы, тогда к стадии I добавляется литера «Е».
Стадия II. Для второй стадии характерно поражение не менее двух лимфатических зон выше или ниже диафрагмы — это могут быть поражённые лимфатические узлы разных регионов, например шейных и подмышечных, узлов средостения и шейных и т. д. Добавление в классификации литеры «Е» происходит при поражении экстралимфатических тканей (печени, селезёнки, костного мозга) и/или органа по ту же сторону диафрагмы.
Стадия III. Поражение лимфатических узлов по обе стороны диафрагмы, например паховых и шейных, паховых и лимфатических узлов средостения. Номенклатура опухоли подразумевает чёткое определение экстранодальных поражений (поражение опухолевыми клетками вне лимфатических узлов):
Стадия IV. Множественное поражение лимфатических узлов в различных зонах организма человека или поражение экстралимфатических органов (одного или несколько). При этом лимфатические узлы могут быть как поражены, так нет.
Обязательным в классификации является оценка общего состояния пациента:
Осложнения лимфомы
| Статус | Определение |
|---|---|
| 0 | Физическая активность больного не отличается от активности до заболевания, пациент ведёт себя как абсолютно здоровый человек |
| 1 | Физическая активность снижена, но пациент сам передвигается и в состоянии выполнять не интенсивные физические нагрузки и заниматься лёгкими видами физической работы и умственным трудом |
| 2 | Физическая активность снижена, появляется утомляемость, но пациент способен самостоятельно передвигаться и обслуживать себя. Усталость компенсируется постельным режимом, которое занимает не более половины светлого времени суток |
| 3 | Физическая активность значительно снижена, пациент не способен полностью обслуживать себя в домашних условиях. Утомляемость вынуждает пациента более половины суток проводить в постели |
| 4 | Самая тяжёлая категория больных, они полностью обездвижены и постоянно находятся в постели или в сидячем положении, не могут себя обслуживать. Минимальная физическая нагрузка моментально истощает их, с пациентами невозможна длительная продуктивная коммуникация |
Осложнения при лимфоме Ходжкина:
Осложнения при неходжкинской лимфоме схожи, но есть некоторые особенности:
Диагностика лимфомы
Как правило, при отсутствии системных проявлений заболевания и увеличении одного или нескольких лимфатических узлов применяют антибиотики. Если картина не меняется, необходимо выполнить ряд дополнительных обследований (рентген грудной клетки, КТ, УЗИ) и пункционную биопсию. Достоверный диагноз лимфомы можно поставить только на основании гистологии, полученной при биопсии лимфатического узла. Наиболее информативный способ — это забор изменённого лимфатического узла. Для определения подвида лимфомы и назначения химиотерапии необходимо провести полное морфологическое исследование с обязательным иммуногистохимическим анализом.
Перед взятием биопсии, помимо стандартного клинического обследования, необходимо исключить следующие факторы, влияющие на изменение лимфоузлов:
Диагноз ставится только по результатам гистологического исследования поражённого лимфатического узла. Анализ проводят методом аспирационной биопсии (забор взвеси клеток). Для этого под новокаином трепан-иглой (режущая игла, оснащённая пункционным пистолетом) берут столбик ткани поражённого органа, затем окрашивают и изучают под микроскопом.
Для постановки диагноза пользуются последней версией МКБ (Международная классификация болезней) с учётом стадийности, которая оценивает не только распространение опухоли по лимфатическим узлам и тканям за пределами лимфатической системы, но и общее состояние больного.
Также для диагностики лимфом применяют лучевые методы:
Визуализация лимфатических узлов и интерпретация полученных результатов во многом зависят от оборудования и специалиста, который проводит обследование. Для оценки динамики лечения лучше наблюдаться в одном медицинском центре и у того же специалиста. Это поможет уменьшить погрешность техники и влияние человеческого фактора.
Лечение лимфомы
При увеличенных лимфатических узлах категорически запрещено заниматься самолечением. Прогревать лимфоузлы нельзя, так как это может привести к распространению инфекции или генерализации опухолевого процесса. Также нельзя прикладывать лёд — это только усилит воспаление и ухудшит общее состояние пациента.
В настоящее время разрабатываются молекулярно-генетические исследования опухолевых клеток, типирование, создание специфических сывороток и вакцин против каждого вида опухоли индивидуально для каждого пациента, но это медицина будущего и доступна пока единичным медицинским центрам.
Клинические рекомендации по определению эффективности лечения [4] [5]
Эффективность лечения следует оценивать после 2-3 курсов химиотерапии при сохранении стабильной клинической картины не менее двух недель. С помощью УЗИ, КТ, МРТ или ПЭТ оценивают:
Также проводят иммуногистохимическое исследование костного мозга для верификации опухолевых клеток. В зависимости от полученных данных, эффективность лечения расценивают как:
Эффективность терапии также оценивают в середине лечения с учётом размеров лимфатических узлов, количество поражённых лимфоузлов, размеров селезёнки, результата пункции костного мозга.
В литературе последних лет [11] [12] появились исследования о прогностическом значении микроРНК (малые некодирующие молекулы РНК) и других маркеров, позволяющих на ранних стадиях и после курса лечения определить возможность рецидива. Эти современные маркеры являются наиболее чувствительными методами, но пока находятся на стадии клинических испытаний.
Прогноз. Профилактика
Прогноз при лимфоме Ходжкина зависит от формы и стадии заболевания:
Хорошо выздоравливают молодые пациенты, особенно на ранних стадиях заболевания.
Неходжкинские лимфомы на ранних стадиях имеют относительно хороший прогноз. Современная терапия позволяет добиться более чем десятилетней выживаемости на ранних стадиях, но поздние стадии заболевания фактически не лечатся и приводят к смерти.
| Международный прогностический индекс (МПИ): | ||
|---|---|---|
| Параметр | Благоприятный | Неблагоприятный |
| Возраст, годы | ≤60 | >60 |
| Общее состояние по шкале ECOG | 0-1 | 2-4 |
| Уровень ЛДГ в сыворотке | Нормальный | Повышен |
| Число экстранодальных очагов поражения | ≤1 | >1 |
| Стадия Ann Arbor | I-II | III-IV |
В правой колонке таблицы представлены значения, характерные для неблагоприятного течения заболевания. Если каждый параметр принять за единицу, то рассчитывается МПИ следующим образом:
При достижении полной ремиссии регулярно проводится осмотр и опрос пациента, лабораторные исследования, рентгенологический контроль органов грудной клетки, УЗИ брюшной полости и периферических лимфатических коллекторов. Частота обследования:
После проведённой химио- и лучевой терапии необходимо проверять функции щитовидной и молочных желёз.
Методов профилактики лимфомы в настоящее время не существует, поскольку до конца не изучены этиологические факторы, ведущие к развитию заболевания.