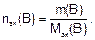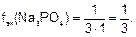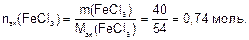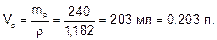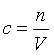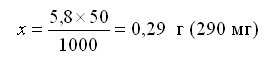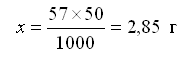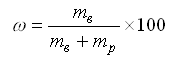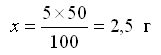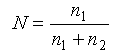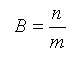Концентрация эквивалента в чем измеряется
Способы выражения концентрации
Существует множество способов измерить концентрацию раствора. Это так называемые способы выражения концентрации раствора.
Концентрация раствора — это количество вещества, находящегося в единице объема или массы раствора.
Что такое раствор
Среди окружающих нас веществ, лишь немногие представляют собой чистые вещества. Большинство являются смесями, состоящими из нескольких компонентов, которые могут находиться в одном или различных фазовых состояниях.
Смеси, имеющие однородный состав являются гомогенными, неоднородный состав – гетерогенными.
Иначе, гомогенные смеси, называют растворами, в которых одно вещество полностью растворяется в другом (растворителе). Растворитель – это тот компонент раствора, который при образовании раствора сохраняет свое фазовое состояние. Он обычно находится в наибольшем количестве.
Существуют растворы газовые, жидкие и твердые. Но более всего распространены жидкие растворы, поэтому, в данном разделе, именно на них мы сосредоточим свое внимание.
Концентрацию раствора можно охарактеризовать как:
Качественная концентрация характеризуется такими понятиями, как разбавленный и концентрированный раствор.
С этой точки зрения растворы можно классифицировать на:
Количественная концентрация выражается через молярную, нормальную (молярную концентрацию эквивалента), процентную, моляльную концентрации, титр и мольную долю.
Способы выражения концентрации растворов
Молярная концентрация растворов (молярность)
Раствор называют молярным или одномолярным, если в 1 литре раствора растворено 1 моль вещества, децимолярным – растворено 0,1 моля вещества, сантимолярным — растворено 0,01 моля вещества, миллимолярным — растворено 0,001 моля вещества.
Термин «молярная концентрация» распространяется на любой вид частиц.
Вместо обозначения единицы измерения — моль/л, возможно такое ее обозначение – М, например, 0,2 М HCl.
Молярная концентрация эквивалента или нормальная концентрация растворов (нормальность).
Понятие эквивалентности мы уже вводили. Напомним, что эквивалент – это условная частица, которая равноценна по химическому действию одному иону водорода в кислотоно-основных реакциях или одному электрону в окислительно – восстановительных реакциях.
Например, эквивалент KMnO4 в окислительно – восстановительной реакции в кислой среде равен 1/5 (KMnO4).
Еще одно необходимое понятие — фактор эквивалентности – это число, обозначающее, какая доля условной частицы реагирует с 1 ионом водорода в данной кислотоно-основной реакции или с одним электроном в данной окислительно – восстановительной реакции.
Он может быть равен 1 или быть меньше 1. Фактор эквивалентности, например, для KMnO4 в окислительно – восстановительной реакции в кислой среде составляет fэкв(KMnO4) = 1/5.
Следующее понятие – молярная масса эквивалента вещества х. Это масса 1 моля эквивалента этого вещества, равная произведению фактора эквивалентности на молярную массу вещества х:
Молярная концентрация эквивалента (нормальность) определяется числом молярных масс эквивалентов на 1 литр раствора.
Для обозначения нормальной концентрации допускается сокращение «н» вместо «моль/л».
Процентная концентрация раствора или массовая доля
Массовая концентрация показывает сколько единиц массы растворенного вещества содержится в 100 единицах массы раствора.
Это отношение массы m(х) вещества x к общей массе m раствора или смеси веществ:
Массовую долю выражают в долях от единицы или процентах.
Моляльная концентрация раствора
Моляльная концентрация раствора b(x) показывает количество молей n растворенного вещества х в 1 кг. растворителя m. Единица измерения моляльной концентрации — моль/кг :
Титр раствора
Титр раствора показывает массу растворенного вещества х, содержащуюся в 1 мл. раствора. Единица измерения титра — г/мл:
Мольная или молярная доля
Мольная или молярная доля α(х) вещества х в растворе равна отношению количества данного вещества n(х) к общему количеству всех веществ, содержащихся в растворе Σn:
Между приведенными способами выражения концентраций существует взаимосвязь, которая позволяет, зная одну единицу измерения концентрации найти (пересчитать) ее в другие единицы. Существуют формулы, позволяющие провести такой пересчет, которые, в случае необходимости, вы сможете найти в сети. В разделе задач показано, как произвести такой пересчет, не зная формул.
Пример перевода процентной концентрации в молярную, нормальную концентрацию, моляльность, титр
Решение.
1. Рассчитать молярную массу FeSO4:
M (FeSO4) = 56+32+16·4 = 152 г/моль
2. Рассчитать молярную массу эквивалента:
Мэ = fэкв· М(FeSO4) = 1/2·152 = 76 г/моль
3. Найдем m раствора объемом 2 л
4. Найдем массу 2 % раствора по формуле:
m(FeSO4) = 0,02·2,06 = 0,0412 кг = 41,2 г
5. Найдем молярность, которая определяется как количество молей растворенного вещества в одном литре раствора:
n = m/М
n = 41,2/152 = 0,27 моль
См = n/V
См = 0,27/2 = 0,135 моль/л
6. Найдем нормальность:
nэ = 41,2/76 = 0,54 моль
Сн = 0,54/2 = 0,27 моль/л
7. Найдем моляльность раствора. Моляльная концентрация равна:
b (x) = n(x)/m
Масса растворителя, т.е. воды в растворе равна:
mH2O = 2,06-0,0412 = 2,02 кг
b (FeSO4) = n(FeSO4)/m = 0,27/2,02 = 0,13 моль/кг
8. Найдем титр раствора, который показывает какая масса вещества содержится в 1 мл раствора:
Т(х) = m (х)/V
Т(FeSO4) = m (FeSO4)/V = 41,2/2000 = 0,0021 г/мл
Эквивалент. Закон эквивалентов
Материалы портала onx.distant.ru
Эквивалент. Закон эквивалентов
Эквивалент – реальная или условная частица вещества Х, которая в данной кислотно-основной реакции или реакции обмена эквивалентна одному иону водорода Н + (одному иону ОН — или единичному заряду), а в данной окислительно- восстановительной реакции эквивалентна одному электрону.
Фактор эквивалентности fэкв(X) – число, показывающее, какая доля реальной или условной частицы вещества Х эквивалентна одному иону водорода или одному электрону в данной реакции, т.е. доля, которую составляет эквивалент от молекулы, иона, атома или формульной единицы вещества.
Наряду с понятием “количество вещества”, соответствующее числу его моль, используется также понятие количество эквивалентов вещества.
Закон эквивалентов: вещества реагируют в количествах, пропорциональных их эквивалентам. Если взято n(экв1) моль эквивалентов одного вещества, то столько же моль эквивалентов другого вещества n(экв2) потребуется в данной реакции, т.е.
При проведении расчетов необходимо использовать следующие соотношения:
1. Молярная масса эквивалента вещества X равна его молярной массе, умноженной на фактор эквивалентности:
2. Количество эквивалентов вещества X определяется делением его массы на молярную массу эквивалента:
3. Объём моль-эквивалента газа Х при н.у. равен молярному объёму газа, умноженному на фактор эквивалентности:
4. Молярная масса эквивалента сложного вещества равна сумме молярных масс эквивалентов составляющих это вещество атомов (ионов).
5. Молярная масса эквивалента оксида равна молярной массе эквивалента элемента плюс молярная масса эквивалента кислорода.
6. Молярная масса эквивалента гидроксида металла равна молярной массе эквивалента металла плюс молярная масса эквивалента гидроксила, например:
М[½Са(ОН)2] = 20 + 17 = 37 г/моль.
М(½ СаSO4) = 20 + 48 = 68 г/моль.
Эквивалент в кислотно-основных реакциях
На примере взаимодействия ортофосфорной кислоты со щелочью с образованием дигидро-, гидро- и среднего фосфата рассмотрим эквивалент вещества H3PO4.
Эквивалент NaOH соответствует формульной единице этого вещества, так как фактор эквивалентности NaOH равен единице. В первом уравнении реакции молярное соотношение реагентов равно 1:1, следовательно, фактор эквивалентности H3PO4 в этой реакции равен 1, а эквивалентом является формульная единица вещества H3PO4.
В третьем уравнении реакции количество веществ реагентов относятся друг к другу как 1:3. Следовательно, фактор эквивалентности H3PO4 равен 1/3, а её эквивалентом является 1/3 часть формульной единицы вещества H3PO4.
Таким образом, эквивалент вещества зависит от вида химического превращения, в котором принимает участие рассматриваемое вещество.
Следует обратить внимание на эффективность применения закона эквивалентов: стехиометрические расчёты упрощаются при использовании закона эквивалентов, в частности, при проведении этих расчётов отпадает необходимость записывать полное уравнение химической реакции и учитывать стехиометрические коэффициенты. Например, на взаимодействие без остатка 0,25 моль-экв ортофосфата натрия потребуется равное количество эквивалентов вещества хлорида кальция, т.е. n(1/2CaCl2) = 0,25 моль.
Эквивалент в окислительно-восстановительных реакциях
Фактор эквивалентности соединений в окислительно-восстановительных реакциях равен:
где n – число отданных или присоединенных электронов.
Для определения фактора эквивалентности рассмотрим три уравнения реакций с участием перманганата калия:
В результате получаем следующую схему превращения KMnO4.
в кислой среде: Mn +7 + 5e = Mn +2
в нейтральной среде: Mn +7 + 3e = Mn +4
в щелочной среде: Mn +7 + 1e = Mn +6
Схема превращений KMnO4 в различных средах
Таким образом, в первой реакции fэкв(KMnO4) = 1/5, во второй – fэкв(KMnO4) = 1/3, в третьей – fэкв(KMnO4) = 1.
Следует подчеркнуть, что фактор эквивалентности дихромата калия, реагирующего в качестве окислителя в кислой среде, равен 1/6:
Примеры решения задач
Задача 1. Определить фактор эквивалентности сульфата алюминия, который взаимодействует со щелочью.
Решение. В данном случае возможно несколько вариантов ответа:
Задача 2. Определить факторы эквивалентности Fe3О4 и KCr(SO4)2 в реакциях взаимодействия оксида железа с избытком хлороводородной кислоты и взаимодействия двойной соли KCr(SO4)2 со стехиометрическим количеством щёлочи КОН с образованием гидроксида хрома (III).
Задача 3. Определить факторы эквивалентности и молярные массы эквивалентов оксидов CrО, Cr2О3 и CrО3 в кислотно-основных реакциях.
CrО3 – кислотный оксид. Он взаимодействует со щёлочью:
Молярные массы эквивалентов рассматриваемых оксидов равны:
Мэкв(CrО) = 68(1/2) = 34 г/моль,
Задача 4. Определить объём 1 моль-экв О2, NH3 и H2S при н.у. в реакциях:
Vэкв(NH3) = 22,4× 1/3 = 7,47 л – в первой реакции.
Vэкв(NH3) = 22,4× 1/5 = 4,48 л – во второй реакции.
В третьей реакции для сероводорода Vэкв(H2S)=22,4 1/6 = 3,73 л.
Задача 5. 0,45 г металла вытесняют из кислоты 0,56 л (н.у.) водорода. Определить молярную массу эквивалента металла, его оксида, гидроксида и сульфата.
Задача 6. Рассчитать массу перманганата калия, необходимую для окисления 7,9 г сульфита калия в кислой и нейтральной средах.
fэкв(K2SО3) = 1/2 (в кислой и нейтральной среде).
В кислой среде Мэкв(KMnO4) = 158·1/5 = 31,6 г/моль, m(KMnO4) = 0,1·31,6 = 3,16 г.
В нейтральной среде Мэкв (KMnO4) = 158·1/3 = 52,7 г/моль, m(KMnO4) = 0,1·52,7 =5,27 г.
Задача 7. Рассчитать молярную массу эквивалента металла, если оксид этого металла содержит 47 мас.% кислорода.
Выбираем для расчётов образец оксида металла массой 100 г. Тогда масса кислорода в оксиде составляет 47 г, а масса металла – 53 г.
В оксиде: nэкв (металла) = nэкв(кислорода). Следовательно:
53:Мэкв(Ме) = 47:(32·1/4). В результате получаем Мэкв(Ме) = 9 г/моль.
Задачи для самостоятельного решения
2.1. Молярная масса эквивалента металла равна 9 г/моль. Рассчитать молярную массу эквивалента его нитрата и сульфата.
Ответ: 71 г/моль; 57 г/моль.
2.2. Молярная масса эквивалента карбоната некоторого металла составляет 74 г/моль. Определить молярные массы эквивалентов этого металла и его оксида.
Ответ: 44 г/моль; 52 г/моль.
2.3. Рассчитать объём 1 моля эквивалента сероводорода (н.у.), который окисляется до оксида серы (IV).
Ответ: 3,73 л.
2.4. Определить молярную массу эквивалента Ni(OH)Cl в реакциях:
Ni(OH)Cl + NaOH = Ni(OH)2 + NaCl.
Ответ: 55,6 г/моль; 111,2 г/моль.
2.5. При взаимодействии 4,8 г неизвестного металла и 13 г цинка с соляной кислотой выделяется одинаковый объём водорода. Вычислить молярные массы эквивалентов металла, его оксида и его хлорида.
Ответ: МЭ(металла)=12 г/моль; МЭ(оксида)=20 г/моль, МЭ(хлорида)=47,5 г/моль.
2.6. Рассчитать молярные массы эквивалентов металла и его гидроксида, если хлорид этого металла содержит 79,7 мас.% хлора, а молярная масса эквивалента хлора равна 35,5 г/моль.
Ответ: МЭ(металла)=9 г/моль; МЭ(оксида)=26 г/моль.
2.7. Какой объём 0,6 М раствора H2O2 пойдёт на окисление 150 мл 2н. раствора FeSO4 в реакции:
Ответ: 250 мл.
2.8. Определить объём хлора (н.у), необходимый для окисления 100 мл 0,5н раствора K2MnO4.
Ответ: 0,56 л.
2.9. 0,66 г кислоты требуются для нейтрализации 10 мл 1М раствора КОН. Найти молярные массы эквивалентов кислоты и ее кальциевой соли в обменной реакции.
Ответ: МЭ(кислоты)=66 г/моль; МЭ(соли)=85 г/моль.
2.10. Бромид металла в результате обменной реакции полностью переведен в сульфат, при этом масса уменьшилась в 1,47 раз. Найти молярную массу эквивалента металла. Определить какой это металл.
Ответ: МЭ(металла)=20 г/моль; Са.
Концентрация растворов. Способы выражения концентрации растворов.
Концентрация раствора может выражаться как в безразмерных единицах (долях, процентах), так и в размерных величинах (массовых долях, молярности, титрах, мольных долях).
Способы выражения концентрации растворов.
1. Массовая доля (или процентная концентрация вещества) – это отношение массы растворенного вещества m к общей массе раствора. Для бинарного раствора, состоящего из растворённого вещества и растворителя:

ω – массовая доля растворенного вещества;
mв-ва – масса растворённого вещества;
Массовую долю выражают в долях от единицы или в процентах.
2. Молярная концентрация или молярность – это количество молей растворённого вещества в одном литре раствора V:

C – молярная концентрация растворённого вещества, моль/л (возможно также обозначение М, например, 0,2 М HCl);
n – количество растворенного вещества, моль;
V – объём раствора, л.
Раствор называют молярным или одномолярным, если в 1 литре раствора растворено 1 моль вещества, децимолярным – растворено 0,1 моля вещества, сантимолярным – растворено 0,01 моля вещества, миллимолярным – растворено 0,001 моля вещества.
3. Моляльная концентрация (моляльность) раствора С(x) показывает количество молей n растворенного вещества в 1 кг растворителя m:

С (x) – моляльность, моль/кг;
n – количество растворенного вещества, моль;
4. Титр – содержание вещества в граммах в 1 мл раствора:

T – титр растворённого вещества, г/мл;
mв-ва – масса растворенного вещества, г;
5. Мольная доля растворённого вещества – безразмерная величина, равная отношению количества растворенного вещества n к общему количеству веществ в растворе:

N – мольная доля растворённого вещества;
n – количество растворённого вещества, моль;
nр-ля – количество вещества растворителя, моль.
Сумма мольных долей должна равняться 1:
Иногда при решении задач необходимо переходить от одних единиц выражения к другим:
М(Х) – молярная масса растворенного вещества;
ρ= m/(1000V) – плотность раствора. 6. Нормальная концентрация растворов (нормальность или молярная концентрация эквивалента) – число грамм-эквивалентов данного вещества в одном литре раствора.
Грамм-эквивалент вещества – количество граммов вещества, численно равное его эквиваленту.
Эквивалент – это условная единица, равноценная одному иону водорода в кислотоно-основных реакциях или одному электрону в окислительно – восстановительных реакциях.
Для записи концентрации таких растворов используют сокращения н или N. Например, раствор, содержащий 0,1 моль-экв/л, называют децинормальным и записывают как 0,1 н.

СН – нормальная концентрация, моль-экв/л;
z – число эквивалентности;
Коэффициент растворимости – отношение массы вещества, образующего насыщенный раствор при конкретной температуре, к массе растворителя:
Молярная концентрация эквивалента(нормальная или эквивалентная концентрация)
Молярная концентрация эквивалента (нормальность) показывает, какое количество моль эквивалентов растворенного вещества содержится в 1 л раствора.
Молярную концентрацию эквивалента Сэк(В) находят как отношение количества эквивалентов вещества nэк(В) к объему раствора Vp
Размерность молярной концентрации эквивалента: моль•л. Сокращенная форма записи единицы молярной концентрации эквивалента – н. моль•л. Например, 2н. означает, что в 1 л раствора содержится 2 моль эквивалента растворенного вещества.
Зная массу растворенного вещества m(B) и его молярную массу эквивалента Мэк(В), можно найти количество эквивалента вещества:
Молярная масса эквивалента вещества равна произведению фактора эквивалентности fэк(В) на молярную массу вещества М(В)
Эквивалент – это реальная или условная частица вещества, соответствующая в реакциях обмена одному атому или иону водорода (Н или Н+), а в окислительно-восстановительных реакциях – одному электрону.
Фактор эквивалентности – число, показывающее, какую часть от реальной частицы (молекулы, атома, иона и т.д.) вещества составляет эквивалент этого вещества.
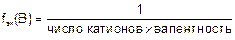
Например, для Na3PO4 заряд катиона Na+ равен 1, число катионов – 3, тогда
Пример. Вычислите молярную концентрацию эквивалента хлорида железа (III) в растворе, полученном при растворении 40 г FeCl3 в 200 мл воды. Плотность раствора 1,182 г/мл.
Молярная масса хлорида железа (III):
Фактор эквивалентности fэк = 1/3.
Молярная масса эквивалента
Mэк(FeCl3) = fэк(FeCl3)•M(FeCl3) = 162 • (1/3) = 54 г/моль.
Количество эквивалента вещества, содержащегося в 40 г хлорида железа (III), составляет:
r(H2O) = 1 г/мл; m(H2O) = 200 • 1 = 200 г;
mp = 40 + 200 = 240 г.
Объем раствора:
Находим молярную концентрацию эквивалента раствора хлорида железа (III):
Концентрация эквивалента в чем измеряется
В технологии выполнения химических анализов необходимым элементом является приготовление растворов химических веществ. В химическом анализе используются различные растворенные вещества (реагенты, буферные смеси, фиксирующие агенты, консерванты и т.п.) и растворители (вода, этанол и водно-спиртовые смеси, органические экстрагенты). В учебных пособиях, руководствах для химиков-аналитиков, нормативных документах (ГОСТах, РД, МУ) и справочной литературе можно встретить различные способы выражения концентраций. Ниже мы остановимся на некоторых из них, наиболее часто встречающихся, но сначала приведем краткую информацию по основополагающим единицам измерений, применяющихся при описании различных способов выражения концентраций химических веществ в растворах*.
Масса вещества обозначается как m(X) (где X – химический символ вещества) и обычно измеряется в граммах или миллиграммах.
За единицу количества вещества n(X) принят моль. Масса одного моля вещества называется молярной массой вещества. Последняя обозначается буквой «М» и обычно измеряется в г/моль. Например, М(Cu) = 63,54 г/моль, М(Н2SO4) = 98,08 г/моль.
Наряду с единицей количества вещества используется также единица количества вещества эквивалентов n[(1/z)Х], определяемая как произведение числа эквивалентности z(X) на количество вещества n(X). При этом под эквивалентом подразумевают реальную или условную частицу вещества, которая в конкретной кислотно-основной реакции эквивалентна одному иону водорода, в окислительно-восстановительной реакции – одному электрону. Соответственно, число эквивалентности z(Х) определяется исходя из химической формулы вещества и типа химической реакции:
для кислот z(Х) равно числу катионов водорода, способных замещаться катионами металлов. Например, z(НCl) = 1; z(Н2SO4) = 2;
для солей z равно числу катионов водорода кислоты, замещенных катионами металла или аммония. Например, z(NaCl) = 1; z[Fe2(SO4)3] = 6.
Молярная масса эквивалента M[(1/z)X] есть отношение молярной массы M(X) вещества к числу эквивалентности. Например, M(1/1HCl) = 36,46/1=36,46 г/моль; M[1/6Fe2(SO4)3] = 399,88/6 = 66,65 г/моль.
Понятие «молярная масса эквивалента» равноценно прежнему «грамм-эквивалент», в современной литературе не используемому.
Молярная концентрация вещества (с) в моль/л – отношение количества растворенного вещества в молях (n) к объему раствора (V):
Молярная концентрация численно равна количеству молей вещества, содержащихся в 1 литре (1000 мл, 1 дм 3 ) раствора.
Молярную концентрацию записывают следующим образом: с(НCl) = 3 моль/л; с(Н2SO4) = 2 моль/л.
Пример. Приготовление 50 мл раствора поваренной соли с молярной концентрацией 0,1 моль/л (т.е. с(NaCl) = 0,1 моль/л).
Молярная масса NaCl составляет М(NaCl) = 58 г/моль. В 1000 мл раствора с концентрацией с(NaCl)=0,1 моль/л должно содержаться n(NaCl) = 0,1 моль NaCl, или m(NaCl) = 5,8 г. В 50 мл раствора должно содержаться х г NaCl, определяемое по формуле:
Навеску в 0,29 г следует поместить в мерную колбу на 50 мл и долить дистиллированную воду до метки. Содержимое колбы перемешивать до полного растворения соли.
Молярная концентрация эквивалента** с[(1/z)Х] есть произведение молярной концентрации с(Х) на число эквивалентности z данного вещества, т.е. с[(1/z)Х] = с(Х)×z. Молярная концентрация эквивалента показывает количество вещества эквивалентов, содержащееся в 1 л раствора.
Для многих используемых в химическом анализе растворов (KCl, HCl, NaOH и др.) молярная концентрация эквивалентов веществ совпадает с их молярной концентрацией.
Размерность молярной концентрации эквивалентов вещества записывается в виде «моль/л экв.» («ммоль/л экв.»).
Пример. Приготовление 50 мл раствора сульфата алюминия c молярной концентрацией эквивалента 1 моль/л (т.е. c[(1/z)Al2(SO4)3] = 1 моль/л экв.).
Составляем пропорцию: 57 г Al2(SO4)3 должно содержаться в 1000 мл раствора, х г – в 50 мл раствора:
Следовательно, необходимо отвесить на весах 2,85 г Al2SO4, поместить эту навеску в мерную колбу на 50 мл и долить дистиллированную воду до метки. Содержимое колбы перемешивать до полного растворения соли.
Массовая доля (массовый процент, процентная концентрация) (w) в % – отношение массы растворенного вещества (mв) к общей массе раствора, т.е. сумме масс растворенного вещества и растворителя (mр):
Пример. Приготовление 50 г раствора соли с массовой долей 5% (5%-ного раствора).
В 100 г раствора содержится 5 г соли, в 50 г раствора содержится – х г соли.
Отвесить 2,5 г соли, поместить ее в колбу (стакан) и добавить 47,5 мл воды. Перемешивать до полного растворения соли.
Мольная доля (N) – отношение числа молей данного компонента (n1) к сумме молей данного компонента и всех других компонентов раствора (растворителя и других растворенных веществ (n2):
Аналогично определяется объемная доля.
Моляльная концентрация (В) в моль/кг – отношение количества растворенного вещества в молях (n) к массе растворителя (m):
Часто встречаются также производные от единиц измерения концентраций: например, мг/л, мг/дм3, мг/см3, мг/мл, ммоль/л, г/мл (титр) и др. Наиболее употребимыми единицами в справочной литературе применительно к оценке содержания примесей в воде (например, значения ПДК) являются мг/л и ммоль/л экв.
* В настоящее время способы выражения концентраций химических веществ в международной системе единиц (СИ) приводятся в соответствии с ГОСТ 8.417-81.
** В опубликованной ранее литературе по химическому анализу и методиках выполнения измерений для выражения данного вида концентрации встречаются также имеющие те же числовые значения единицы нормальность, эквивалентная концентрация, нормальная концентрация (н., N), применявшиеся до введения ГОСТа 8.417-81.