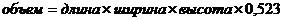Края резекции негативные что такое
Методика морфологического исследования препарата после радикальной простатэктомии
Набебина Т.И., Дубровский А.Ч., Ролевич А.И., Поляков С.Л.
В последние годы отмечается значительный рост выявления рака предстательной железы (РПЖ) на территории Республики Беларусь. По всей видимости, этот рост отражает наметившуюся тенденцию в странах СНГ к раннему выявлению РПЖ вследствие участившегося определения уровня простат-специфического антигена (ПСА) в крови у бессимптомных пациентов [1]. Увеличение частоты выявления локализованного и местно-распространенного РПЖ привело к увеличению частоты выполнения радикальной простатэктомии (РП) в последние 3-5 лет в ГУ НИИ ОМР (рис. 1).
Одним из самых важных вопросов, стоящих перед патоморфологами и урологами, является грамотное определение прогноза после операции для каждого конкретного больного. Результаты патоморфологического исследования препарата после РП являются наиболее ценной информацией для ответа на этот вопрос. Так, по данным Stamey с соавт. [2] рецидив РПЖ после РП может быть предсказан с высокой степенью точности на основании результатов патоморфологического исследования. В настоящей работе, в основу которой положены последние рекомендации рабочей группы Европейского Общества Уропатологов [3], дается обзор методики морфологического исследования препарата после РП.
СТРОЕНИЕ И ФУНКЦИЯ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
Роль и функция предстательной железы (ПЖ) в организме мужчины, по-видимому, до конца не выяснены. Секрет железы составляет около 20% объема семенной жидкости, в нем содержатся вещества, способствующие подвижности сперматозоидов, но не являющиеся жизненно необходимыми для оплодотворения. ПЖ охватывает проксимальную часть мочеиспускательного канала и имеет форму усеченного конуса, обращенного широкой частью к мочевому пузырю. Выделяют переднюю, заднюю и боковые поверхности, снизу – верхушку и сверху – основание. Проходящая по задней поверхности бороздка делит ПЖ на две доли.
ПЖ состоит из тубуло-альвеолярных желез, сгруппированных в дольки и окружающей железы стромы. Выводные протоки желез соединяются в более крупные, которые открываются в простатическую уретру. ПЖ окружена плотной капсулой, состоящей из коллагена, эластина и большого количества гладкой мускулатуры. ПЖ граничит с прямой кишкой сзади, мочевым пузырем сверху и лонной костью спереди, мышцами тазового дна латерально и произвольным поперечно-полосатым сфинктером снизу. Кзади и латеральнее ПЖ проходят т.н. сосудисто-нервные пучки. В их составе идут тонкие ветви внутренней подвздошной артерии, кровоснабжающие семенные пузырьки и простату. Эти сосуды сопровождают вегетативные нервные волокна (т. н. кавернозные нервы), которые идут от тазового сплетения и иннервируют ПЖ и кавернозные тела полового члена. ПЖ окружена венозным Санториниевым сплетением.
Зональная анатомия ПЖ. ПЖ состоит из пяти зон: центральной, периферической, переходной, периуретральной и передней фибромускулярной стромы (рис. 2). РПЖ развивается с различной частотой в каждой зоне, и эта частота не пропорциональна массе железистой ткани в ней. Центральная и периферическая зоны – наиболее крупные участки ПЖ – вместе составляют около 95% железистой ткани предстательной железы. Центральная зона окружает семявыносящие протоки на их пути от основания ПЖ к семенному бугорку. Центральная зона занимает 15-20% объема железы, однако в ней возникают только 5-10% от всех РПЖ. Периферическая зона – пальпируемая через прямую кишку часть железы. Она окружает центральную зону, включает 70% железистой ткани, и в ней возникает около 70% аденокарцином ПЖ. Переходная зона – парные участки ПЖ, которые располагаются по бокам от простатической уретры на уровне семенного бугорка, занимают оставшиеся 5% железы. Самой частой патологией этой зоны является доброкачественная гиперплазия предстательной железы (ДГПЖ), которая может приводить к значительному увеличению этих зон, иногда превышающему по объему остальные участки ПЖ. В этой зоне РПЖ развиваются реже, чем ДГПЖ, частота его составляет около 20%. Периуретральные железы располагаются между простатической уретрой и проксимальным гладкомышечным сфинктером мочевого пузыря. Фибромускулярная строма занимает переднюю поверхность ПЖ и состоит преимущественно из мышечной ткани. Аденокарциномы в двух последних зонах не развиваются.
МЕТОДИКА ОБРАБОТКИ МАКРОПРЕПАРАТА ПОСЛЕ РП
Свежий (нефиксированный) препарат после РП рекомендуется взвешивать и измерять в трех измерениях (длина, ширина и толщина). Оценка веса макропрепарата после РП достаточно важна, особенно в сочетании с комментариями патоморфолога, относящимися к оценке полноты резекции предстательной железы. Из-за того, что ПЖ имеет неправильную форму и симметрична только относительно сагиттальной плоскости, линейные размеры препарата менее точны, воспроизводимы и ценны чем вес препарата [5, 6]. Объем препарата может быть приблизительно определен по формуле, используемой для округлых образований [7]:
Поскольку поверхность ПЖ покрывает фиброзно-мышечная ткань, не образующая отдельной обособленный гистологической границы между железой и экстрапростатической соединительной тканью, оценить радикальность операции может быть весьма сложно как хирургу, так и патоморфологу, что привело к разработке специальной методики оценки краев резекции ПЖ. Для последующего определения состояния краев резекции органа вся поверхность удаленной и нефиксированной ПЖ должна быть окрашена. Если этого не выполнить, то морфолог не сможет определить в микропрепарате является ли обнаружение роста опухоли по краю позитивным хирургическим краем или это артефакт нарезки. Также достоверно судить о наличии опухоли по краю резекции на основании осмотра поверхности макропрепарата также нельзя. Для этого может использоваться черная тушь, поскольку черные края резекции проще распознаются при микроскопическом исследовании. Другим вариантом окраски поверхности железы является применение двух разных цветов для каждой стороны препарата для облегчения последующей ориентации и распознавания правой и левой стороны [8]. Обычно используются зеленый и красный (или синий) цвета. После окраски поверхности препарат погружается в фиксирующий раствор, например раствор Боуэна или уксусную кислоту, после чего тушь фиксируется на поверхности ПЖ и не смывается при проводке [8].
Перед разрезанием ПЖ на фрагменты рекомендуется ее фиксировать в формалине, что обеспечивает получение более тонких срезов. Для снижения времени фиксации и равномерной пенетрации формалина в железу, в препарат инъекционно вводится нейтральный 10% раствор формалина с использованием тонкой внутрикожной иглы. Обоснованием этой методики является то, что при обычном погружении железы в раствор формалина, проникновение его в толщу органа слишком медленное и неравномерное, кроме того, коагулированные формалином белки в ткани периферической зоны ПЖ затрудняют дальнейшую пенетрацию раствора [9].
После фиксации производится нарезка препарата на отдельные части (рис. 3). Сначала из макропрепарата удаляются семенные пузырьки. Семенные пузырьки исследуются после их секции через место вхождения в ПЖ (основание семенного пузырька) [10]. Практически все случаи опухолевой инвазии семенных пузырьков первоначально вовлекают основание семенного пузырька. Опухоль врастает в семенные пузырьки либо прямо через семяизвергающий проток либо вторично вследствие распространения опухоли за пределы ПЖ в перипростатические соединительные ткани и затем в просвет семенного пузырька [10].
После удаления семенных пузырьков двумя поперечными разрезами на расстоянии 4 мм от дистального и проксимального краев ПЖ от препарата отрезаются апикальная и базальная части железы. Эти участки затем нарезаются на части в парасагиттальном направлении перпендикулярно окрашенной поверхности с интервалом 4 мм как показано на рис. 3.
Оставшийся после удаления апикальной и базальной частей ПЖ макропрепарат последовательно нарезается с 4 мм интервалами перпендикулярно длинной (апико-базальной) оси ПЖ. Эти срезы ПЖ рекомендуется обозначать последовательными заглавными буквами алфавита, всегда начиная с наиболее апикального участка и заканчивая базальным. Такие срезы через всю ПЖ после заливки в парафин для микроскопического исследования рекомендуется нарезать таким же образом, т.е. перпендикулярно длинной (апико-базальной) оси на всю толщу ПЖ. Альтернативой такому приготовлению микропрепаратов может быть разделение 4-мм слоев на квадранты, которые нумеруются арабскими цифрами. При таком методе вся предстательная железа доступна для гистологического исследования [11]. Если для окраски поверхности ПЖ используется тушь, то для пометки правой стороны используется надрез скальпелем каждого среза по переднее-латеральной поверхности препарата справа. После такой нарезки препарата фрагменты можно дополнительно фиксировать в формалине в течение 24 ч.
Обоснованием необходимости полной заливки ПЖ в парафин является то, что идентификация локализации и распространения опухоли при макроскопическом исследовании порезанной ПЖ не всегда возможна, особенно при РПЖ, выявленном случайно или в ходе скрининга. Недавно опубликованное исследование Desai с соавт. [12] демонстрирует, что по сравнению с обычной методикой приготовления микропрепарата, полная заливка и частая нарезка макропрепарата после РП увеличивает частоту выявления распространения опухоли за пределы ПЖ, и приводит к повышению безрецидивной выживаемости при каждой стадии РПЖ.
Получившиеся фрагменты ПЖ ступенчато дегидратируются в разведенных спиртах, осветляются в ксилоле, заливаются в парафин, нарезаются на слои толщиной 5 мкм, окрашиваются гематоксилин-эозином, после чего могут исследоваться гистологически (рис. 4). При этом должны использоваться формовочные кассеты и предметные стекла специальных размеров. Предметные и покровные стекла должны быть как минимум 76 мм в длину и 50 мм в ширину [11, 13].
Выбор между получением срезов всего препарата или исследования его квадрантов зависит от предпочтений патоморфолога, на которое влияют удобство и простота исследования больших срезов и технические проблемы получения и хранения препаратов нестандартного размера. Единственным существенным отличием в методике получении препаратов при использовании этих двух подходов является то, что требуется более толстая нарезка целой ПЖ. Кроме того, выполнение ИГХ требует обычно большего количества реагента и может выполняться только вручную [13].
МЕТОДИКА ИССЛЕДОВАНИЯ МАКРОПРЕПАРАТА ПОСЛЕ РП В СЛУЧАЕ pT0
Если при исследовании микропрепаратов патоморфолог не находит РПЖ, рекомендуется следующее: если ПЖ не была залита в парафин полностью, то рекомендуется это выполнить; если ПЖ была полностью залита в парафин, для оценки локализации опухоли необходимо пересмотреть микропрепараты после биопсии. Необходимо перерезать участки препарата после РП в этой зоне после переворачивания блока.
Для обнаружения т.н. “минимального остаточного рака”, особенно у больных, получавших до операции неоадъювантную гормональную терапию можно выполнить иммуногистохимическое исследование с антителом против CAM 5,2 [14].
ЗАКЛЮЧЕНИЕ ПО ПРЕПАРАТУ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
Полное и четкое заключение патоморфолога по удаленному в ходе РП препарату ПЖ весьма важно для выработки оптимальной тактики лечения больного. Заключение должно содержать клинически значимую информацию, полученную на основании макро- и микроскопического исследований препарата после РП. Основное внимание должно уделяться оценке факторов прогноза, включенных Коллегией Американских Патологов (College of American Pathologists) в категории 1 и 2 (табл. 1) [6]. Эти факторы с доказанной прогностической значимостью и используемые в лечении больного, включают гистологический тип опухоли, степень дифференцировки, объем рака, степень местной распространенности и стадию РПЖ а также состояние краев резекции. Также могут использоваться и другие изученные биологические и клинические факторы, прогностическая значимость которых еще не подтверждена в крупных исследованиях.
Гистологический тип РПЖ. Гистологическая классификация РПЖ представленная в табл. 2 [15]. Более 95% от всего РПЖ имеют типичное строение ацинарной аденокарциномы. В последние годы были описаны несколько новых и необычных гистологических вариантов РПЖ. Эти варианты представляют собой спектр изменений, которые могут происходить в аденокарциноме и должны указываться в морфологическом заключении, если обнаруживаются в препарате. Кроме того, существует ряд опухолей ПЖ, например, переходно-клеточный, плоскоклеточный, базалоидный и аденокистозный раки, биологическое поведение и методы лечения которых существенно отличаются от типичного РПЖ, что делает точную диагностику типа опухоли крайне важной для определения тактики лечения больного.
Степень дифференцировки (степень злокачественности). Наиболее значимым предиктором прогрессирования РПЖ после РП является сумма Глисона, определенная в препарате после РП (табл. 3) [16–19]. Система Глисона является методикой выбора при определении степени злокачественности опухоли, использовать термины “высокодифференцированный”, “умереннодифференцированный” и “низкодифференцированный” для определения степени злокачественности РПЖ не рекомендуется [6]. Сумма Глисона состоит из двух слагаемых: первичного (наиболее распространенного) и вторичного (второй по распространенности) показателей Глисона (Gleason grade). Если в препарате не выявляется вторичный показатель Глисона, то для получения сумы Глисона первичный показатель Глисона удваивается. Первичный и вторичный показатели Глисона должны указываться в скобках после указания суммы Глисона (например: сумма Глисона 7 (3 + 4)). Для группировки суммы Глисона в категории с целью обобщения результатов лечения и т.д., рекомендуется следующая группировка (табл. 4): 2-5, 6, 7, 8-10, или 2-6, 7, 8-10.
Если в препарате после РП идентифицируется две или более отдельных опухоли, можно указывать суммы Глисона каждой опухоли либо должна быть указана сумма Глисона наиболее значительной опухоли. Например, если имеется большая опухоль в переходной зоне ПЖ с суммой Глисона 5 и отдельная меньшая опухоль в периферической зоне с суммой Глисона 7, то должны указываться обе суммы Глисона или по меньшей мере сумма Глисона последней опухоли, а не усредненное значение суммы Глисона.
Из-за большего количества опухоли в препарате после РП, доступной для исследования, (в отличие от биопсийного материала), часто возможна ситуация, когда в опухоли обнаруживается более двух показателей Глисона (Gleason grade), т.е. имеется третичный показатель Глисона. Поскольку оригинальная система Глисона учитывает только первичный и вторичный показатели Глисона, в подходе к оценке степени злокачественности при опухолях с третичным показателем Глисона имеются разногласия, несмотря на то, что наличие третичного показателя Глисона влияет на прогноз. Так, частота прогрессирования РПЖ с суммой Глисона 5-6 и третичным показателем 4 почти такая же, как и при опухолях с суммой Глисона 7. В свою очередь опухоли с суммой Глисона 7 и третичным показателем 5 ведут себя как опухоли с суммой Глисона 8. С другой стороны таких различий не наблюдается при РПЖ с суммой Глисона 8 и третичным показателем 5, по-видимому вследствие небольшого количества больных с такой патологией а также настолько неблагоприятного прогноза при РПЖ с суммой Глисона 8, что присутствие третичного показателя 5 существенно не может его ухудшить [20].
Другим дискутабельным вопросом при определении степени злокачественности является вопрос об определении суммы Глисона в опухолях, состоящих на 95% из одного типа по Глисону, в которых имеется только небольшое количество более низкодифференцированной опухоли. Например, опухоль ПЖ, содержащую > 95% опухолевой ткани с показателем Глисона 3 и
Операция по удалению меланомы
Меланома – одна из самых опасных злокачественных опухолей. Она характеризуется агрессивным ростом и ранним метастазированием. Тем не менее, если «злокачественная родинка» вовремя диагностирована, ее можно удалить и вылечить человека. На поздних стадиях проводят паллиативные хирургические вмешательства, которые помогают улучшить состояние пациента, справиться с симптомами.
Широкое иссечение
Если по результатам биопсии диагностирована меланома, она должна быть полностью удалена. Хирург иссекает опухоль и некоторое количество здоровой ткани вокруг нее, под ней. Нормальные ткани захватывают для того, чтобы полностью удалить все опухолевые клетки.
После хирургического удаления меланому кожи отправляют для анализа в лабораторию. Важно проверить край резекции – участок ткани, который находится в месте разреза. Если здесь обнаружена только здоровая ткань, то край резекции негативный, это означает, что опухоль удалена полностью. Если в крае резекции обнаружены злокачественные клетки, то его называют позитивным. Это говорит о том, что опухолевая ткань, вероятно, удалена не полностью.
Чем больше здоровой ткани хирург захватил во время операции, тем выше вероятность того, что край резекции окажется негативным. Но в некоторых местах, например, на лице, важен косметический эффект. В таких случаях нужно искать золотую середину: постараться удалить как можно меньше окружающих здоровых тканей, но так, чтобы иссечь меланому полностью и не оставить опухолевых клеток в коже. После операции врач может назначить курс адъювантной химиотерапии. В некоторых случаях, если меланома находится на руке или на ноге, проводят ампутацию. Можно ли выполнить лазерное удаление меланомы? Лазерную хирургию широко применяют для удаления родинок, но при меланоме она зачастую не дает каких-либо преимуществ. Меланома – потенциально смертельное заболевание, это хирургическая патология, и в большинстве случаев ее нужно иссекать скальпелем. Чаще всего операцию проводят под местной анестезией. Одно из возможных последствий удаления меланомы лазером состоит в том, что может просто не остаться материала для биопсии, вся ткань опухоли будет уничтожена лазером. Лазерную хирургию иногда применяют на ранних стадиях опухоли, как правило, у пожилых людей.
Иссечение лимфатических узлов
После того как подтвержден диагноз меланомы, нужно проверить близлежащие к опухоли (их называют регионарными) лимфатические узлы – возможно, опухолевые клетки успели в них распространиться. Проводят компьютерную томографию, МРТ, ПЭТ-сканирование, тонкоигольную биопсию лимфоузлов. Если они тоже поражены, их иссекают.
Если по данным обследования регионарные лимфоузлы не поражены, можно провести сентинель-биопсию, или биопсию сигнального лимфатического узла. В область меланомы вводят радиофармпрепарат или флуоресцентный краситель.
Он проникает в лимфатические сосуды и распространяется по ним в лимфоузлы. Лимфатический узел, в который краситель попадает в первую очередь, называется сигнальным. Его удаляют и проводят биопсию.
Если в нем обнаруживают злокачественные клетки, то они, скорее всего, успели распространиться и в другие регионарные лимфоузлы. Сентинель-биопсия особенно полезна в случаях, когда меланома толще 1 мм.
В настоящее время неизвестно, можно ли вылечить пациента, удалив пораженные меланомой лимфоузлы. По крайней мере, это помогает продлить жизнь, уменьшить боль и другие симптомы.
Паллиативная хирургия при меланоме с метастазами
На ранней стадии возможно полное удаление меланомы. Даже если поражены регионарные лимфатические узлы, все еще остаются шансы на ремиссию. Если же обнаружены отдаленные метастазы, лечение может носить лишь паллиативный характер. Оно направлено на облегчение симптомов и продление жизни, но не на излечение.
Есть ли шанс вылечить больного, если у него только 1–2 метастаза, которые можно удалить хирургически? Если во время компьютерной томографии или МРТ обнаружен всего один метастаз, скорее всего, есть и другие, просто они очень малы, и их не удалось выявить. Шансы на ремиссию очень малы.
Тем не менее, хирургическое лечение все еще может помочь. Хирург может удалить некоторые метастазы, чтобы улучшить работу пораженных органов, устранить симптомы, увеличить продолжительность жизни больного.
На поздних стадиях на первый план выходят другие, нехирургические, методы лечения. Например, выживаемость помогают сильно увеличить иммунопрепараты из группы ингибиторов контрольных точек.
Последствия удаления меланомы
Возможные последствия хирургических вмешательств у пациентов с меланомой:
Цена удаления меланомы в Москве
Стоимость зависит от многих факторов: объема операции, исследований, которые могут потребоваться пациенту, ценовой политики клиники, опыта, квалификации и статуса хирурга, дополнительных методов лечения до и после операции.
Мы сотрудничаем с лучшими онкологическими центрами в Москве, в которых выполняются операции по удалению меланом на спине, лице и других частях тела. Мы порекомендуем хорошую клинику, в которой можно получить лечение при меланоме 4 стадии:
Края резекции негативные что такое
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
Московский научно-исследовательский онкологический институт им. П.А. Герцена, Москва
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Состояние краев резекции при органосохраняющих операциях по поводу рака молочной железы
Журнал: Онкология. Журнал им. П.А. Герцена. 2015;4(6): 65-73
Зикиряходжаев А. Д., Ермощенкова М. В., Волченко Н. Н., Сухотько А. С., Фетисова Е. Ю., Рассказова Е. А., Тыщенко Е. В. Состояние краев резекции при органосохраняющих операциях по поводу рака молочной железы. Онкология. Журнал им. П.А. Герцена. 2015;4(6):65-73.
Zikiryakhodzhaev A D, Ermoshchenkova M V, Volchenko N N, Sukhot’ko A S, Fetisova E Iu, Rasskazova E A, Tyshchenko E V. Resection margin status during organ-sparing surgery for breast cancer. P.A. Herzen Journal of Oncology. 2015;4(6):65-73.
https://doi.org/10.17116/onkolog20154665-73
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Цель — изучить данные разных авторов о вариантах хирургических краев резекции молочной железы при органосохраняющих операциях по поводу рака, разработать показания к методике определения абластичности операции. Материал и методы. Представлены данные из различных рандомизированных и описательных исследований. Изучены зависимость развития рецидива от состояния краев резекции, 10-летняя частота рецидивов рака молочной железы при различных состояниях краев резекции по данным международных онкологических центров. Рассмотрены взаимосвязь состояния краев резекции и выживаемости, методики забора материала для исследования краев резекции, причины ложной позитивности краев резекции, частота встречаемости позитивности краев резекции и ширина резекции при органосохраняющих операциях, алгоритм хирургической тактики в зависимости от состояния краев резекции, причины для принятия решения о реоперации при позитивных или «тесных» краях резекции с целью локального контроля и эстетического результата. Результаты и выводы. Реоперация строго необходима пациенткам моложе 40 лет, при распространенной DCIS, лимфоваскулярной инвазии, отсутствии системной терапии, нескольких позитивных краях резекции, отсутствии данных о краях резекции, «тесных» краях резекции и наличии отрицательных прогностических факторов. При органосохраняющих операциях необходима адекватная ширина резекции (не менее 10 мм) для минимизации риска местных рецидивов, улучшения общей и безрецидивной выживаемости.
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
Московский научно-исследовательский онкологический институт им. П.А. Герцена, Москва
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Хирургический метод является основным в комплексном лечении рака молочной железы (РМЖ) [1—4]. Органосохраняющее лечение больных при ранних стадиях РМЖ с последующим проведением лучевой терапии на молочную железу и лекарственной терапии становится стандартным подходом при соблюдении критериев отбора [2].
Широкое внедрение маммографического скрининга позволило выявлять опухоли малого размера и способствовало внедрению органосохраняющего лечения [5]. Последнее стало возможно благодаря более раннему выявлению болезни, осознанию того, что расширение объема операции не приводит к улучшению выживаемости больных, применению лучевого воздействия на сохраненную молочную железу и, как следствие, снижению вероятности местного рецидива, а совершенствование комплексной и комбинированной терапии при РМЖ с учетом прогностических факторов привело к возможности применять органосохраняющие операции у значительного числа пациенток [4, 6, 7]. Этому способствует также контроль радикальности операции путем исследования краев резекции на наличие опухолевых клеток [3].
Лучше сделать мастэктомию, чем несоответствующую онкологическим критериям органосохраняющую операцию. Противопоказаниями к органосохраняющим операциям являются: размер опухоли более 3 см (относительное противопоказание, так как после проведения НАПХТ с целью уменьшения размеров опухоли можно выполнить органосохраняющую операцию); мультицентрический рост опухоли; III—IV стадия РМЖ; медицинские противопоказания к проведению лучевой терапии [8]. Основными критериями при выполнении органосохраняющих операций являются соотношение диаметра опухоли и размера молочной железы, состояние подмышечных лимфатических узлов, гистологическая оценка чистоты краев резецируемого участка железы с опухолью, возможность проведения послеоперационной лучевой терапии, оценка необходимости предоперационного лечения. Чистота краев резекции — главный показатель адекватности органосохраняющей операции [4, 9—13]. Один из главных факторов развития местного рецидива после органосохраняющих операций у больных РМЖ является состояние краев резекции [9, 10, 14, 16, 17]. Стандартной является хирургическая практика добиваться чистых краев резекции путем повторного иссечения [3, 15]. В настоящее время широкое внедрение в практику получили онкопластические радикальные резекции. Данный термин подразумевает резекцию молочной железы по поводу рака с использованием методов пластической хирургии для восстановления формы молочной железы, в большинстве случаев с одномоментной коррекцией контралатеральной молочной железы (рис. 1).

Возможная необходимость последующей мастэктомии в случае позитивных краев резекции и отсутствие онкологических и положительных эстетических результатов после онкопластической операции требует интраоперационного исследования краев резекции.
Края резекции — это участки ткани молочной железы рядом с разрезом. При гистологическом исследовании выдают следующие заключения: края позитивны — раковые клетки обнаруживаются в краях иссеченных тканей; края негативны — раковые клетки не обнаруживаются в краях иссеченных тканей (в пределах 1 мм и менее от края опухоли); края «тесные» («закрытые») — промежуточная ситуация (опухоль в пределах 1 мм и менее от края опухоли). При изучении препарата следует указать макроскопическое и микроскопическое расположение опухоли от края [18]. Препараты готовят таким образом, чтобы можно определить расстояние от края опухоли до границы хирургического препарата, т. е. ширину резекции, которая определяет риск рецидива. Диапазон, дискутируемой разными авторами, ширины резекции колеблется от 1 до 10 мм. Однако при ширине резекции 5 мм 30% больных подлежат ререзекции [19—27].
Края резекции необходимо помечать красителями, маркировка дает точный ответ с какой именно стороны в молочной железе остались опухолевые изменения. Большинство онкологов исследуют ближайший край резекции, но есть сообщения об изучении края с 6 сторон: спереди и сзади, сверху и снизу, слева и справа, а также с 9 сторон.
При изучении базы данных Henrietta Banting Breast Centre в 1987—1997 гг. выделено 1430 пациенток, которым была выполнена лампэктомия по поводу инвазивного РМЖ: 1225 пациенток (группа A) имели негативные края резекции, 152 (группа B) перенесли одну или более резекций до достижения негативных краев, у 53 (группа C) были позитивные края после хирургического вмешательства и ререзекция им не выполнялась. При анализе безрецидивной выживаемости не было получено статистически достоверных различий между группами, А и В, отмечено повышение частоты местных рецидивов в группе С [3, 19].
Разными авторами в онкологических центрах изучалась частота развития рецидивов в зависимости от состояния краев резекции при органосохраняющих операциях по поводу РМЖ (табл. 1, 2).


По данным M. Lagios и соавт. увеличение ширины краев резекции от 1 до 10 мм приводит к снижению частоты местного рецидивирования практически в 5 раз (от 42 до 8,3%). M. Silverstein утверждает, что при достаточной ширине резекции (10 мм и более) размер опухоли и степень гистологической злокачественности практически не влияют на риск развития местного рецидива [21].
В.Ф. Семиглазов и соавт. [22] также представил данные различных авторов, которые установили, что «близкие» края по сравнению с широкими чистыми краями не оказывают никакого влияния на показатели безрецидивной выживаемости. Эта неопределенность побудила многих хирургов выполнять повторные резекции при «близких» краях в целях снижения угрозы местного рецидива (или улучшения показателей безрецидивной выживаемости). Указанные диапазоны местных рецидивов в течение 5 лет при чистых, близких и позитивных краях составили 2—3, 2—8 и 10—25% соответственно [23]. Также представлены результаты метаанализа 21 исследования по изучению взаимосвязи между состоянием краев резекции и исходом органосохраняющего лечения у пациенток при инвазивном РМЖ [24]. По результатам работы увеличение ширины края резекции имеет слабую взаимосвязь с риском местного рецидива, эффект улучшается, когда вносятся коррективы в адъювантной гормональной и лучевой терапии. Авторы приходят к выводу, что выбор широких краев резекции по сравнению с более узкими для достижения чистых краев резекции не имеет дополнительного преимущества при долгосрочном местном контроле после органосохраняющего лечения.
Сложности могут возникнуть при определении краев резекции при раке in situ ductale молочной железы. Для проведения органосохраняющих операций при раке in situ необходимы следующие условия:
2) ширина краев резекции должна быть не менее 10 мм;
3) степень гистологической злокачественности должна быть низкой или промежуточной, хотя некоторые исследователи считают, что пациентки с DCIS высокой степени гистологической злокачественности могут быть кандидатами для сохранных операций, если есть возможность отступить от края опухоли на 10 мм и более;
4) молочная железа должна выглядеть после операции эстетично. Если этого добиться невозможно, предпочтительно выполнить мастэктомию с последующей реконструкцией молочной железы [21].
Клинические признаки минимальной опухоли или маммографически определяемые очаги микрокальцинации не всегда отражают действительные границы образования. В результате при DCIS в 40% случаев требуется повторная операция из-за вовлечения краев резекции в опухолевый процесс. Поэтому для достижения адекватной радикальной резекции сложно точно определить истинную распространенность опухоли по протокам и необходимую ширину резекции [21].
Количество оперативных вмешательств с позитивными краями резекции, по данным рандомизированных и описательных исследований международных онкологических центров, представлено в табл. 3.

По данным ретроспективного анализа 607 случаев РМЖ у 583 пациенток, проходивших лечение в US-центре в 1980—1996 гг., установили, что общая и безрецидивная выживаемость ассоциированы с состоянием краев резекции (р=0,0032 и р 
В настоящее время нет единого мнения в отношении состояния краев резекции при хирургическом лечении РМЖ. Многих российских и зарубежных авторов интересовало, когда будут адекватные края резекции — при радикальных мастэктомиях, в которых может отсутствовать необходимость, при многочисленных повторных операциях после органосохраняющих операций или в излишне обширных резекциях (Monica Morrow) [28, 50].
В Ohio State Uniersity, Columbus, США с августа 2003 г. по июнь 2007 г. проведен ретроспективный анализ 204 органосохраняющих операций, при которых выполнено исследование 9 краев резекции молочной железы: superior, superior-medial, superior-lateral, medial, lateral, inferior, inferior-medial, inferior-lateral, deep-posterior. 6,4% (13/204) имели позитивные края резекции, 4,4% (9/204) — «тесные» поля (опухоль в пределах 1 мм или меньше от края резекции), 11,8% (24/204) имели повторную резекцию края, содержащего опухолевые клетки, 7,1% (13/182) — негативные края резекции (нет опухолевых клеток в пределах 1 мм и менее от края опухоли). Методика взятия материала для исследования краев резекции при органосохраняющих операциях заключалась в заборе фрагментов прямоугольной формы после удаления сектора с опухолью из 9 стандартных участков (рис. 2—4) в области краев резекции с помощью изогнутых ножниц или скальпеля без использования электрокоагулятора.



У 164 пациенток расстояние от опухоли до края резекции составляло в среднем 0,79 см (от 0,16 до 2,00 см — негативные края резекции), при 0,05 см (от 0,01 до 0,09 см — «тесные» края резекции). Из 204 случаев органосохраняющих операций 24 имели позитивные края в одном или из более 9 стандартных образцов, взятых с краев резекции молочной железы: 15 пациенток имели 1 позитивный край, 2 — 2 позитивных края, 5 — 3 позитивных края, 1 — 4 позитивных края и 1 — 5 позитивных краев. Таким образом, было обнаружено 43 позитивных края из всех 1836 резецированных краевых образцов.
У всех пациенток с несколькими позитивными краями резекции предприняты повторные хирургические вмешательства на молочной железе, за исключением 1 больной, которая отказалась от дальнейшего лечения.
Наличие негативных краев резекции и дополнительная ререзекция в области позитивных краев не гарантируют отсутствие последующего развития рецидива [29].
Так, в 1994 г. D. England и соавт. [30] сообщили о развитии в 9,6% (5/52) случаев в ложе опухоли, где после обнаружения позитивных краев резекции была выполнена широкая локальная эксцизия. В 1998 г. N. Beck и соавт. [31] сообщили о рецидиве в 13,3% (14/105) случаев у пациенток с негативными краями резекции после широкой локальной эксцизии опухоли. А. Jenkinson и соавт. [32] сообщили о рецидиве у 6% (5/83) пациенток с исходными негативными краями резекции при «частичной мастэктомии». М. Keskek и соавт. [33] выявили 4,3% (13/303) рецидивов у пациенток с негативными краями резекции. D. Cao и соавт. [34] отметили 8,7% (2/23) рецидивов в области ранее негативных краев резекции после лампэктомии. Т. Huston и соавт. [35] описали 6,4% (3/26) рецидивов в зоне лампэктомии при ранее негативных краях резекции. I. Tengher-Barna и соавт. [36] сообщили о 10,3% (11/107) рецидивов после лампэктомии и негативных краев резекции. J. Hewes и соавт. [37] отметили 8,6% (82/957) рецидивов после регистрации негативных краев резекции.
Существуют различные методики забора материала для исследования краев резекции: выборочная — «selective cavity margin sampling» technique (исследование до 6 краев резекции) [30, 38—46]; полная — «complete cavity margin re-excision» technique [31, 33, 47, 48]; методика полного непрерывного иссечения ткани в виде оболочки в полости удаленной ткани и опухоли [47, 48]; методика иссечения ткани по краям резекции в виде кольца [31]; методика удаления стенок всей полости в виде 4 образцов [33].
Недостаток полной эксцизии краев резекции — возможность косметического дефекта.
Продолжает оставаться спорным вопрос о срочном интраоперационном исследовании краев резекции. Нет общего мнения насколько эффективно выполнение интраоперационного исследования краев резекции и интраоперационной немедленной реэксцизии краев резекции, которые являются суспициозными. Основная оценка основана на визуальном осмотре участков молочной железы в зоне операции, поверхностном осмотре резецированной поверхности окрашенного, нефиксированного, разрезанного тканевого образца. Многие авторы рекомендуют рассмотрение других возможных методов для интраоперационной оценки хирургических краев резекции, чтобы попытаться уменьшить вероятность последующей реэксцизии у пациенток, перенесших операцию на молочной железе [29]. Имеются данные об использовании радиочастотной спектроскопии [49], рентгенологического исследования, маркированного клипсами и проводниками препарата.
Существует две основные методики забора материала для исследования краев резекции [29]:
1. Методика «касательного (тангенциального) срезания краев — поверхность самого препарата молочной железы срезается или пилингуется, тонкие тканевые фрагменты помещают в специальные кассеты и используют для микроскопической оценки. Присутствие любых опухолевых клеток в пределах осмотренного фрагмента является основанием для интерпретации краев резекции положительными. В связи с выделением фрагментов по касательной линии измерение действительного расстояния между опухолью и краем хирургической резекции не может быть точно определено. Главное преимущество этой методики заключается в том, что общая площадь основного периферического края препарата микроскопически осматривается значительно больше.
2. Методика перпендикулярных краев — получают перпендикулярные секции вдоль всей длинной оси препарата молочной железы. Очевидно предоставление ограниченной выборки краевой поверхности препарата. Оценка хирургического края возможна в меньшей фракции от всей площади поверхности препарата. Эта методика необходима при наличии микроскопически выявленных опухолевых клеток в маркированном крае перпендикулярной секции (позитивном крае резекции). Главное преимущество методики перпендикулярных краев — взаимосвязь и точность измерений расстояния между опухолью и краем резекции в самом препарате могут быть микроскопически оценены.
Основная причина ложной позитивности краев резекции связана с образцом ткани [29, 37, 42, 50—52]:
1) нарушения методики обычной обработки и окрашивания в патологоанатомическом отделении: использование большого количества чернил, так же как и любое давление в процессе их нанесения на свежие образцы; при удалении лишнего количества чернил (т.е. «blotting dry») с поверхности свежих образцов они могут попасть в потенциальные места, которые не являются репрезентативными, но могут быть взяты для оценки и привести к ложноположительным результатам; применение чернил на рыхлых и дольчатых поверхностях свежих образцов ткани и измененных тканях в процессе сжатия может привести к попаданию чернил в эти искусственные расщелины и потенциальные пробелы;
2) сжатие образца при маммографии препарата (может привести к искусственному закрытию или ложной позитивности краев);
3) любое сжатие свежих образцов может создавать искусственные неровности, истончение ткани и переориентацию вышележащей фиброзно-жировой ткани и ткани молочной железы, покрывающих опухолевую поверхность, что может привести к снижению фактического расстояния между поверхностью свежих образцов и поверхностью опухоли.
Повышение квалификации лиц, участвующих в транспортировке образцов, маммографической оценке, подготовке препаратов в патологоанатомическом отделении может помочь уменьшить частоту ложной позитивности краев [29].
S. Povoski и соавт. [29] представили подробные характеристики 9 стандартных повторно резецированных краев по результатам гистологического исследования препаратов 204 случаев РМЖ (табл. 5, 6, 7, 8, 9).





Американским обществом хирургов-маммологов был предложен алгоритм хирургической тактики в зависимости от состояния краев резекции [53] (рис. 5).

Согласно рекомендациям Национальной всеобщей онкологической сети (National Comprehensive Cancer Network — NCCN) можно не выполнять реэксцизию краев, если вовлечены передние и задние края, а лежащие в основе мышечная фасция и кожа были удалены. Ширина резекции менее 1 мм считается неадекватной (NCCN, 2013).
Факторы, которые следует учитывать при принятии решения о реоперации при позитивных или «тесных» краях резекции (с целью локального контроля)
I. Характеристика больной:
1) возраст (молодой возраст менее 35 лет увеличивает риск рецидива);
2) наследственная предрасположенность (мутации генов BRCA увеличивают риск);
3) сопутствующие заболевания (противопоказания к лучевой и лекарственной терапии).
II. Характеристика опухоли:
2) степень злокачественности;
3) лимфоваскулярная и периневральная инвазия;
4) внутрипротоковый компонент;
5) состояние регионарных лимфатических узлов;
6) края резекции (позитивные с негативными, «тесные» с негативными);
7) молекулярно-биологические особенности опухоли.
1) дозы и объем лучевой терапии;
2) лекарственная терапия;
3) количество удаленных лимфатических узлов;
4) объем хирургического вмешательства (органосохраняющая операция или радикальная мастэктомия).
1) соотношение объема молочной железы и опухоли;
2) индекс массы тела больной;
3) размер молочной железы;
5) сопутствующие заболевания.
II. Хирургическое лечение:
1) иссечение кожи над образованием;
2) направление и длина разрезов;
3) объем перемещаемых тканей молочной железы;
5) количество реопераций;
6) объем и вид первичной операции;
7) объем и вид предстоящей операции.
III. Лучевая терапия:
1) общая доза облучения;
2) доза буста и техника;
3) вид лучевой терапии;
4) продолжительность лучевой терапии.
С учетом рекомендаций BCCA [20], реоперация строго необходима пациенткам в возрасте менее 40 лет, при распространенной DCIS, лимфоваскулярной инвазии, отсутствии системной терапии, нескольких позитивных краях резекции, отсутствии данных о краях резекции.
1. Различные методики исследования краев резекции позволяют точно оценивать адекватность органосохраняющих операций при раке молочной железы, отобрать пациенток для повторной резекции с целью минимизации риска местных рецидивов, а также выделить пациенток, которым необходимо расширение операции до мастэктомии.
2. При органосохраняющих операциях необходима оценка состояния краев резекции, чтобы выбрать наиболее адекватную тактику ведения в каждом конкретном случае и снизить нагрузку на пациенток и медицинских работников при лечении рецидивов.
3. Нет единого мнения относительно того, что считать адекватными краями резекции.
4. При позитивных и «тесных» краях резекции отмечено увеличение риска местного рецидива и ухудшение прогноза заболевания.
5. Пациентки, которым выполнены ререзекции до достижения негативных краев, имеют такой же прогноз как пациентки с изначально негативными краями.
6. При положительных и «тесных» краях резекции и наличии отрицательных прогностических факторов показана реоперация.
7. Необходима адекватная ширина резекции при органосохраняющих операциях (не менее 10 мм) для минимизации риска местных рецидивов, улучшения общей и безрецидивной выживаемости.