Кровоток антеградный что это
Антеградный диастолический ток крови и классический рефлюкс при варикозном расширении межсафенной вены
1) Институт экспериментальной медицины,
2) НУЗ ООО «medalp», Санкт-Петербург,
3) НУЗ ООО «Аксон», Выборг, Россия
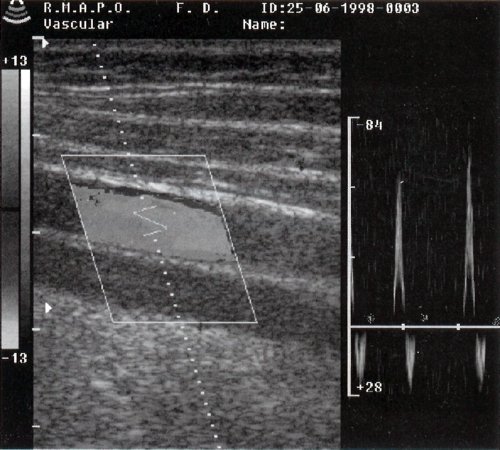
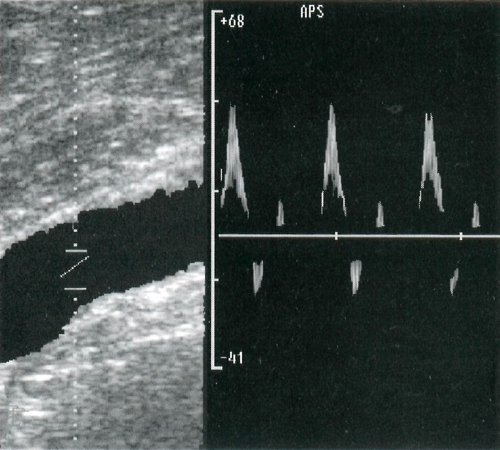
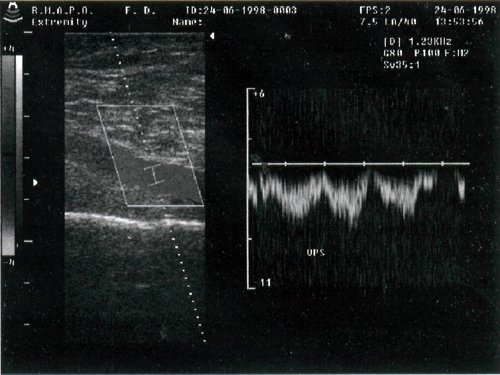
Введение. В межсафенной вене (МВ) может иметь место так называемый «антеградный» или «парадоксальный» рефлюкс. Этот ток крови выявляется у ряда больных в период мышечной диастолы и является звеном патогенеза варикозной болезни, но имеет, в отличие от «классического» рефлюкса, антеградное направление. Источником антеградного диастолического тока крови (АДТК) по МВ является несостоятельное сафенопоплитеальное соустье (СПС). Описания возможных вариантов нарушений кровотока по МВ разрозненны, их трактовки противоречивы. Распространенность и патогенез этих нарушений не изучены.
Материалы и методы. Поперечное исследование: за 4 года в трех центрах обследовано 1 413 пациентов с диагнозом варикозное расширение вен класса С2–С6 по классификации СЕАР. Всем пациентам проводилось УЗДС вен нижних конечностей. АДТК определялся как однонаправленный антеградный ток крови, длительностью более 0,5 секунды, наблюдавшийся после освобождения голени от компрессии (в диастолу). Из пациентов, включенных в исследование, у которых не было варикозного расширения вен на контралатеральной конечности и при этом лоцировалась МВ, было последовательно отобрано 40 в группу контроля для анализа кровотока и диаметра МВ в норме.
Результаты. На 61 (4,8%) из 1 265 включенных в исследование конечностей выявлены нарушения кровотока в МВ: «классический» рефлюкс на 9 (14,8%) конечностях, АДТК выявлен на 37 (60,7%), сочетание «классического» и АДТК на 15 (24,6%). Таким образом, пациенты были разделены на три группы.
При исследовании характера кровотока по МВ в группе контроля на 40 нижних конечностях нарушений кровотока не выявлено. Средний диаметр МВ составил 1,68 мм (МЕ=1 мм). Диаметр МВ был значительно больше во всех исследуемых группах по сравнению с контрольной (p

ISSN: 1027-6661 (Print)
Ангиология и сосудистая хирургия » созданное автором по имени Покровский Анатолий Владимирович, публикуется на условиях лицензии Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Основано на произведении с http://www.angiolsurgery.org/magazine/.
Разрешения, выходящие за рамки данной лицензии, могут быть доступны на странице http://www.angiolsurgery.org/contacts/.—>
Российское Общество ангиологов и сосудистых хирургов © 2014
117997, Москва, ул. Б.Серпуховская, 27
Допплеросонография периферических сосудов. Часть I (опыт применения УЗИ сканеров фирмы «Медисон» в скрининговых исследованиях)
Введение
В современной функциональной диагностике для исследования сосудов все шире применяются ультразвуковые методики. Это связано с ее относительно низкой стоимостью, простотой, неинвазивностью и безопасностью исследования для больного при достаточно высокой информативности по сравнению с традиционными рентген-ангиографическими методиками. Последние модели ультразвуковых сканеров фирмы MEDISON позволяют провести высококачественное обследование сосудов, с успехом диагностировать уровень и протяженность окклюзирующих поражений, выявлять аневризмы, деформации, гипо- и аплазии, шунты, клапанную недостаточность вен и другую патологию сосудов.
Для проведения сосудистых исследований необходим УЗ-сканер, работающий в дуплексном и триплексном режимах, набор датчиков (таблица 1) и пакет программ для сосудистых исследований.
Исследования, приведенные в данном материале, проведены на ультразвуковом сканере SA-8800 «Digital GAIA» (фирма «Medison» Ю. Корея) во время скрининга среди пациентов, направленных на УЗ-обследование других органов.
Технология УЗИ сосудов
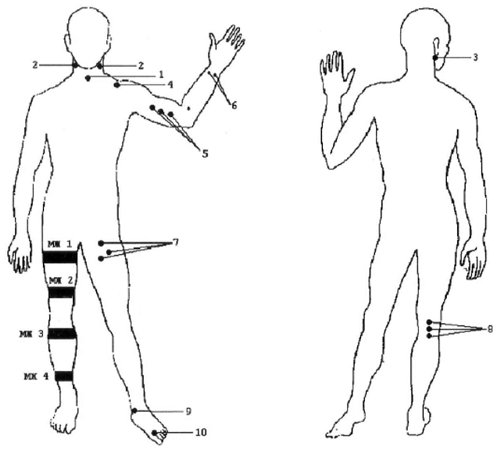
Датчик устанавливают в типичной области прохождения исследуемого сосуда (рис. 1).
Рис. 1. Стандартные доступы при допплеросонографии периферических сосудов. Уровни наложения компрессионных манжет при измерении регионального САД.
Для уточнения топографии сосудов проводят сканирование в плоскости, перпендикулярной анатомическому ходу сосуда. При поперечном сканировании определяют взаиморасположение сосудов, их диаметр, толщину и плотность стенок, состояние периваскулярных тканей. Воспользовавшись функцией и обведя внутренний контур сосуда, получают площадь его эффективного поперечного сечения. Далее производят поперечное сканирование вдоль исследуемого сегмента сосуда для поиска участков стенозирования. При выявлении стенозов используют программу для получения расчетного показателя стеноза. Затем проводят продольное сканирование сосуда, оценивая его ход, диаметр, внутренний контур и плотность стенок, их эластичность, активность пульсации (с использованием М-режима), состояние просвета сосуда. Измеряют толщину комплекса интима-медиа (по дальней стенке). Проводят допплеровское исследование в нескольких участках, перемещая датчик вдоль плоскости сканирования и осматривая возможно больший участок сосуда.
Оптимальной является следующая схема допплеровского исследования сосудов:
Расчет скоростных характеристик потоков в режиме импульсной допплерографии возможен при скорости потока не более 1-1,5 м/сек (Nyquist limit). Для получения более точного представления о распределении скоростей необходимо установить контрольный объем не менее 2/3 просвета исследуемого сосуда. Используются программы при исследовании сосудов конечностей и при исследовании сосудов шеи. Работая в программе, отмечают название соответствующего сосуда, фиксируют значения максимальной систолической и минимальной диастолической скоростей, после чего производят обводку одного комплекса. После проведения всех этих измерений можно получить отчет, включающий значения V max, V min, V mean, PI, RI для всех обследованных сосудов.
Количественные допплеросонографические параметры артериального кровотока
PI, RI важно использовать вместе, т.к. они отражают разные свойства кровотока в артерии. Использование лишь одного из них без учета другого может быть причиной диагностических ошибок.
Качественная оценка допплеровского спектра
Выделяют ламинарный, турбулентный и смешанный типы потока.
Турбулентный тип кровотока характерен для мест стеноза или неполных окклюзий сосуда и характеризуется отсутствием «спектрального окна» на допплерограмме. При ЦДК выявляется мозаичность окрашивания, в связи с движением частиц в разных направлениях.
Смешанный тип кровотока может в норме определяться в местах физиологических сужений сосуда, бифуркациях артерий. Характеризуется наличием небольших зон турбулентности при ламинарном потоке. При ЦДК выявляется точечная мозаичность потока в области бифуркации или сужения.
В периферических артериях конечностей выделяют также следующие типы кровотока на основании анализа огибающей кривой допплеровского спектра.
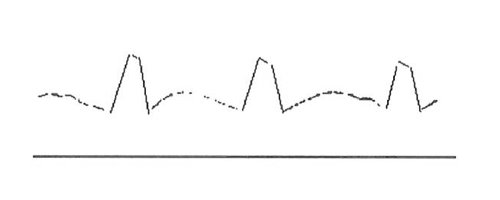
Коллатеральный тип кровотока также регистрируется ниже места окклюзии. Он проявляется близкой к монофазной кривой со значительным изменением систолического и отсутствием ретроградного и второго антеградного пиков (рис. 2в).
Рис. 3. Отличие огибающих допплерограмм НСА (а) и ВСА (б).
Рис. 4. Варианты магистрального типа кровотока в артерии. Продольное сканирование. ЦДК. Допплерография в импульсном режиме.
Исследование сосудов шеи
Датчик устанавливают поочередно на каждой стороне шеи в области грудино-ключично-сосцевидной мышцы в проекции общей сонной артерии. При этом визуализируются общие сонные артерии, их бифуркации, внутренние яремные вены. Оценивают контур артерий, их внутренний просвет, измеряют и сравнивают диаметр с обеих сторон на одном уровне. Чтобы отличить внутреннюю сонную артерию (ВСА) от наружной (НСА), используют следующие признаки:
При исследовании позвоночных артерий датчик ставят под углом 90° к горизонтальной оси, либо непосредственно над поперечными отростками в горизонтальной плоскости.
По программе Carotid рассчитывают Vmax (Vpeak), Vmin (Ved), Vmean (TAV), PI, RI. Сравнивают показатели, полученные с противоположных сторон.
Исследование сосудов верхних конечностей
Исследование вен нижних конечностей. Проводится одновременно с исследованием одноименных артерий либо как самостоятельное исследование.
Исследование бедренной вены проводится в положении больного на спине с несколько разведенными и ротированными кнаружи ногами. Датчик устанавливается в области паховой складки параллельно ей. Получают поперечный срез бедренного пучка, находят бедренную вену, которая располагается медиальнее одноименной артерии. Оценивают контур стенок вены, просвет ее, записывают допплерограмму. Развернув датчик, получают продольный срез вены. Проводят сканирование вдоль вены, оценивают контур стенок, просвет сосуда, наличие клапанов. Записывают допплерограмму. Оценивают форму кривой, ее синхронизацию с дыханием. Проводят дыхательную пробу: глубокий вдох, на задержке дыхания с натуживанием в течение 5 секунд. Определяют функцию клапанного аппарата: наличие расширения вены во время выполнения пробы ниже уровня клапана и ретроградной волны. При выявлении ретроградной волны измеряют ее продолжительность и максимальную скорость. Проводят исследование глубокой вены бедра по аналогичной методике, установив при допплерографии контрольный объем за клапан вены.
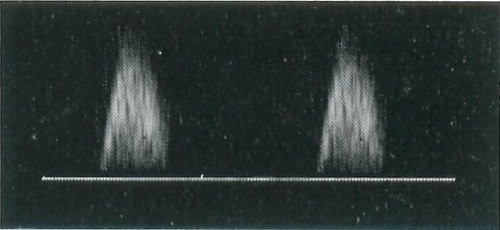
Исследование подколенных вен проводится в положении больного на животе. Для усиления самостоятельного кровотока по вене и облегчения получения допплерограммы пациенту предлагают опереться выпрямленными большими пальцами стоп в кушетку. Датчик устанавливают в области подколенной ямки. Проводят поперечное сканирование для определения топографических взаимоотношений сосудов. Записывают допплерограмму и оценивают форму кривой. Если кровоток в вене слабый, проводят компрессию голени, при этом выявляется усиление кровотока по вене. При продольном сканировании сосуда обращают внимание на контур стенок, просвет сосуда, наличие клапанов (обычно можно выявить 1-2 клапана) (рис. 5).
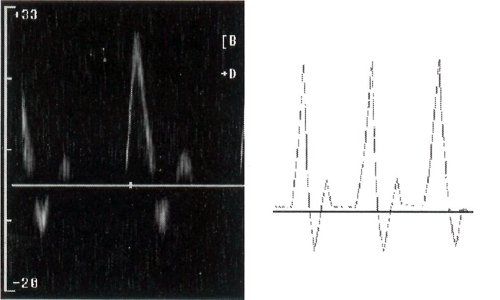
Рис. 5. Исследование кровотока в вене с использованием ЦДК и допплерографии в импульсном режиме.
Проводят пробу с проксимальной компрессией для выявления ретроградной волны. После получения устойчивого спектра сдавливают нижнюю треть бедра на 5 секунд для выявления ретроградного тока. Исследование подкожных вен проводится высокочастотным (7,5-10,0 МГц) датчиком по вышеописанной схеме, предварительно установив датчик в проекции этих вен. Важно проводить сканирование через «гелевую подушку», удерживая датчик над кожей, так как даже небольшого давления на эти вены достаточно для того, чтобы редуцировать в них кровоток.
Рубрика «Разговор со специалистом» Синдром позвоночной артерии
Данная статья совместно подготовлена неврологами ООО «Академия Здоровья» Соловьевой Татьяной Валерьевной и Ананьиной Александрой Владимировной.
Синдром позвоночной артерии (СПА) – это комплекс симптомов, возникающих вследствие нарушения тока крови в позвоночных (или вертебральных) артериях. В последние десятилетия эта патология получила достаточно широкое распространение, что, вероятно, связано с увеличением количества офисных работников и лиц, ведущих малоподвижный образ жизни, проводящих много времени за компьютером. Если ранее диагноз СПА выставлялся преимущественно людям пожилого возраста, то сегодня заболевание диагностируется даже у двадцатилетних пациентов. Поскольку любую болезнь проще предотвратить, чем лечить, каждому важно знать, по каким причинам возникает синдром позвоночной артерии, какими симптомами проявляется и как диагностируется данная патология. Об этом, а также о принципах лечения СПА мы и поговорим в нашей статье.
Основы анатомии и физиологии
Кровь поступает в головной мозг по четырем крупным артериям: левой и правой общей сонным и левой и правой позвоночным. Стоит отметить, что 70-85% крови пропускают через себя именно сонные артерии, поэтому нарушение кровотока в них зачастую приводит к острым нарушениям мозгового кровообращения, то есть к ишемическим инсультам.
Позвоночные артерии обеспечивают мозг кровью лишь на 15-30%. Нарушение кровотока в них острых, опасных для жизни проблем, как правило, не вызывает – возникают хронические нарушения, которые, тем не менее, существенно снижают качество жизни больного и даже приводят к инвалидности.
Позвоночная артерия представляет собой парное образование, берущее свое начало от подключичной артерии, которая в свою очередь отходит слева – от аорты, а справа – от плечеголовного ствола. Позвоночная артерия идет кверху и чуть назад, проходя позади общей сонной артерии, вступает в отверстие поперечного отростка шестого шейного позвонка, поднимается вертикально через аналогичные отверстия всех вышележащих позвонков, через большое затылочное отверстие вступает в полость черепа и следует к мозгу, снабжая кровью задние отделы мозга: мозжечок, гипоталамус, мозолистое тело, средний мозг, частично – височную, теменную, затылочную доли, а также твердую мозговую оболочку задней черепной ямки. До вступления в полость черепа от позвоночной артерии отходят ветви, несущие кровь к спинному мозгу и его оболочкам. Следовательно, при нарушении кровотока в позвоночной артерии возникают симптомы, свидетельствующие о гипоксии (кислородном голодании) участков мозга, которые она питает.
Причины и механизмы развития синдрома позвоночной артерии
На своем протяжении позвоночная артерия контактирует и с твердыми структурами позвоночного столба, и с мягкими тканями, окружающими его. Патологические изменения, возникающие в этих тканях, и являются предпосылками к развитию СПА. Кроме того, причиной могут стать врожденные особенности и приобретенные заболевания непосредственно артерий.
Итак, существует 3 группы причинных факторов синдрома позвоночной артерии:
Врожденные особенности строения артерии: патологическая извитость, аномалии хода, перегибы.
Заболевания, в результате которых уменьшается просвет артерии: атеросклероз, всевозможные артерииты (воспаления стенок артерий), тромбозы и эмболии.
Сдавления артерии извне: остеохондроз шейного отдела позвоночника, аномалии строения костей, травмы, сколиоз (это вертеброгенные, то есть связанные с позвоночником, причины), а также опухоли тканей шеи, их рубцовые изменения, спазм мышц шеи (это невертеброгенные причины).
Зачастую СПА возникает под воздействием сразу нескольких причинных факторов.
Стоит отметить, что чаще развивается СПА слева, что объясняется анатомическими особенностями левой позвоночной артерии: она отходит от дуги аорты, в которой нередко имеются атеросклеротические изменения. Второй ведущей причиной, наряду с атеросклерозом, являются дегенеративно-дистрофические заболевания, то есть остеохондроз. Костный канал, в котором проходит артерия, достаточно узок, и при этом подвижен. Если в области поперечных позвонков имеются остеофиты, они сдавливают сосуд, нарушая приток крови к мозгу.
При наличии одной или нескольких из вышеуказанных причин, факторами, предрасполагающим к ухудшению самочувствия больного и появлению жалоб, являются резкие повороты или наклоны головы.
Симптомы синдрома позвоночной артерии
Патологический процесс при СПА проходит 2 стадии: функциональных нарушений, или дистоническую, и органическую (ишемическую).
Стадия функциональных нарушений (дистоническая)
Главным симптомом на этой стадии является головная боль: постоянная, усиливающаяся во время движений головой или при длительном вынужденном положении, пекущего, ноющего или пульсирующего характера, охватывающая области затылка, висков и следующая вперед ко лбу.
Также на дистонической стадии пациенты предъявляют жалобы на различной интенсивности головокружения: от чувства легкой неустойчивости до ощущения быстрого вращения, наклона, падения собственного тела. Помимо головокружения больных нередко беспокоит шум в ушах и нарушения слуха.
Могут иметь место и разнообразные зрительные нарушения: песок, искры, вспышки, потемнение в глазах, а при осмотре глазного дна – снижение тонуса его сосудов.
Если на дистонической стадии причинный фактор в течение длительного времени не устраняется, заболевание прогрессирует, наступает следующая, ишемическая стадия.
Ишемическая, или органическая, стадия
На данной стадии у пациента диагностируются преходящие нарушения мозгового кровообращения: транзиторные ишемические атаки. Они представляют собой внезапно возникающие приступы выраженного головокружения, нарушения координации движений, тошноты и рвоты, нарушений речи. Как было сказано выше, эти симптомы зачастую провоцируются резким поворотом или наклоном головы. Если при подобных симптомах больной примет горизонтальное положение, высока вероятность их регрессирования (исчезновения). После приступа больной ощущает разбитость, слабость, шум в ушах, искры или вспышки перед глазами, головную боль.
Клинические варианты синдрома позвоночной артерии
Таковыми являются:
дроп-атаки (больной внезапно падает, голова его запрокидывается, пошевелиться и встать в момент приступа он не может; сознание не нарушено; в течение нескольких минут двигательная функция восстанавливается; данное состояние возникает вследствие недостаточного кровоснабжения мозжечка и хвостовых отделов ствола головного мозга);
синкопальный вертебральный синдром, или синдром Унтерхарнштайдта (при резком повороте или наклоне головы, а также в случае длительного нахождения ее в вынужденном положении больной на короткий срок теряет сознание; причиной данного состояния является ишемия области ретикулярной формации головного мозга);
задне-шейный симпатический синдром, или синдром Баре-Льеу (основным признаком его являются постоянные интенсивные головные боли по типу «снимания шлема» — локализуются в затылочной области и распространяются в передние отделы головы; усиливаются боли после сна на неудобной подушке, при повороте или наклоне головы; характер болей пульсирующий или стреляющий; могут сопровождаться другими симптомами, характерными для СПА);
вестибуло-атактический синдром (основными симптомами в данном случае являются головокружение, ощущение неустойчивости, нарушение равновесия, потемнение в глазах, тошнота, рвота, а также нарушения со стороны сердечно-сосудистой системы (одышка, боли в области сердца и другие);
базилярная мигрень (приступу предшествуют нарушения зрения обоих глаз, головокружение, шаткость походки, шум в ушах и смазанность речи, после которых возникает интенсивная головная боль в области затылка, рвота, а затем больной теряет сознание);
офтальмический синдром (на первый план выступают жалобы со стороны органа зрения: боль, чувство песка в глазах, слезотечение, покраснение конъюнктивы; больной видит вспышки и искры перед глазами; острота зрения снижается, что особенно заметно при нагрузке на глаза; частично или полностью выпадают поля зрения);
кохлео-вестибулярный синдром (больной предъявляет жалобы на снижение остроты слуха (особенно затрудненно восприятие шепотной речи), шум в ушах, чувство покачивания, неустойчивости тела или вращения предметов вокруг больного; характер жалоб меняется – они напрямую зависят от положения тела больного);
синдром вегетативных нарушений (пациента беспокоят следующие симптомы: озноб или чувство жара, потливость, постоянно влажные холодные ладони и стопы, колющие боли в сердце, головные боли и так далее; зачастую этот синдром не протекает сам по себе, а сочетается с одним или несколькими другими);
транзиторные ишемические атаки, или ТИА (больной отмечает периодически возникающие преходящие чувствительные или двигательные нарушения, нарушения со стороны органа зрения и/или речи, шаткость и головокружения, тошноту, рвоту, двоение в глазах, затруднения глотания).
Диагностика синдрома позвоночной артерии
На основании жалоб больного врач определит наличие одного или нескольких вышеуказанных синдромов и, в зависимости от этого, назначит дополнительные методы исследования:
рентгенографию шейного отдела позвоночника;
магнитно-резонансную или компьютерную томографию шейного отдела позвоночника;
дуплексное сканирование позвоночных артерий;
вертебральную допплерографию с функциональными нагрузками (сгибанием/разгибанием/поворотами головы).
Если при проведении дообследования диагноз СПА подтверждается, специалист назначит соответствующее лечение.
Лечение синдрома позвоночной артерии
Эффективность лечения данного состояния напрямую зависит от своевременности его диагностики: чем раньше выставлен диагноз, тем менее тернистым будет путь к выздоровлению. Комплексное лечение СПА должно осуществляться одновременно в трех направлениях:
терапия патологии шейного отдела позвоночника;
восстановление просвета позвоночной артерии;
дополнительные методы лечения.
Прежде всего, больному будут назначены противовоспалительные и противоотечные средства, а именно нестероидные противовоспалительные препараты (мелоксикам, нимесулид, целекоксиб), ангиопротекторы (диосмин) и венотоники (троксерутин).
С целью улучшения тока крови через позвоночную артерию применяют агапурин, винпоцетин, циннаризин, ницерголин, инстенон и другие подобные препараты.
Чтобы улучшить метаболизм (обмен веществ) нейронов, используют цитиколин, глиатилин, церебролизин, актовегин, мексидол и пирацетам.
Для улучшения обмена веществ не только в нервах, но и в других органах и тканях (сосудах, мышцах), больной принимает милдронат, триметазидин или тиотриазолин.
С целью расслабить спазмированные поперечнополосатые мышцы будут использованы мидокалм или толперил, гладкие мышцы сосудов – дротаверин, более известный пациентам, как Но-шпа.
При приступах мигрени применяют антимигренозные средства, например суматриптан.
Для улучшения питания нервных клеток – витамины группы В (Мильгамма, Нейробион, Нейровитан и другие).
Чтобы устранить механические факторы, сдавливающие позвоночную артерию, больному может быть назначено физиолечение (мануальная терапия, постизометрическая релаксация мышц) или же хирургическое вмешательство.
В восстановительный период широко применяются массаж воротниковой зоны, лечебная физкультура, иглорефлексотерапия, а также санаторно-курортное лечение.
Профилактика синдрома позвоночной артерии
Основными профилактическими мероприятиями в данном случае являются активный образ жизни и здоровый сон на удобных спальных принадлежностях (очень желательно, чтобы они относились к категории ортопедических). В случае, если ваша работа предусматривает длительное нахождение головы и шеи в одном положении (например, это работа за компьютером или деятельность, связанная с непрерывным письмом), настоятельно рекомендуется делать перерывы в ней, во время которых проводить гимнастику для шейного отдела позвоночника. При появлении жалоб, указанных выше, не следует ждать их прогрессирования: правильным решением будет в короткий срок обратиться к врачу.
Записаться на консультативный прием невролога можно по телефону: 8(3435)230-500
Мы заботимся о Вас!
Всегда Ваш, Медицинский центр «Академия Здоровья»
Начальные проявления недостаточности кровоснабжения мозга (этиология, патогенез, клиника и диагностика)
Согласно “Классификации сосудистых поражений головного и спинного мозга”, разработанной НИИ неврологии РАМН, к начальным проявлениям недостаточности кровоснабжения мозга (НПНКМ) относят синдром, включающий признаки основного сосудистого заболевания и час
Согласно “Классификации сосудистых поражений головного и спинного мозга”, разработанной НИИ неврологии РАМН, к начальным проявлениям недостаточности кровоснабжения мозга (НПНКМ) относят синдром, включающий признаки основного сосудистого заболевания и частые (не реже одного раза в неделю на протяжении последних трех месяцев) жалобы на головные боли, головокружение, шум в голове, нарушение памяти и снижение работоспособности. Причем основанием для установления диагноза НПНКМ может быть только сочетание двух или более из пяти перечисленных возможных жалоб больных. Кроме того, следует особо отметить, что у пациента не должно быть симптомов очагового поражения центральной нервной системы, преходящих нарушений мозгового кровообращения (транзиторных ишемических атак и церебральных гипертонических кризов), поражений мозга другого происхождения, таких как последствия черепно-мозговых травм, нейроинфекции, опухоли и др., а также тяжелых психических и соматических заболеваний.
 |
| Рисунок 1. Компьютерная томограмма головного мозга. Кровоизлияние в боковой желудочек |
По нашим данным, в группе мужчин 40-49 лет с артериальной гипертонией (АГ), выделенной при эпидемиологическом обследовании населения, за семь лет наблюдения преходящие нарушения мозгового кровообращения возникали в 2,8, а инсульты — в 2,7 раза чаще у пациентов, которым при первом обследовании был поставлен диагноз НПНКМ по сравнению с лицами без цереброваскулярной патологии (см. табл.).
Основными этиологическими факторами возникновения НПНКМ являются АГ, атеросклероз и вегетососудистая дистония.
Наиболее значительную роль в патогенезе НПНКМ играют нарушение нервной регуляции сосудов; морфологические изменения экстра- и интракраниальных сосудов (стенозы и окклюзии); изменения биохимических и физико-химических свойств крови: увеличение вязкости, адгезии и агрегации форменных элементов крови; нарушения метаболизма мозга; заболевания сердца.
Одним из наиболее ранних и частых симптомов является головная боль, характер и локализация которой отличаются большим разнообразием. Причем нередко она не зависит от уровня артериального давления. Головокружение – специфическое ощущение, связанное с вестибулярной дисфункцией, — может служить ранним признаком сосудистых нарушений в вертебрально-базилярной системе. Появление шума объясняется затруднением тока крови в
| Результаты семилетнего проспективного наблюдения мужчин 40–49 лет с АГ в зависимости от наличия НПНКМ при первом обследовании* | ||||
| Первое обследование | Заключительное обследование | |||
| Без ЦВП | НПНКМ | ПНМК | МИ | |
| 87 человек без ЦВП | 24 27.6% | 32 36.8% | 11 12.6% | 2 2.3% |
| 160 человек с НПНКМ | 3 1.9% | 42 26.3% | 57 35.6% | 10 6.2% |
| * ЦВП — цереброваскулярная патология НПНКМ — начальные проявления недостаточности кровоснабжения мозга ПНМК — преходящие нарушения мозгового кровообращения МИ — мозговой инсульт | ||||
близко расположенных к лабиринту крупных сосудах. Память чаще всего ухудшается на текущие события, тогда как профессиональная память и память на прошлое не снижается. Чаще страдает механическая память, чем логическая. Ухудшаются как умственная, так и физическая работоспособность. Изменения психического тонуса отмечаются преимущественно при увеличении объема и ограничении времени выполнения заданий и сочетаются с нарушениями в эмоционально-личностной сфере. Нередко у больных НПНКМ отмечаются астенический, ипохондрический, тревожно-депрессивный и другие неврозоподобные синдромы.
Психологическое исследование. При НПНКМ на фоне вегетососудистой дистонии у подавляющего большинства больных выявляются повышенная раздражительность, неустойчивость внимания, ослабление памяти и сужение объема восприятия, а у некоторых пациентов – снижение темпа деятельности. Нарушения умственной деятельности выражены меньше, чем у больных атеросклерозом. На самых ранних стадиях АГ обнаружены функциональные мозговые нарушения, спровоцированные психоэмоциональными перенапряжениями. Эти нарушения способствуют развитию гемодинамических сдвигов, приводящих к формированию сосудистой патологии мозга. НПНКМ при гипертонической болезни I-II стадии возникают на фоне вегетативных нарушений, эмоциональных сдвигов тревожного характера, патологической фиксации эмоций. Нередко отмечаются раздражительность, слезливость, немотивированное чувство страха, тревоги.
При атеросклерозе преобладают астенические состояния. Наиболее часты жалобы на общую слабость, апатию, быструю утомляемость, нарушение памяти, внимания, неспособность сосредоточиться, неустойчивое настроение.
Тем не менее у больных НПНКМ основные виды психической деятельности остаются на достаточно высоком уровне. Такие люди успешно выполняют сложные задания и даже творческую работу.
Реоэнцефалография и тетраполярная реография. Одним из самых доступных методов ранней диагностики патологии сосудов головы является реоэнцефалография (РЭГ).
При вегетососудистой дистонии чаще всего обнаруживаются ангиодистонические изменения, синдром регионарной гипертонии, сосудов, нарушения венозного тонуса. Центральная и периферическая гемодинамика существенно не страдают.
У больных АГ типичными являются признаки повышения тонуса сосудистой стенки, которые наблюдаются уже на ранней стадии болезни и коррелируют с уровнем артериального давления. Кроме того, характерно уменьшение кровенаполнения сосудов, нарастающее с развитием заболевания. Повышенный сосудистый тонус чаще определяется в молодом и несколько реже – в среднем возрасте. По мере прогрессирования заболевания уменьшаются дистонические изменения и реактивность по отношению к вазоактивным препаратам, снижаются объемное пульсовое кровенаполнение и эластичность сосудистой стенки. У большинства больных НПНКМ при АГ на фоне выраженного стойкого повышения тонуса сосудов головы отмечается значительное снижение минутного объема кровообращения за счет ударного объема сердца, брадикардии и экстрасистолии. Значения сдвигов показателей гемодинамики при физической нагрузке, по данным РЭГ, у больных НПНКМ на фоне АГ определяются исходным состоянием пульсового кровенаполнения сосудов головы, типовыми особенностями центральной гемодинамики, степенью выполняемой нагрузки, стадией основного заболевания и возрастом больных.
Типичными изменениями РЭГ у больных НПНКМ при атеросклерозе являются признаки снижения пульсового кровенаполнения, эластичности сосудистой стенки и реакции на вазоактивные препараты, затруднения венозного оттока и повышения тонуса. Наблюдается снижение минутного объема в связи с уменьшением ударного объема сердца и периферического сосудистого сопротивления.
Важную роль в формировании недостаточности кровоснабжения мозга играют нарушения венозного кровообращения. У больных НПНКМ могут регистрироваться дистония, гипертония или умеренная гипотония вен головы и смешанные виды нарушения их тонуса. Поэтому рекомендуется комплексное исследование венозной системы головы, включающее РЭГ, радиоциркулоэнцефалографию, биомикроскопию бульбарной конъюнктивы, офтальмоскопию и офтальмодинамометрию в центральной вене сетчатки.
Электроэнцефалография. Электроэнцефалография (ЭЭГ) отражает локализацию и степень дисциркуляторных мозговых нарушений. У больных НПНКМ, как правило, отмечаются диффузные, нерезко выраженные изменения в ЭЭГ, снижение амплитуды и регулярности a-ритма, общая дезорганизация биопотенциалов и отсутствие доминирующего ритма.
При вегетососудистой дистонии часто выясняется, что в процесс вовлечены структуры промежуточного мозга и гипоталамуса, которые ответственны за церебральный электрогенез и оказывают диффузное влияние на биоэлектрическую активность коры больших полушарий. Чем ярче выражены явления раздражения вегетативных структур, тем более диффузными и грубыми становятся патологические формы биопотенциалов и феномены неустойчивости.
У больных АГ обнаруживаются диффузные изменения биоэлектрической активности мозга в виде дезорганизации a-ритма, усиления быстрых колебаний, появления медленных волн, исчезновения зональных различий. Чаще всего наблюдается III тип ЭЭГ (по Е. А. Жирмунской, 1965), который характеризуется отсутствием доминирования тех или иных ритмов при низком амплитудном уровне (не более 35 мкB). Иногда отмечается гиперсинхронизация основного ритма, подчеркнутая его регулярностью на высоком амплитудном уровне (IV тип ЭЭГ). Нередко встречаются выраженные изменения биоэлектрической активности мозга, проявляющиеся диффузной дезорганизацией ритмов на высоком амплитудном уровне или пароксизмальной активностью (V тип ЭЭГ).
В начальной стадии церебрального атеросклероза отмечаются диффузные изменения в ЭЭГ, очаговые сдвиги встречаются лишь в редких случаях. Характерны явления десинхронизации и редукции a-ритма, нарастание удельного веса плоских бездоминантных кривых, сглаженность зональных различий основных ритмов, сужение диапазона усвоения навязанных ритмов.
| При НПНКМ часто наблюдается головная боль, головокружение, нарушение памяти, изменение психического статуса |
Таким образом, при всем многообразии и отсутствии специфичности ЭЭГ при НПНКМ имеются некоторые особенности, характерные для вегетососудистой дистонии, ПГ и церебрального атеросклероза, что, по-видимому, связано с различиями в этиологической и патогенетической сущности этих заболеваний. Отрицание нозологической специфичности отдельных компонентов ЭЭГ не умаляет значения исследования биоэлектрической активности мозга у больных НПНКМ.
В связи с тем что сопоставление данных РЭГ и ЭЭГ в определенной степени может свидетельствовать о соответствии между уровнем кровоснабжения мозга и его функциональным состоянием, метод сочетанной регистрации РЭГ и ЭЭГ с функциональными пробами используют для выявления начальных признаков недостаточности кровоснабжения мозга.
Ультразвуковая допплеросонография магистральных сосудов головы. В последние годы показано, что в диагностике сосудистых заболеваний мозга важное значение имеет ультразвуковая доплерография (УДГ). Диагностическая достоверность этого метода веско аргументирована путем сопоставления результатов исследования с данными церебральной ангиографии. Доказана его высокая эффективность в распознавании окклюзирующих поражений магистральных сосудов головы, их локализации, степени стеноза, наличия и выраженности коллатерального кровообращения. Внедрение вычислительной техники в обработку допплеросонограмм существенно расширило диагностические возможности метода, возросла точность получаемых результатов. Таким образом, удалось получить ряд количественных спектральных характеристик доплеровского сигнала, коррелирующих с определенными клиническим состояниями, и разработать технику изображения общей, внутренней и наружной сонных артерий. При этом стеноз и окклюзия сосудов выявляются в 90% случаев, что важно для решения вопроса о проведении ангиографии и выбора тактики лечения.
У больных НПНКМ отмечается высокая частота поражений магистральных сосудов головы и связанных с ними изменений гемодинамики. Так, из обследованных нами 275 мужчин с НПНКМ в возрасте 50–59 лет окклюзирующие поражения выявлены у 57 (20,7%). Чаще всего они обнаруживались в одном (47%) и двух (39%) сосудах, значительно реже – в трех (8%) и четырех (6%).
В настоящее время для обследования больных с цереброваскулярной патологией применяется транскраниальная УДГ, позволяющая судить о состоянии внутричерепных сосудов.
Выявленные при НПНКМ случаи окклюзирующего поражения сосудов подтверждают принципиально важное положение о частом несоответствии степени выраженности сосудистого процесса и его клинических проявлений.
Хронометрирование показало, что на проведение и последующую оценку исследования методом УДГ одного больного требуется в среднем 16,4 мин, что позволяет использовать его, как и РЭГ, при массовых обследованиях населения в возрасте старше 40 лет.
Применение таких современных методов исследования, как ультразвуковой и ангиографический, свидетельствует о том, что атеросклеротическое поражение артерий мозга, приводящее к стенозу или окклюзии, является важным фактором риска цероброваскулярных заболеваний. Однако нередко ишемические поражения мозга возникают и без существенных изменений этих сосудов, в первую очередь при патологии сердца.
Электрокардиография и эхокардиография. Ухудшение гемодинамики в результате нарушения сердечной деятельности играет важную роль в патогенезе недостаточности мозгового кровообращения, особенно при ремиттирующем течении. Тесные цереброкардиальные взаимосвязи обнаруживаются уже на ранних этапах формирования сосудистых заболеваний. У больных НПНКМ при АГ и атеросклерозе отмечается достоверное увеличение числа случаев гипертрофии левого желудочка и ишемической болезни сердца,
| НПНКМ, по данным эпидемиологических исследований, составляют 60–75% всех случаев цереброваскулярных заболеваний и являются серьезным фактором риска острых нарушений мозгового кровообращения, что подтверждается длительными проспективными исследованиями |
по данным ЭКГ, по сравнению с лицами, у которых основное сосудистое заболевание протекает без цереброваскулярных нарушений. С развитием стойкой АГ и выраженного атеросклероза нарастание общих и регионарных гемодинамических расстройств приводит к тому, что функциональные церебральные и кардиальные нарушения трасформируются в ишемическую болезнь сердца и мозга.
По данным эхокардиографии, у больных НПНКМ в сочетании с ишемической болезнью сердца наблюдается снижение сократимости миокарда, уменьшение ударного объема сердца, фракции выброса и нарастание конечного систолического и диастолического объема.
Исследования липидов крови. Для уточнения характера основного сосудистого заболевания, проведения вторичной профилактики и дифференцированного лечения важна комплексная оценка нарушений липидного обмена с фенотипированием гиперлипопротеидемий. Нарушения липидного обмена обнаруживаются уже на ранних стадиях развития церебрального атеросклероза и возрастают по мере увеличения гемодинамических расстройств в головном мозге. Они проявляются повышением содержания в плазме крови атерогенных классов b-липопротеидов, пре-b-липопротеидов, триглицеридов и неэстерифицированных жирных кислот. Повышаются уровень общего холестерина, суммарные фракции липопротеидов низкой плотности и очень низкой плотности. При НПНКМ преобладают II-А, II-Б и IV типы гиперлипопротеидемий по классификации Фредриксона и соавт. (1974).
Установлена прямая корреляция между дислипопротеидемией и атеросклеротическими поражениями сосудов мозга, обнаруженными при ангиографии.
При НПНКМ усиливается перекисное окисление липидов и уменьшается их антиоксидантная активность.
Исследование реологических и коагулирующих свойств крови. Для диагностики и лечения НПНКМ определенное значение имеет исследование гемокоагуляции. В настоящее время для уточнения состояния системы свертывания крови применяется расширенная коагулография, а при профилактических обследованиях – тромбоэластография, преимуществом которой являются высокая чувствительность, быстрота получения результатов (через 1–1,5 ч), возможность изменения механических свойств, структуры сгустка без заметных нарушений обычных условий коагуляции. У лиц с НПНКМ по сравнению со здоровыми установлены достоверные различия почти по всем показателям тромбоэластограммы.
Уже на ранних стадиях развития сосудистых поражений мозга отмечаются изменения в системе микроциркуляции, обусловленные гемореологическими расстройствами. Повышение вязкости крови выявляется у больных НПНКМ, и развивается не только при атеросклерозе, но и при АГ. Рассогласование процессов свертывания крови и фибринолиза является патогенетической предпосылкой микроциркуляторных расстройств. Эта дисфункция рассматривается как гемореологический критерий предболезни.
У лиц с НПНКМ при нормальном уровне АД отмечено повышение агрегации тромбоцитов под воздействием адреналина и увеличение концентрации фибриногена. Выявлена зависимость реологических показателей от степени поражения магистральных сосудов головы, по данным УДГ. При наличии признаков стеноза и окклюзии у больных НПНКМ обнаружено повышение агрегации тромбоцитов под действием разных стимуляторов: адреналина, АДФ. Нарастает вязкость крови, а в ряде случаев увеличивается агрегация эритроцитов, снижаются их деформационные свойства.
Офтальмологическое исследование. Одним из наиболее значимых в диагностике АГ и определении стадии заболевания является офтальмологическое исследование. Повторные осмотры глазного дна необходимы для оценки динамики процесса и эффективности лечения. Глазные симптомы нередко предшествуют другим проявлениям основного сосудистого заболевания и даже повышению артериального давления.
При АГ наиболее ранние проявления патологии сосудов глазного дна заключаются в функциональном тоническом сокращении артериол сетчатки и склонности их к спастическим реакциям. Об ухудшении течения АГ свидетельствует увеличение площади слепого пятна.
У больных с начальными стадиями церебрального атеросклероза комплекс офтальмологических исследований позволяет выделить наиболее типичные формы изменения глазных сосудов. Чаще всего у них встречается ровный ход артерий, сужение и неравномерность калибра, патологический артерио-венозный перекрест.
Результаты офтальмо- и фотокалиброметрических исследований подтверждают тенденцию к сужению артерий сетчатки при некотором расширении ретинальных вен с уменьшением артерио-венозного соотношения.
Офтальмодинамометрические исследования позволяют судить о состоянии гемодинамики в глазничной артерии. У большинства больных атеросклерозом регистрируется повышение систолического, диастолического и особенно среднего давления, а также снижение соотношения между ретинальным и плечевым давлением.
Атеросклеротические поражения конъюнктивальных сосудов обнаруживаются значительно раньше, чем сосудов сетчатки. Характерны изменения их хода, калибра и формы, интраваскулярная агрегация эритроцитов. Патология сосудов конъюнктивы и эписклеры отмечается более чем у 90% больных ранним церебральным атеросклерозом. Кроме того, для атеросклеротических поражений типично отложение липоидов и кристаллов холестерина по лимбу роговицы и в стекловидном теле. Выявление этих симптомов наиболее важно при обследовании лиц молодого возраста, у которых другие проявления атеросклероза выражены меньше.
У больных вегетососудистой дистонией, особенно при церебральной форме, протекающей по гипертоническому типу, обнаружена неустойчивость полей зрения, обусловленная нарушением функции главным образом коркового отдела зрительного анализатора.
Рентгенологические методы исследования. Компьютерная томография головного мозга. У отдельных больных НПНКМ могут выявляться небольшие ишемические очаги поражения головного мозга.
Рентгенография черепа. В ряде случаев обнаруживается обызвествленная внутренняя сонная и реже – основная артерия, кальциноз общих сонных артерий.
Рентгенография шейного отдела позвоночника. Метод позволяет обнаружить признаки остеохондроза, деформирующего спондилеза и другие изменения шейного отдела позвоночника.
Термография. Метод применяется для исследования кровотока в сонных артериях. Особенно важно, что его можно использовать для обнаружения малосимптомно или асимптомно протекающего стеноза. Целесообразно широкое применение термографии в амбулаторно-поликлинических условиях для обследования больших контингентов населения в возрасте старше 40 лет.
Иммунологические исследования. У больных НПНКМ при атеросклерозе обнаружены снижение уровня Т-лимфоцитов и увеличение индекса соотношения иммунорегуляторных клеток, указывающие на снижение супрессорной функции Т-лимфоцитов. Эти изменения способствуют развитию аутоиммунных реакций. Положительные результаты реакции подавления прилипания лейкоцитов, подтверждающие их сенсибилизацию к антигенам мозга, достоверно чаще встречаются у больных НПНКМ при атеросклерозе и АГ, чем у лиц без цереброваскулярной патологии, что свидетельствует о развитии аутоиммунных реакций. Отмечена связь между сенсибилизацией лейкоцитов к антигенам мозга и жалобами больных на снижение памяти и умственной работоспособности, что позволяет судить о возможности участия аутоиммунных реакций в патогенезе заболевания.
Литература
1. Акимов Г. А. Начальные проявления сосудистых заболеваний головного мозга. М., 1983
2. Гусев Е. И., Бурд Г. С., Нифонтова Л. А. и др. Начальные проявления недостаточности кровоснабжения мозга // Журн. невропатол. и психиатр. 1983. № 1. С. 3-10.
3. Гусев Е. И. Ишемическая болезнь головного мозга. Актовая речь. М., 1992.
4. Канарейкин К. Ф., Манвелов Л. С., Бахур В. Т. Клиника и диагностика начальных проявлений недостаточности кровоснабжения мозга // Клиническая медицина. 1991. № 2. С. 64-66.
5. Маджидов Н. М., Трошин В. Д. Доинсультные цереброваскулярные заболевания. Ташкент; М., 1985.
6. Манвелов Л. С. О некоторых итогах изучения начальных проявлений недостаточности кровоснабжения мозга // Клиническая медицина. 1995. № 5. С. 28-30.
7. Панков Д. Д. Клиническая сущность термина “начальные проявления недостаточности кровоснабжения мозга” // Журн. неврол. и психиатр. 1996. № 6. С. 12-15.
8. Шмидт Е. В., Лунев Д. К., Верещагин Н. В. Сосудистые заболевания головного и спинного мозга. М., 1976.
9. Шмидт Е. В. Классификация сосудистых поражений головного и спинного мозга // Журн. неврол. и психиатр. 1985. № 9. С. 1281-1288.