Ксеродерма что это такое
Пигментная ксеродерма
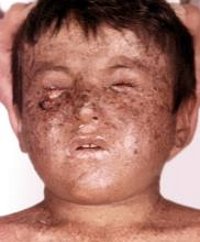
Пигментная ксеродерма (лентикулярный меланоз, злокачественное лентиго, пигментная атрофодермия) — хроническое наследственное заболевание, обусловленное повышенной чувствительностью кожи к солнечной радиации и УФ-лучам. Изменения кожи характеризуются последовательно сменяющими друг друга процессами воспаления, гиперпигментации, атрофии, гиперкератоза и злокачественной трансформации клеток кожи. У большинства больных отмечается поражение глаз: конъюнктивит, кератит и опухоли. Диагноз устанавливается при выявлении повышенной чувствительности кожи к УФ и характерной гистологической картины. Лечение симптоматическое.
Общие сведения
По данным статистических исследований, которые проводит дерматология, пигментная ксеродерма встречается в среднем с частотой 1 случай на 250 тыс. человек. Наиболее высокая заболеваемость отмечается среди населения стран Среднего Востока и Средиземноморского побережья Африки. Пигментной ксеродермой заболевают оба пола, однако некоторые дерматологи отмечают, что среди девочек болезнь встречается чаще. Заболевание часто носит семейный характер и наблюдается при близкородственных браках.
Причины возникновения пигментной ксеродермы
Различают 2 генотипа пигментной ксеродермы: передающийся аутосомно-доминантным путем и аутосомно-рецессивным. В основе заболевания лежит генетически обусловленная недостаточность ферментов УФ-эндонуклеазы и полимеразы-1, которые отвечают за восстановление ДНК после ее повреждения УФ-лучами. В связи с этим у больных после пребывания в условиях повышенной солнечной радиации развиваются поражения кожи и глаз. У некоторых гетерозиготных носителей гена наблюдаются стертые формы пигментной ксеродермы в виде различных пигментных нарушений.
Симптомы пигментной ксеродермы
Наиболее часто (в 75% случаев) начало пигментной ксеродермы приходится на первые 6-12 месяцев жизни. Заболевание проявляется весной или летом, как только ребенок попадает под интенсивное воздействие солнечных лучей. В отдельных случаях начальные проявления пигментной ксеродермы наблюдались у пациентов в возрасте 14-35 лет и даже на 65-ом году жизни.
В течении пигментной ксеродермы выделяют 5 переходящих одна в другую стадий: зритематозную, стадию гиперпигментаций, атрофическую, гиперкератическую и стадию злокачественных опухолей.
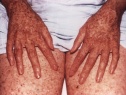
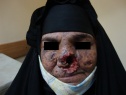
Эритематозная стадия характеризуется воспалительными изменениями кожи на участках, подвергшихся воздействию ультрафиолета. В таких областях кожного покрова появляются покраснение, отек, мелкие пузырьки и пузыри. После разрешения элементов первой стадии на коже остаются коричневые, желтоватые или бурые пигментные пятна, похожие на веснушки (стадия гиперпигментаций).
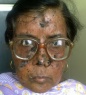
Последующие облучения кожи у пациентов с пигментной ксеродермой ведут к новым воспалительным и пигментным изменениям кожи, что вызывает развитие атрофических процессов. Заболевание переходит в атрофическую стадию, для которой характерны истончение и сухость кожи, образование трещин и рубцов. Кожа натянута и не собирается в складки. Отмечается уменьшение рта (микротомия), атрезия отверстия рта и носа, истончение кончика носа и ушей.
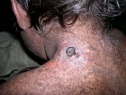
Гиперкератическая стадия проявляется развитием в очагах пораженной кожи бородавчатых разрастаний, папиллом, кератом, фибром. Стадия злокачественных опухолей наблюдается, как правило, спустя 10-15 лет от начала пигментной ксеродермы. Но иногда злокачественные новообразования появляются в первые годы заболевания. К злокачественным опухолям, встречающимся при пигментной ксеродерме, относятся базалиомы, меланомы, эндотелиомы, саркомы, трихоэпителиомы, ангиосаркомы. Они характеризуются быстрым метастазированием во внутренние органы, приводящим заболевание к летальному исходу.
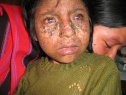
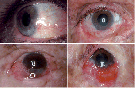
В 80-85% случаев пигментной ксеродермы наблюдаются поражения глаз в виде конъюнктивита, кератита, гиперпигментации и атрофии радужки и роговицы, приводящих к понижению зрения. На коже век появляются телеангиэктазии, гиперкератозы, дисхромии и опухолевые процессы. Нередко пигментная ксеродерма сочетается с дистрофическими изменениями тканей: дистрофией зубов, синдактилией, врожденной алопецией, отставанием в росте. Пигментная ксеродерма, сопровождающаяся умственной отсталостью ребенка, выделена как отдельная клиническая форма — синдром де Санктиса-Какионе.
Диагностика пигментной ксеродермы
Специфический метод диагностики пигментной ксеродермы проводится при помощи монохроматора и заключается в выявлении повышенной чувствительности кожного покрова к воздействию ультрафиолета.
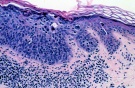
Для уточнения диагноза дерматолог назначает биопсию пораженного участка кожи. Последующее гистологическое исследование в ранней стадии заболевания определяет гиперкератоз, отек и воспалительную инфильтрацию дермы, истончение росткового слоя, пигментацию базального слоя. В атрофической и гиперкератической стадии наблюдается атрофия эпидермиса, дегенеративные изменения коллагеновых и эластических волокон. В стадии злокачественных опухолей — атипические клетки и гистологическая картина рака кожи.
Лечение пигментной ксеродермы
Пациентам следует избегать воздействия УФ-лучей: носить шляпы с большими полями и вуали, применять солнцезащитные крема и мази, использовать пудры с танином. Медикаментозное лечение пигментной ксеродермы в основном симптоматическое и, к сожалению, малоэффективно. Применяют ароматические ретиноиды, токоферол, хингамин. При развитии злокачественных процессов дополнительно назначают проспидин, пиридоксин, тиамин, цианокобаламин. Папилломатозные и бородавчатые разрастания удаляют хирургически, путем криодеструкции, электрокоагуляции или удаления лазером.
Ксеродерма что это такое
Этиология и встречаемость пигментной ксеродермы. Пигментная ксеродерма — генетически разнородное, панэтническое, аутосомно-рецессивное заболевание репарации ДНК, вызывающее выраженную гиперчувствительность к ультрафилетовым лучам. В США и Европе распространенность составляет приблизительно 1 на миллион, но в Японии — 1 на 100 000.
Патогенез пигментной ксеродермы
Репарация ДНК, повреждаемой ультрафиолетовым излучением, происходит благодаря трем механизмам: эксцизионной репарации, пострепликационной репарации и фотореактивизации. Эксцизионная репарация устраняет повреждения ДНК восстановлением нуклеотида или одного основания. Пострепликационная репарация — аварийный механизм, обеспечивающий репликацию ДНК вдоль поврежденного шаблона. Фотореактивация возвращает поврежденную ДНК в нормальное химическое состояние без удаления или замены генетического материала.
Нуклеотидная эксцизионная репарация — сложный разносторонний процесс, в котором участвуют, по крайней мере, 30 белков. Основной принцип — удаление небольшого однонитевого участка ДНК, содержащего повреждение, разрезами с обеих сторон поврежденного сегмента, с последующим заполнением промежутка вновь синтезированной нитью на основе неповрежденной дополнительной нити, используемой как шаблон. В ходе транскрипции гена повреждение ДНК блокирует продвижение РНК-полимеразы II.
Остановленная РНК-полимераза II инициирует эксцизионную репарацию нуклеотидов (репарация, вызванная транскрипцией). В остальной части генома и в нетранскрибируемых генах комплекс нуклеотидной эксцизионной репарации выявляет повреждения ДНК по искажению скручивания ДНК (глобальная геномная репарация).
Иногда нуклеотидная эксцизионная репарация неспособна исправить повреждение ДНК до репликации. Поскольку такие повреждения тормозят репликацию ДНК, пострепликационная репарация обходит повреждение, позволяя продолжить синтез ДНК. ДНК-полимераза n обеспечивает ДНК синтез через поврежденные участки; она эффективно и точно катализирует правильный синтез, пропуская дитимидиновые повреждения.
Пигментная ксеродерма вызвана мутациями, влияющими на геномную нуклеотидную эксцизионную репарацию или пострепликационную репарацию. В отличие от нее, синдром Коккейна — сходное заболевание, вызываемое мутациями, влияющими на связанный с транскрипцией путь нуклеотидной эксцизионной репарации. И пигментная ксеродерма, и синдром Коккейна подразделяют на 10 биохимических групп комплементации; каждая группа отражает мутации различных компонентов нуклеотидной эксцизионной или пострепликационной репарации.
Снижение или полное отсутствие возможности глобальной геномной репарации или пострепликационной репарации приводит к потере функций, необходимых для поддержания целостности генома, и вызывает накопление онкогенных мутаций. Новообразования у пациентов с пигментной ксеродермой имеют более высокий уровень мутаций генов-онкогенов и супрессоров опухолевого роста, чем опухоли в нормальной популяции, и эти мутации специфично вызывает ультрафиолетовое облучение.
Фенотип и развитие пигментной ксеродермы
Симптоматика у пациентов с пигментной ксеродермой развивается в среднем в возрасте 1-2 года, хотя приблизительно у 5% пациентов описано начало после 14 лет. Первые симптомы обычно включают легкие ожоги, повышенную фоточувствительность, появление лентигинозной сыпи и фотобоязнь. Постоянное воздействие вызывает преждевременное старение кожи (истончение, морщины, веснушки, телеангиэктазии), фотокератоз и доброкачественные и злокачественные новообразования. Почти у 45% пациентов развиваются базальноклеточные или сквамозноклеточные карциномы, у 5% — меланомы.
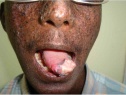
Приблизительно 90% карцином появляется в местах сильного ультрафиолетового воздействия — на лице, шее, голове, кончике языка. До введения профилактических мероприятий средний возраст развития новообразований был 8 лет, на 50 лет раньше, чем в общей популяции, а их частота более чем в 1000 раз выше общепопуляционной.
Кроме кожных симптомов, у 60-90% пациентов отмечают нарушения со стороны глаз, включая фотобоязнь, конъюнктивиты, блефариты, эктропион и новообразования. Распределение патологии глаз и новообразований соответствуют участкам наибольшего влияния ультрафиолета.
Приблизительно у 18% пациентов развивается прогрессирующая дегенерация нейронов. Симптоматика представлена нейросенсорной глухотой, задержкой умственного развития, спастичностью, гипорефлексиией или арефлексией, сегментарной демиелинизацией, атаксиями, хореоатетозом и надъядерной офтальмоплегией. Тяжесть неврологических симптомов обычно пропорциональна степени нарушения нуклеотидной эксцизионной репарации. Нейродегенерация может быть вызвана неспособностью исправлять ДНК, повреждаемую эндогенными свободными радикалами.
Эксцизионная нуклеотидная репарация также исправляет повреждения ДНК, вызванные большинством химических канцерогенов, например сигаретным дымом, подгоревшей пищей или цисплатином (производное платины с противоопухолевой активностью, способное стимулировать механизмы клеточно-опосредованной цитотоксичности). В связи с этим у пациентов в 10-20 раз повышена частота опухолей внутренних органов, например опухолей мозга, лейкозов, рака легких и желудка.
Пациенты с пигментной ксеродермой имеют уменьшенный срок жизни; без профилактической защиты срок их жизни почти на 30 лет короче по сравнению с лицами без пигментной ксеродермы. Наиболее частые причины смерти — метастатические меланомы и сквамозноклеточные карциномы кожи.
Два сходных с пигментной ксеродермой заболевания, синдром Коккейна и трихотиодистрофия, также вызываются дефектами в различных компонентах клеточного механизма репарации нарушений ДНК, вызванных ультрафиолетом. Для обоих заболеваний характерны плохой постнатальный рост, уменьшение подкожной клетчатки, контрактуры суставов, тонкая кожа с фоточувствительностью, умственная задержка и неврологические симптомы.
У детей с синдромом Коккейна также развиваются дегенерация сетчатки и глухота; дети с трихотиодистрофией имеют ихтиоз и ломкие волосы и ногти. При обоих синдромах пациенты редко живут дольше 20 лет. Интересно, что ни тот, ни другой синдром не сопровождаются увеличением частоты опухолей кожи. Тем не менее дефекты в некоторых генах репарации ДНК (ERCC2, ERCC3 и ERCC5) приводят к фенотипам, имеющим общие симптомы между пигментной ксеродермой, синдромом Коккейна и трихотиодистрофией.
Особенности фенотипических проявлений пигментной ксеродермы:
• Возраст начала: детство
• Чувствительность к ультрафиолету
• Опухоли кожи
• Неврологическая дисфункция
Лечение пигментной ксеродермы
Подтверждение диагноза пигментной ксеродермы проводят функциональными тестами репарации ДНК и чувствительности к ультрафиолету; такие тесты обычно выполняют на зрелых фибробластах кожи. Подтверждение диагноза идентификацией мутаций в генах, связанных с пигментной ксеродермой, в настоящее время клинически недоступно.
Оказание помощи пациентам с пигментной ксеродермой состоит в исключении воздействия солнечного света, ношении защитной одежды, использовании физических и химических солнцезащитных кремов и тщательном наблюдении для своевременного выявления и удаления злокачественных новообразований. Исцеляющее лечение в настоящее время недоступно.
Риски наследования пигментной ксеродермы
Поскольку пигментная ксеродерма — аутосомно-рецессивное заболевание, семейный анамнез у большинства пациентов не отягощен. Для родителей, имеющих ребенка с пигментной ксеродермой, риск для последующих детей — 1 к 4. Пренатальная диагностика возможна путем определения функции репарации ДНК и чувствительности к ультрафиолету в культуре амниоцитов или клеток ворсин хориона.
Пример пигментной ксеродермы. B.C., 3-летний мальчик, направлен в клинику дерматологии в связи с выраженной чувствительностью к солнечным лучам и появлением множественных пятен. При клиническом осмотре выявлены фотобоязнь, конъюнктивит и значительная лентигинозная гиперпигментация в незащищенных от солнца областях; в остальном его развитие и данные осмотра оказались нормальными. Пациент — ребенок от неродственного брака родителей японского происхождения; никто в семье подобным образом не болел. Дерматолог сказал, что у ребенка классические проявления пигментной ксеродермы.
Для подтверждения диагноза проведена биопсия кожи с целью оценить репарацию ДНК и чувствительность к ультрафиолетовому излучению фибробластов кожи. Результаты этого теста подтвердили диагноз пигментной ксеродермы. Несмотря на соответствующие профилактические меры, в возрасте 15 лет у ребенка развилась метастатическая меланома, и через 2 года он умер. У его родителей есть два других ребенка; ни один из них не болен пигментной ксеродермой.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Публикации в СМИ
Ксеродерма пигментная
Пигментная ксеродерма — группа наследственных заболеваний, вызванных нарушением системы эксцизионной репарации ДНК, протекающих с различными симптомами поражения кожи, фоточувствительностью, злокачественными новообразованиями.
Генетические аспекты. Типы и гены: • тип A, XPA, 278700, 9q22.3 q31; • тип B, ERCC3, XPB, 133510, 2q21; • тип C, XPC, XPCC, 278720, 3p25; • тип D, 278730, ERCC2, EM9 (126340, 19q13.2 q13.3); • тип E, 278740, DDB2 (600811, 11p12 p11); • тип E, подтип 2, DDB1 (600045, 11q12 q13); • тип F, XPF, 278760, 16p13.2 p13.1; • тип G, 278780, ERCC5, XPG (133530, 13q33); • 278800 Синдром де Санктиса; • 278810 Пигментная ксеродерма типа I.
Клиническая картина. Различные типы могут отличаться по срокам проявления и выраженности отдельных признаков. Начало заболевания на первом году жизни в виде сыпи на открытых участках кожи, сопровождаемой многочисленными пигментированными пятнами, напоминающими веснушки • Более выраженные атрофические изменения приводят к появлению очагов глянцевой истончённой кожи с телеангиэктазиями вокруг них • Распространённый кератоз, обусловленный солнечным воздействием (выраженная чувствительность кожи к инсоляции) и подвергающийся малигнизации (возможны множественные очаги эпителиом, рака кожи) • Кератиты, конъюнктивиты, эктропион, фотофобия • Снижение интеллекта • Микроцефалия • Нейросенсорная тугоухость • Снижение сухожильных рефлексов • Спастичность • Атаксия • Хореоатетоз.
Профилактика — избегать инсоляции, пользоваться солнцезащитными кремами.
Лечение. Предотвратить прогрессирование процесса нельзя, малигнизация наступает в 100% случаев. Проводят крио- или лазерную деструкцию папилломатозных разрастаний, кератом.
Синдром де Санктиса (#278800, r ) — фенотип, который может проявиться у пациентов с любым из типов пигментной ксеродермы, хотя его наиболее часто регистрируют при пигментной ксеродерме типа D. Клиническая картина: фоточувствительность кожи, ранние случаи рака кожи, пойкилодермия, пигментация кожи, атрофия кожи, телеангиэктазии, кератоакантоматоз, фотофобия, кератит, эктропион, энтропион, умственная отсталость, микроцефалия, нейросенсорная тугоухость, гипорефлексия/арефлексия, спастичность, атаксия, хореоатетоз, карликовость.
Методы исследования • Лабораторный метод: нарушение эксцизионной репарации ДНК после УФО; существует вариант заболевания, при котором нарушена рекомбинационная репарация ДНК • Специальный метод: исследование кожной чувствительности к УФО с применением монохроматора.
МКБ-10 • Q82.1 Ксеродермия пигментная.
Код вставки на сайт
Ксеродерма пигментная
Пигментная ксеродерма — группа наследственных заболеваний, вызванных нарушением системы эксцизионной репарации ДНК, протекающих с различными симптомами поражения кожи, фоточувствительностью, злокачественными новообразованиями.
Генетические аспекты. Типы и гены: • тип A, XPA, 278700, 9q22.3 q31; • тип B, ERCC3, XPB, 133510, 2q21; • тип C, XPC, XPCC, 278720, 3p25; • тип D, 278730, ERCC2, EM9 (126340, 19q13.2 q13.3); • тип E, 278740, DDB2 (600811, 11p12 p11); • тип E, подтип 2, DDB1 (600045, 11q12 q13); • тип F, XPF, 278760, 16p13.2 p13.1; • тип G, 278780, ERCC5, XPG (133530, 13q33); • 278800 Синдром де Санктиса; • 278810 Пигментная ксеродерма типа I.
Клиническая картина. Различные типы могут отличаться по срокам проявления и выраженности отдельных признаков. Начало заболевания на первом году жизни в виде сыпи на открытых участках кожи, сопровождаемой многочисленными пигментированными пятнами, напоминающими веснушки • Более выраженные атрофические изменения приводят к появлению очагов глянцевой истончённой кожи с телеангиэктазиями вокруг них • Распространённый кератоз, обусловленный солнечным воздействием (выраженная чувствительность кожи к инсоляции) и подвергающийся малигнизации (возможны множественные очаги эпителиом, рака кожи) • Кератиты, конъюнктивиты, эктропион, фотофобия • Снижение интеллекта • Микроцефалия • Нейросенсорная тугоухость • Снижение сухожильных рефлексов • Спастичность • Атаксия • Хореоатетоз.
Профилактика — избегать инсоляции, пользоваться солнцезащитными кремами.
Лечение. Предотвратить прогрессирование процесса нельзя, малигнизация наступает в 100% случаев. Проводят крио- или лазерную деструкцию папилломатозных разрастаний, кератом.
Синдром де Санктиса (#278800, r ) — фенотип, который может проявиться у пациентов с любым из типов пигментной ксеродермы, хотя его наиболее часто регистрируют при пигментной ксеродерме типа D. Клиническая картина: фоточувствительность кожи, ранние случаи рака кожи, пойкилодермия, пигментация кожи, атрофия кожи, телеангиэктазии, кератоакантоматоз, фотофобия, кератит, эктропион, энтропион, умственная отсталость, микроцефалия, нейросенсорная тугоухость, гипорефлексия/арефлексия, спастичность, атаксия, хореоатетоз, карликовость.
Методы исследования • Лабораторный метод: нарушение эксцизионной репарации ДНК после УФО; существует вариант заболевания, при котором нарушена рекомбинационная репарация ДНК • Специальный метод: исследование кожной чувствительности к УФО с применением монохроматора.
МКБ-10 • Q82.1 Ксеродермия пигментная.
Содержание
Дерматология в России
Зарегистрируйтесь!
Если Вы врач, то после регистрации на сайте Вы получите доступ к специальной информации.
Если Вы уже зарегистрированы, введите имя и пароль (форма в верхнем правом углу или здесь).
Пигментная ксеродерма
Пигментная ксеродерма
Введение
Вовлечённые группы населения также были описаны в Северной Африке и на Ближнем Востоке с менее хорошо изученной частотой 1.
XP был впервые описан в 1874 году дерматологом Моризом Капоши на основе серии из четырех наблюдений за пациентами с тонкой, сухой кожей, морщинистостью, сетчатой пигментацией, небольшим расширением сосудов, стянутостью кожи и развитием опухолей на поражённой коже [5].
Спектр заболеваний был расширен последующими отчетами о случаях, включающими неврологические нарушения [6], а также тяжелую форму, характеризующуюся карликовостью, гипоплазией гонад и умственной отсталостью наряду с остальными признаками ХР [7].
Еще в 1926 году заболевание было признано врожденным и обусловленным крайней чувствительностью кожи к ультрафиолетовому ( UV ) спектру, что имеет явное значение в профилактических мерах по минимизации воздействия солнца [8].
Ранние исследования подтвердили важность ультрафиолетового излучения в патогенезе заболевания ХР [9].
Кливер и соавт. [10] описали дефектную репарацию ДНК в культивируемых фибробластах кожи, и последующие исследования показали, что клетки при XP не способны противостоять UV или использовать эксцизионную репарацию поврежденной ДНК ультрафиолетовым излучением 14.
XP-вариант был охарактеризован Берком и соавт. [15] и Кливером и соавт. [16] как форма XP с ненарушенной эксцизионой репарацией ДНК.
Дальнейшие исследования показали неоднородность молекулярных нарушений, составляющих патогенез XP [17], выявив различные формы XP с различными дефектами, которые в сочетании могут комплексно усиливать дефекты репарации ДНК, поврежденной ультрафиолетовым излучением.
Эта комплементарная особенность обосновала описание групп комплементации, различных подтипов XP с различными дефектами эксцизионной репарации ДНК [18].
Эти подтипы обобщены в таблице 1 и включают типы XP A-G и вариант XP (XPV). Дальнейшие исследования на протяжении многих лет выявили точные молекулярные механизмы, ответственные за типы комплемента [18].
Обсуждение
Процесс репарации повреждений ДНК, вызванных ультрафиолетовым излучением, был обобщен в недавнем обзоре DiGiovanna и соавт. [18].
Когда ДНК подвергается воздействию ультрафиолетового излучения, в результате образуются фотопродукты на основе нескольких нуклеиновых кислот, которые служат субстратом для репарации ДНК с помощью процесса эксцизионной репарации нуклеотидов (NER).
Поврежденная ДНК распознается в пределах активно транскрибируемых генов с помощью репарации, спаренной с транскрипцией (TCR), и в остальной части генома с помощью более медленной общей репарации генома генома (GGR). В пути TCR специализированные белки (продукты генов CSA и CSB) распознают аномальный сегмент и блокируют активность РНК-полимеразы II.
В пути GGR другой набор белков (DDB2, продукт гена XPE и продукты гена XPC) распознает аномально измененную ультрафиолетовым излучением ДНК, эффективно маркируя их для репарации.
Оба пути затем приводят к раскручиванию спирали ДНК в области поврежденной ДНК с помощью множества различных белков, включая две геликазы, ERCC3 и ERCC2, кодируемых генами XPB и XPD соответственно, и дополнительных белков, включая продукты генов XPA и XPG (ERCC5) и белок репликации A (RPA).
Эндонуклеазы XPF (ERCC4) и XPG (ERCC5) разрезают цепочку ДНК и удаляют небольшие фрагменты пораженного генома. Полученный дефект устраняется с использованием хорошо изученных путей синтеза ДНК, включающих ДНК-полимеразу и лигазы.
Мутации в любом из этих белков из TCR, GGR или общих NER-путей приводят к нарушениям в репарации ДНК.
Эти мутации привели к множественным клиническим синдромам, некоторые из которых имеют пересекающиеся признаки, включая XP, синдром Кокейна (CS), цереброокуло-лицево-скелетный синдром (COFS) и трихотиодистрофию (TTD), обобщенные в таблице 1.
Классический фенотип ХР проявляется в раннем детстве в виде веснушек в возрасте до 2 лет, сильного ожога после минимального пребывания на солнце и рака кожи, проявляющегося в раннем возрасте [1-3, 18-20].
Средний возраст первого появления рака кожи, по сообщениям, составляет 9 лет (возрастной диапазон 1-32 года) для немеланоцитарного рака кожи и 22 года для меланомы (возрастной диапазон 2-47 лет) [19].
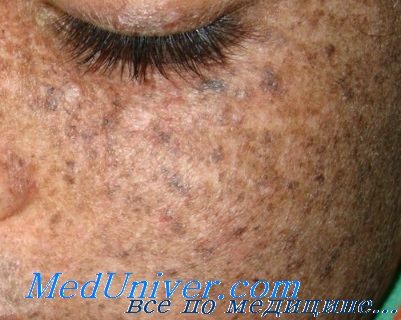
Кожа больных также подвергается преждевременному старению с прогрессирующей атрофией, сухостью, телеангиэктазиями и аномальной лентигинозной пигментацией со смешанными гипопигментированными и гиперпигментированными участками (рис. 1, 22).
Плоскоклеточный рак, базалиома и меланома встречаются у пациентов с ХР. Пациенты с ХР имеют >10 000-кратный риск развития немеланоцитарного рака кожи в течение жизни по сравнению с общей популяцией и >2000-кратный риск развития меланомы [19].
Этот повышенный риск развития рака приводит к снижению возраста на 58 лет развития первичного немеланоцитарного рака кожи, возникающего у пациентов с ХР, и к снижению возраста развития первичной меланомы на 33 года [19].
Эта закономерность противоположна той, которая наблюдается у пациентов без ХР, у которых более вероятно развитие меланомы в более раннем возрасте, чем немеланоцитарных опухолей кожи, а также предполагает, что механизмы злокачественной трансформации различны между меланоцитарным и немеланоцитарным раком кожи [18, 21].
Кроме того, по-видимому, существуют явные различия в меланоцитарных поражениях, наблюдаемых у пациентов с ХР, по сравнению с общей популяцией. Исследования секвенирования ДНК показали, что мутации PTEN встречаются гораздо чаще (53%) при меланомах при XP, чем в общей популяции (16%), и мутации PTEN характерны для изменений, вызванных ультрафиолетовым излучением [21].
Кроме того, невусы пациентов с ХР имеют несколько иную гистологию, чем типичные невусы, и у них также чаще встречаются мутации PTEN [21].
Не у всех пациентов развивается рак кожи, и в ретроспективном исследовании Брэдфорда и соавт. [19] в 33% сообщалось об отсутствии рака кожи.
В подгруппе пациентов с ХР сообщалось, что у них не было солнечных ожогов (около 38% в исследовании Брэдфорда), но у этих пациентов с большей вероятностью был диагностирован рак кожи в более раннем возрасте, чем у тех, у кого имелись ожоги кожи, вероятно, из-за более широкого использования профилактических мер против ожогов кожи, которые привели бы к снижению воздействия ультрафиолетового излучения [19].
Все дополнительные типы XP обладают фоточувствительностью и повышенным риском развития рака кожи, но между этими типами есть несколько различий.
Типы XPC, XPE и XP V были связаны с менее сильным солнечным ожогом после минимального пребывания на солнце, и они могут иметь нормальную, но все же чаще приобретать аномальную пигментацию [19, 22].
Нейродегенерация наблюдается не во всех типах одинаково, но чаще всего ассоциируется с типами XPA, XPB, XPD, XPF и XPG и редко с типами XPC и XPE [23].
Существует также большая вариабельность в группах сравнения из-за индивидуального воздействия ультрафиолетового излучения и профилактических мер.
XPC является наиболее распространена в Соединенных Штатах, Европе и Северной Африке, в то время как XPA является наиболее распространенным типом в Японии [19, 20].
Пациенты с XPV могут иметь повышенную долгосрочную выживаемость по сравнению с другими типами XP [25].
Пациенты с ХР имеют различные офтальмологические заболевания, так как передние отделы глаза также подвержены повышенному воздействию ультрафиолетового излучения.
В долгосрочном последующем исследовании Брукса и соавт. 91% пациентов с ХР сообщили о какой-либо глазной патологии [26].
Наиболее распространенные аномалии в исследовании включали конъюнктивит (51%), неоваскуляризацию роговицы (44%), сухость глаз (38%), рубцевание роговицы (26%), эктропион (25%), блефарит (23%), меланоз конъюнктивы (20%) и катаракту (14%).
У тринадцати процентов пациентов наблюдалась некоторая степень нарушения зрительной оси, а у 5% пациентов отсутствовало восприятие света в 1 или обоих глазах. Рак глаза или рак глаза в анамнезе присутствовали у 10% пациентов.
Другие патологии включают птеригиум, пингвукулу, кератит, выпадение ресниц, полосатую кератопатию, разрыв слоя Боумена, эпителиальную луковицу, катаракту, гамартому цилиарного тела, ирит, макулярный отек, хориоретинальные спайки, пигментную дегенерацию сетчатки с миграцией пигмента, цистоидную дегенерацию, глиоз, друзу и атрофию зрительного нерва [20, 26].
Центральная нервная система ( CNS ) поражается у значительной части пациентов с ХР [18, 20, 23].
CNS не подвергается прямому воздействию ультрафиолетового излучения, что делает механизм заболевания неясным, но в качестве возможной причины было предложено вероятное окислительное повреждение [23].
Нейродегенерация встречается примерно в 24% [19], включая утрату интеллектуального развития, нарушение неврологического статуса, нарушение слуха, нарушенную речь, арефлексию, атаксию, периферическую невропатию и потерю способности ходить и говорить.
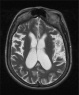
Эти недостатки коррелируют с потерей нейронов, атрофией коры головного мозга и расширением желудочков без воспаления, как видно из исследований изображений и патологического исследования. Наиболее пострадавшими группами являются пациенты с мутациями XPD и XPA [19].
Пациенты с ХР также имеют 50-кратный риск развития опухолей головного мозга, включая медуллобластому, глиобластому, астроцитому спинного мозга и шванному [18, 20].
У пациентов XP с нейродегенеративным заболеванием рак кожи развился в более раннем возрасте, чем у тех, у кого его нет (группы XPC и варианты) [19].
На рак кожи приходится наибольшее число смертей, связанных с заболеваниями, у пациентов с ХР, но нейродегенерация является второй по значимости причиной.
Среди пациентов с ХР у пациентов с нейродегенерацией был более ранний средний возраст смерти (29 лет) по сравнению с теми, у кого не было неврологической дегенерации (средний возраст смерти 37 лет) [19].
Пациенты с ХР, которые курят, имеют повышенный риск развития рака легких по сравнению с общей популяцией, среди других видов рака, поскольку компоненты сигаретного дыма обладают мутагенными эффектами, аналогичными ультрафиолетовому излучению [18].
Рак кожи также может возникать в необычных местах, которые подвергаются меньшему воздействию ультрафиолетового излучения, включая язык.
Африканские и афроамериканские пациенты с ХР имели такие же показатели заболеваемости раком, как и белые, не являющиеся латиноамериканцами, в одном исследовании [19] и имеют повышенный риск развития рака кожи в передней части языка.
Наиболее частой причиной смерти у пациентов с ХР является рак кожи, чаще всего из-за метастатической меланомы или инвазивной плоскоклеточной карциномы [19].
Overlap и связанные с ним синдромы, которые имеют общие черты с XP, также выявили информацию о различных ролях генов, вовлеченных в процесс NER.
Синдром Кокейна (CS) возникает в результате мутаций в генах CSA или CSB, которые, помимо роли в пути NER, также, по-видимому, играют роль в общих процессах транскрипции и, возможно, в поддержании функции митохондрий. CS характеризуется низким ростом с микроцефалией, пигментной дегенерацией сетчатки, кифосколиозом, дефектами походки, нейросенсорной глухотой и отчетливыми чертами лица, включая глубоко посаженные глаза, оттопыренные уши и морщинистый внешний вид [27].
Было описано несколько типов.
Трихотиодистрофия характеризуется аномальными волосами, нарушением интеллекта, снижением фертильности, низким ростом и ихтиозом [27].
Фоточувствительность обычно присутствует и связана с мутациями генов XPD, XPB, TTDA, но не с мутациями TTDN1. Подобно CS, TTD не имеет повышенной ассоциации со злокачественными новообразованиями или аномальной пигментацией.
Ломкие волосы при TTD не содержат серы и имеют полосатый светлый и темный вид при поляризационной световой микроскопии. Кроме того, как и в случае с CS, считается, что аномальные неврологические особенности обусловлены аномальным развитием миелина и нарушениями транскрипции, без неврологического ухудшения, наблюдаемого при XP.
Нейровизуализация показывает дисмиелинизацию, но также может показать корковые гетеротопии, частичную агенезию мозолистого тела, перимедуллярный фиброз спинного мозга и внутричерепную кальцификацию [27].
Были задействованы множественные мутации в системе NER, в основном с участием пути TCR, включая гены CSB, XPD, XPG и ERCC1 [28].
В настоящее время не существует лекарства от пигментной ксеродермы, но существует огромная польза в постоянной защите от ультрафиолетового излучения, которая может существенно снизить количество случаев рака кожи; рекомендуются многослойная одежда наряду с солнцезащитным кремом и защитой глаз [21].
Уменьшение воздействия ультрафиолетового излучения может не уменьшить нейродегенеративные эффекты. Пациентам часто требуется препарат витамина D, чтобы компенсировать избегание солнца [21].
Была предпринята попытка системного лечения ретиноидами, и оно показало некоторую пользу в снижении числа случаев рака кожи [29], хотя побочные эффекты запрещают применение их у детей.
Ранняя резекция предраковых и злокачественных поражений важна для долгосрочной выживаемости. Исследовательские методы лечения с использованием генной терапии и антиоксидантов для уменьшения окислительного повреждения могут лечь в основу будущих вариантов лечения [30].
Вывод
Ранняя диагностика и профилактические меры могут значительно улучшить качество и продлить жизнь пациентов.