Ламизил и тербинафин в чем разница
Ламизил : инструкция по применению
Состав
1 г крема содержит:
Вспомогательные вещества: бензиловый спирт, натрия гидроксид, сорбитан стеарат, цетилпальмитат, стеариловый спирт, цетиловый спирт, полисорбат 60, изопропилмиристат, вода очищенная.
Описание
Белый однородный или почти однородный, глянцевый крем со слабым характерным запахом.
Противогрибковые средства для лечения заболеваний кожи. Прочие противогрибковые средства для местного применения. Код ATX: D01AE15.
Противогрибковый препарат для местного применения, обладающий широким спектром противогрибковой активности.
В небольших концентрациях тербинафин оказывает фунгицидное действие в отношении дерматофитов (Trychophyton rubrum, T. mentagrophytes, T. verrucosum, T. violaceum, T. tonsurans, Microsporum canis, Epidermophyton floccosum), плесневых (в основном C.albicans) и определенных диморфных грибов (Pityrosporum orbiculare).
Активность в отношении дрожжевых грибов, в зависимости от их вида, может быть фунгицидной или фунгистатической.
Тербинафин специфическим образом изменяет ранний этап биосинтеза стеролов, происходящего в грибах. Это ведет к дефициту эргостерола и к внутриклеточному накоплению сквалена, что вызывает гибель клетки гриба. Действие тербинафина осуществляется путем ингибирования фермента скваленэпоксидазы, расположенного на клеточной мембране гриба.
Тербинафин не оказывает влияния на систему цитохрома Р450 у человека и, соответственно, на метаболизм гормонов или других лекарственных препаратов.
Показания к применению
Грибковые инфекции кожи, такие как дерматомикозы стоп (tinea pedis или «грибок» стопы), паховый дерматомикоз (tinea cruris), микозы гладкой кожи тела (tinea corporis), вызванные дерматофитами, такими как Trichophyton (в том числе, Т. rubrum, Т. mentagrophytes, Т. verrucosum, Т. violaceum), Microsporum canis, Epidermophyton floccosum.
Дрожжевые инфекции кожи, в основном те, которые вызываются родом Candida (например, Candida albicans), в частности опрелости.
Разноцветный лишай (Tinea versicolor), вызываемый Pityrosporum orbiculare (также известный под названием Malasseziafurfur).
Противопоказания
Повышенная чувствительность к тербинафину или к любому из неактивных ингредиентов, входящих в состав препарата.
Способ применения и дозы
Наружно. Взрослым и детям в возрасте старше 12 лет.
Перед нанесением крема необходимо очистить и подсушить пораженные участки. Крем наносят один или два раза в сутки тонким слоем на пораженную кожу и прилегающие участки и слегка втирают. При инфекциях, сопровождающихся опрелостью (под молочными железами, в межпальцевых промежутках, между ягодицами, в паховой области), места нанесения крема можно прикрывать марлей, особенно на ночь.
Средняя продолжительность лечения
| Дерматомикоз стоп (межпальцевая область) | 1 неделя 1 раз в день |
| Дерматомикоз стоп «мокасинового типа» | 2 недели 2 раза в день |
| Паховый дерматомикоз, микозы гладкой кожи тела | 1 неделя 1 раз в день |
| Дрожжевые инфекции кожи (кандидоз кожи) | 1 неделя 1-2 раза в день |
| Разноцветный лишай | 2 недели 1-2 раза в день |
Уменьшение выраженности клинических проявлений обычно отмечается в первые дни лечения. В случае нерегулярного лечения или преждевременного его прекращения существует риск возобновления инфекции. В случае если через одну-две недели лечения не отмечается признаков улучшения, следует обратиться к врачу.
Режим дозирования крема Ламизил у лиц пожилого возраста
Не отличается от вышеописанного.
Применение препарата у детей
Опыт применения крема Ламизил у детей в возрасте до 12 лет ограничен. В связи с этим не рекомендуется применение данного препарата у детей до 12 лет.
Применение во время беременности и грудного вскармливания
В экспериментальных исследованиях тератогенных свойств тербинафина выявлено не было. До настоящего времени не сообщалось о каких-либо пороках развития при применении Ламизила. Однако, поскольку клинический опыт применения Ламизила у беременных женщин очень ограничен, его следует применять только по строгим показаниям.
Тербинафин выделяется с грудным молоком. Не следует применять Ламизил крем в период грудного вскармливания.
В местах нанесения препарата может появиться покраснение, ощущение зуда или жжения, шелушение кожи, боль или раздражение, однако прекращение лечения по причине данных явлений требуется редко. Эти не столь серьезные побочные явления следует отличать от редко возникающих аллергических реакций (например, генерализованная сыпь и/или покраснение, крапивница, ангионевротический отек, повторная аллергическая реакция), развитие которых требует прекращения лечения. В редких случаях возможно обострение грибковой инфекции.
В случае возникновения нежелательного явления, даже если оно не упомянуто выше, следует сообщить лечащему врачу.
О случаях передозировки препарата не сообщалось. Если же случайно крем Ламизил будет принят внутрь, можно ожидать развития таких же побочных явлений, как и при передозировке таблеток Ламизил (головная боль, тошнота, боли в эпигастрии и головокружение).
Взаимодействия с другими лекарственными средствами
Какие-либо лекарственные взаимодействия для крема Ламизил не известны.
Меры предосторожности
Ламизил крем предназначен только для наружного применения. Следует избегать попадания крема в глаза, так как он может вызвать раздражение. При случайном попадании препарата в глаза, их следует немедленно промыть проточной водой, а в случае развития стойких явлений раздражения необходимо проконсультироваться с врачом.
Ламизил крем содержит цетиловый спирт и стеариловый спирт, которые могут вызвать раздражение кожи в месте нанесения.
Влияние на способность управлять автотранспортом и работать с механизмами
Крем Ламизил не влияет на способность управлять автомобилем и работать с механизмами.
Упаковка
По 15 г или 30 г в ламинированной тубе с защитной мембраной и крышкой из полипропилена. Туба с инструкцией по применению упакована в картонную пачку.
Срок годности
3 года. Не использовать после истечения срока годности.
Условия хранения
3 года. Не использовать после истечения срока годности.
Фармакотерапевтическая группа
3 года. Не использовать после истечения срока годности.
Способ применения и дозы
3 года. Не использовать после истечения срока годности.
Сопоставимость брендов и дженериков на примере Ламизила (тербинафина)
Интересно проследить сопоставимость брендов и дженериков на примере Ламизила (тербинафина), синтезированного в 1983 г. фирмой Novartis Farma (Швейцария). Сегодня препарат зарекомендовал себя во всем мире как надежный системный антимикотик, эффективность которого составляет 93-100%. Это объясняется его двойным действием: фунгистатическим и преобладающим фунгицидным.
Фунгицидное действие Ламизила связано с накоплением скваленов в микотической клетке благодаря тому, что препарат препятствует их дальнейшему превращению. Сквалены, накапливаясь внутри клеток, еще больше ухудшают состояние клеточных мембран, экстрагируя из них липидные компоненты. Одновременно увеличивается объем липидных гранул, что в конце концов ведет к разрыву ослабленной клеточной стенки и гибели грибковой клетки. Фунгицидное действие Ламизила превосходит фунгистатическое. Этот процесс схематически показан на рис.
По данным литературы, Ламизил лучше своих аналогов по таким параметрам, как скорость достижения клинического и микологического излечения, доля полностью излеченных пациентов через 1 год от начала терапии, частота побочных эффектов (на примере Экзифина).
В процессе лечения больные ежемесячно проводили дезинфекцию обуви формалином. Все пациенты переносили лечение удовлетворительно. Лишь в одном случае в течение 5 дней была отмечена тошнота и в 1-м периодически появлялись запоры. Через 3-4 недели у всех больных кожа ладоней и подошв нормализовалась. Спустя 18 недель от начала терапии клиническое и микологическое излечение ногтевых пластинок было достигнуто у 34 больных, а у 4-х ногтевые пластинки больших пальцев стоп оставались на 1/3-1/4 длины измененными, микологическое излечение также не было достигнуто. Наблюдение за ними продолжалось еще 6 месяцев, и через 3 месяца у всех 4-х больных без дополнительного лечения ногтевые пластинки больших пальцев стоп отросли полностью здоровыми. Спустя 18-24 месяца после окончания лечения удалось обследовать 30 пациентов (мы не выявили ни одного случая клинического или микологического рецидива онихомикоза и/или микоза стоп или ладоней). Все больные были полностью удовлетворены проведенным лечением.
У 1-го ребенка применение Ламитера в течение 2-х месяцев оказалось неэффективным и еще у 1-го терапия была прекращена на 5-й неделе ввиду плохой переносимости препарата (тошнота, рвота, боли в желудке). Окончательное клиническое и микологическое излечение было достигнуто у всех детей, получавших Ламизил, спустя 9-13 недель от начала терапии. Лечение Ламитером привело к клиническому и микологическому излечению 16 из 19 детей в сроки от 11 до 16 недель.
| Препарат | 4-я нед. | 5-я нед. | 6-я нед. | 7-я нед. | 8-я нед. | Неудача в лечении | Лече- ние прек- ращено |
| Ламизил (10 больных) | 0 | 2 | 4 | 4 | |||
| Ламитер (19 больных) | 0 | 0 | 4 | 8 | 4 | 2 | 1 |
Таким образом, лечение Ламизилом оказалось более эффективным, чем его дженериковыми формами, как у больных микозами стоп и онихомикозами, так и микроспорией.
_______________________
Вы читаете тему: Использование оригинальных антимикотиков и дженериков в лечении микозов кожи, волос и ногтей (Панкратов В. Г. БГМУ. «Медицинская панорама» № 6, июнь 2005)
Дженерики тербинафина в России: взгляд практического миколога
Ключевые слова: оригинальные лекарственные средства, дженерики, тербинафин, Экзифин.
TERBINAFINE GENERICS IN RUSSIA: A PRACTICAL MYCOLOGIST’S OPINION
E.I. Kasikhina, N.V. Savchenko
Russian Medical Academy of Postgraduate Education, Ministry of Health and Social Development of the Russian Federation, Medico-C Medical Center, Moscow
Key words: original drugs, generics, terbinafine, Exifine.
В настоящее время фармацевтический рынок предлагает большой выбор антимикотиков. В этом изобилии нелегко разобраться даже специалисту-микологу при условии, что вся информация достойна доверия и действительно имела место в практике. Одной из частых и нередко болезненных задач, стоящих перед врачом, является выбор между оригинальным лекарственным средством и воспроизведенным препаратом (дженериком). Дженерик — лекарственный продукт, обладающий доказанной терапевтической взаимозаменяемостью с оригинальным инновационным лекарственным средством аналогичного состава, выпускаемый не разработчиком оригинального препарата и без лицензии разработчика. Облегченные правила регистрации и более низкая цена способствуют распространению дженериков на фармацевтическом рынке. В России объем продаж достигает 80%, в Канаде — 64%, в Японии — 30% [1]. В Испании более 20% препаратов, выписанных врачами разных специальностей, являются дженериками [2]. Список дженериков системных антимикотиков в России ежегодно пополняется и насчитывает десятки наименований. Фактически на отечественном фармакологическом рынке представлены аналоги каждого оригинального системного антимикотика, а перечень наименований наружных форм антимикотиков еще более широк. Сложившаяся ситуация с дженериками характерна не только для России. В странах Центральной и Восточной Европы, Юго-Восточной Азии, Индии и Китае дженерики известных противогрибковых средств — довольно распространенное явление. В США и ряде стран Западной Европы еще сохраняется господствующее положение оригинальных препаратов, но и оно сдает свои позиции [3].
Как правило, регистрация дженериков допускается на основании оценки регистрационного досье сокращенного объема и данных биоэквивалентности Воспроизведенный аналог содержит то же действующее вещество, что и оригинальный препарат, но, как правило, отличается от него вспомогательными веществами. Лекарственные препараты считаются фармацевтически эквивалентными, если содержат одни и те же активные субстанции в одинаковом количестве (допустимое отличие — не более 5%) и в одинаковой лекарственной форме, а также отвечают требованиям одних и тех же сходных стандартов. Согласно положению Всемирноорганизациздравоохранения, «два препарата считают эквивалентными, если они фармацевтически эквивалентны, имеют одинаковую биодоступность и при назначении в одинаковой дозе обеспечивают должную эффективность и безопасность». По определению FDA, фармацевтически эквивалентные лекарственные препараты содержат одинаковые ингредиенты в одинаковой лекарственной форме, предназначены для одного способа введения и являются идентичными по силе действия или концентрации активных веществ [3, 4].
В микологии данное положение должно относиться к препаратам, используемым как системно, так и наружно, так как не все пациенты микологического профиля могут получать системное лечение. Отсутствие подтверждения терапевтической эквивалентности порождает сомнения в качестве воспроизведенного препарата и может ограничить использование дженериков в ситуациях, когда врач рассчитывает на максимальную надежность и безопасность лекарственного средства. К таким ситуациям относится терапия микозов у детей и пожилых людей с отягощенным соматическим анамнезом (прежде всего эндокринной патологией). Именно в этих возрастных группах вопросы безопасности наиболее значимы, и используемый препарат должен подтвердить свою состоятельность не только в фармакологическом, но и в клиническом аспекте.
Безусловно, на окончательный выбор препарата влияют разные факторы [5]. Во-первых, оценка врачом-микологом клинической ситуации и его клинический опыт. Во-вторых, пациент имеет право на выбор оригинального препарата или дженерика, при этом выбор должен быть информированным. Поскольку информацию должен предоставлять врач, то и он должен ориентироваться на качественные сведения о препаратах. К сожалению, для большинства дженериков противогрибковых препаратов не проводилось всего комплекса исследований, которые легли в основу современных схем используемых оригинальных препаратов. Сведения о результатах исследований, которые производители указывают в информационных материалах, в подавляющем большинстве случаев относятся к оригинальному препарату. Финансовые затруднения пациента или недоступность оригинала по тем или иным причинам служат основанием для назначения дженерика. При этом следует ориентироваться на воспроизведенные аналоги, которые давно существуют на рынке или имеют свою доказательную базу эффективности и безопасности. Например, среди известных дерматологам дженериков тербинафина такой базой владеют Экзифин, термикон, фунготербин. Информация о доказанной фармацевтической эквивалентности препаратов упоминается в немногочисленных отечественных публикациях, посвященных клинической эффективности таких дженериков флуконазола, как микофлюкан и флюкостат. В-третьих, велика роль аптечного звена, нередко выступающего в качестве «первичного звена» дерматологической помощи населению, или «корректора» врачебных назначений.
Итак, фармакокинетическая эквивалентность является главным условием регистрации препарата-дженерика. Биоэквивалентные препараты имеют сходные показатели биодоступности при исследовании в одинаковых экспериментальных условиях. Исследования биоэквивалентности проводят на ограниченном контингенте здоровых добровольцев с помощью рандомизированного перекрестного метода. Данные о биоэквивалентности используемых в других странах дженериков тербинафина оригинальному препарату можно без труда получить из зарубежных научных публикаций [6—8]. В нашей стране мы сталкиваемся в основном с данными сравнительных исследований, оценивающих терапевтическую эквивалентность системных препаратов или дающих фармакоэкономическую оценку антимикотикам [9].
Для определения биоэквивалентности сравнивают так называемую площадь под фармакокинетической кривой (AUC) «концентрация—время». Препарат-дженерик считается биоэквивалентным оригинальному, если 90% средней AUC вещества входит в диапазон от 80 до 125% от средней AUC оригинального препарата [6].
Примером может служить характер фармакокинетических кривых, полученных после приема препаратов Экзифин и ламизил, который в целом сходен, причем индивидуальная вариабельность концентраций тербинафина в обоих случаях примерно одинаковая. Усредненные фармакокинетические профили тербинафина в сыворотке крови больных, принимавших препараты Экзифин и ламизил (рисунок) характеризовались сходными кривыми, причем во всех временных точках различия между соответствующими значениями концентрации не были статистически достоверными. Среднее значение максимальной концентрации тербинафина после приема испытуемого препарата и скорость ее достижения достоверно не отличались от этих параметров препарата сравнения. Площадь под кривой «концентрация-время» (AUC24h) для Экзифина была незначительно меньше, чем для ламизила. Разница в значениях среднего времени удерживания также была незначительной (в среднем 11,6 и 12,2 ч соответственно). Данное исследование биоэквивалентности препаратов Экзифин (дженерик) и ламизил (оригинальный тербинафин) выполнено открытым методом по перекрестной и рандомизированной схеме у больных с онихомикозами, обусловленными T. rubrum. Испытания препаратов проводили в соответствии с программой изучения биоэквивалентности, утвержденной Фармакологическим государственным комитетом МЗ РФ на базе Уральского научно-исследовательского института дерматовенерологии и иммунопатологии Минздрава России [10].
Пример «соответствия» фармакокинетических профилей тербинафина в сыворотке в крови больных, принимавших Экзифин (1) и ламизил (2; нг/мл).
Параметры биодоступности тербинафина после приема препаратов Экзифин и ламизил
Одной из важнейших фармацевтических характеристик препарата является точность его дозирования. Для обеспечения точности (однородности) дозирования и кинетики высвобождения активной субстанции из оральных таблетированных форм желательно применять современные технологии, которые требуют материальных затрат и делают производство экономически невыгодным. Регламентирующие нормы предписывают содержание действующих веществ по однородности дозирования в пределах 85—115% от номинала. Отличия процентного содержания антимикотика и примесей могут отражаться на переносимости препаратов, а также на их клинической эффективности. Как правило, остаются неизвестными показатели распределения дженериков в органах-мишенях, в частности конкретной концентрации дженериков в ногте и продолжительности их сохранения в нем [11]. Не учитываются также сравнительные статистические данные по побочным эффектам и осложнениям при применении оригинальных антимикотиков и их воспроизведенных аналогов. Нельзя сказать, что это способствует исключительно распространению дженериков. Напротив, отсутствие подтверждения терапевтической эквивалентности порождает сомнения в качестве воспроизведенного препарата и может ограничить использование дженериков, когда врач рассчитывает на максимальную надежность и безопасность лекарственного средства. Конечно, требовать от производителей дженериков того же комплекса фармакологических и клинических исследований, который необходим для регистрации оригинального препарата, нельзя. С другой стороны, это обычное явление в странах Европы и Юго-Восточной Азии [6—8, 12]. Во Франции предложен метод спектроскопии для определения терапевтической эквивалентности дженериков топических антимикотиков с целью оценки не только проникающей способности препарата, но и контроля повреждения барьерных слоев эпидермиса [13]. Внедрение дженериков в клиническую практику не может осуществляться без проведения исследований, подтверждающих их реальное, а не номинальное соответствие эффективности и безопасности оргинальному препарату.
В «досье» старейшего в России дженерика тербинафина Экзифина (на отечественном фармакологическом рынке с 1999 г.), практический миколог может найти ответы на многие вопросы. Так, применение Экзифина у пациентов с аллергодерматозами изучали на базе ГНЦ Институт иммунологии ФМБА России, а также на кафедре кожных и венерических болезней Московского государственного медико-стоматологического университета [14, 15]. Полученные данные клинико-лабораторного исследований свидетельствуют об эффективности и безопасности Экзифина в комплексной терапии больных атопическим дерматитом с гиперчувствительностью к грибам рода Malassezia, что выражалось в быстром купировании зуда и положительной динамике индекса SCORAD. Клинические исследования по применению Экзифина при микроспории волосистой части головы проводились на базе Уральского НИИ дерматовенерологии и иммунопатологии, при этом этиологическая эффективность препарата составила 92,9%, побочные эффекты отмечались в 5,4% случаев [16]. На базе НИИ медицинской микологии им. П.Н. Кашкина ГОУ ДПО СПб МАПО изучали эффективность и безопасность Экзифина у больных онихомикозом стоп на фоне соматических заболеваний с нарушением кровообращения в нижних конечностях [17].
Таким образом, клиническая практика расставляет все препараты по своим местам. Это расширяет врачебный выбор, что в значительной степени является «шагом вперед на пути к совершенствованию противогрибковой терапии». Безусловно, воспроизведенные препараты позволяют врачам стремиться лечить всех и хорошо даже в экономически слабых странах, при этом используя самые современные дженерики дорогих оригинальных препаратов. С другой стороны, давление дженериков на рынке является одним из факторов, заставляющих компании производить оригинальные препараты и активнее внедрять новые перспективные разработки.
Современные методы лечения онихомикоза
Онихомикоз является наиболее распространенным заболеванием ногтей. Установлено, что 50 % случаев изменений ногтевых пластинок связано с микотической инфекцией. Эпидемиологические исследования, проведенные в России и зарубежных странах, выявили высокую з
Онихомикоз является наиболее распространенным заболеванием ногтей. Установлено, что 50 % случаев изменений ногтевых пластинок связано с микотической инфекцией. Эпидемиологические исследования, проведенные в России и зарубежных странах, выявили высокую заболеваемость онихомикозом, которая составила в общей популяции населения от 2 до 13 % [1, 2, 3]. Риск развития онихомикоза наиболее высок у больных старшего возраста. Например, у людей старше 70 лет распространенность онихомикоза стоп может составлять 50 % и выше [2, 4, 5]. Считается, что этому способствуют медленный рост ногтевых пластинок, нарушения периферического и магистрального кровообращения у лиц пожилого возраста [6]. Высокую частоту онихомикоза выявляют также у больных с иммунодефицитными состояниями (в том числе у больных СПИДом) и у больных сахарным диабетом [6, 7, 8].
Часто больные и некоторые врачи воспринимают онихомикоз как исключительно эстетическую проблему. Однако это серьезное заболевание, которое протекает хронически и в случаях возникновения иммунодефицитного состояния, декомпенсации эндокринных заболеваний может стать причиной развития распространенного микоза кожи и ее придатков. Нередко онихомикоз сопровождается развитием тяжелых осложнений, например диабетической стопы, хронического рожистого воспаления конечностей, лимфостаза, элефантиаза [9, 10]. У больных, получающих цитостатическую или иммуносупрессивную терапию, болезнь может стать причиной развития инвазивных микозов. Вот почему лечение онихомикоза является необходимым и должно проводиться своевременно [11].
Всего несколько десятилетий назад лечение онихомикоза было трудоемким, длительным и малоперспективным. Лекарственные препараты, применявшиеся для лечения грибковых заболеваний кожи и ее придатков, отличались низкой эффективностью и высокой токсичностью. Для достижения положительного результата требовалось длительное лечение или увеличение дозы препаратов, что нередко сопровождалось тяжелыми осложнениями. Некоторые методы лечения были потенциально опасны для жизни пациентов. Например, рентгенотерапия, применение таллия и ртути приводили к развитию у пациентов онкологических заболеваний кожи, заболеваниям головного мозга и внутренних органов.
Появление высокоэффективных и малотоксичных антимикотических препаратов значительно облегчило лечение грибковых заболеваний кожи и ее придатков. Однако результаты применения новых антимикотиков оказались недостаточно удовлетворительными. Контролируемые клинические испытания показали, что эффективность применения системных антимикотиков после окончания лечения составляет от 40 до 80 %, а через 5 лет — от 14 до 50 % [12]. В то же время эффективность терапии онихомикоза повышается при применении комплексных методов лечения, которые предусматривают использование этиотропных препаратов и средств, влияющих на звенья патогенеза [13]. Также в результате клинических испытаний, проведенных в странах Европы, было установлено, что эффективность лечения онихомикоза можно повысить в среднем на 15 % при сочетанном применении антимикотиков системного действия и антифунгального лака, содержащего аморолфин [14].
Лечение
Аллиламины являются синтетическими антимикотиками. Аллиламины преимущественно действуют на дерматомицеты, при этом они оказывают фунгицидное действие. Механизм их действия заключается в ингибировании фермента скваленэпоксидазы, которая принимает участие в синтезе эргостерола — основного структурного компонента клеточной мембраны дерматомицетов. К аллиламинам относятся тербинафин и нафтифин.
Аллиламины активны в отношении большинства дерматомицетов (Epidermophyton spp., Trichophyton spp., Microsporum spp., Malassezia spp.), возбудителя хромомикоза и некоторых других грибов.
Показаниями для назначения тербинафина внутрь являются онихомикоз, распространенные формы дерматомикозов кожи, микоз волосистой части головы, хромомикоз. Показаниями для наружного применения тербинафина и нафтифина служат ограниченное поражение кожи при микозах, отрубевидный лишай, кандидоз кожи. Тербинафин обладает высокой биодоступностью, хорошо всасывается в ЖКТ независимо от приема пищи. В высоких концентрациях препарат накапливается в роговом слое кожи, ногтевых пластинках, волосах, выделяется с секретами потовых и сальных желез. Абсорбция тербинафина при местном применении составляет менее 5 %, нафтифина — 4–6 %. Концентрация тербинафина и нафтифина в коже и ее придатках значительно превышает МПК для основных возбудителей дерматомикозов. Коррекция режима дозирования тербинафина может потребоваться при сочетанном назначении его с индукторами (рифампицин) или ингибиторами микросомальных ферментов печени (циметидин), так как первые повышают его клиренс, а вторые его понижают.
В результате многочисленных контролируемых многоцентровых сравнительных клинических испытаний было установлено, что тербинафин является наиболее эффективным антимикотиком в терапии онихомикоза [12] (табл. 1).
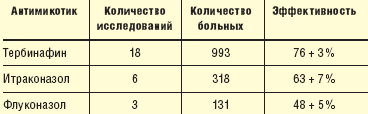 |
| Таблица 1. Сравнительная эффективность антимикотиков в терапии онихомикоза (по результатам метаанализа 27 рандомизированных исследований) |
Тербинафин применяют при распространенном поражении кожи, онихомикозе, хромомикозе, в таких случаях тербинафин назначают перорально. Тербинафин является препаратом выбора в терапии онихомикоза, так как наиболее эффективен по отношению к основных возбудителям онихомикоза — дерматомицетам. Противопоказаниями для назначения аллиламинов являются аллергические реакции на препараты группы аллиламинов, беременность, кормление грудью, возраст до 2 лет, заболевания печени, сопровождающиеся нарушением ее функции (повышением трансаминаз).
Азолы — самая многочисленная группа синтетических антимикотиков. В 1984 г. был внедрен в практику первый системный противогрибковый препарат из группы азолов — кетоконазол, в 1990 г. — флуконазол, в 1992 г. — итраконазол.
Азолы, применяемые в качестве системных препаратов, обладают преимущественно фунгистатической активностью. Важным преимуществом азолов перед другими препаратами является их широкий спектр противогрибковой активности. Итраконазол активен in vitro в отношении большинства возбудителей онихомикоза — дерматомицетов (Epidermophyton spp., Trichophyton spp., Microsporum spp.), Candida spp. (C. albicans, C. parapsilosis, C. tropicalis, C. lusitaniae и др.), Aspergillus spp., Fusarium spp., S. Shenckii и др. Флуконазол активен против дерматомицетов (Epidermophyton spp., Trichophyton spp., Microsporum spp.) и Candida spp. (C. albicans, C. parapsilosis, C. tropicalis, C. lusitaniae и др.), но не действует на Aspergillus spp., Scopulariopsis spp., Scedosporium spp.
Фармакокинетика у разных азолов различна. Флуконазол (90 %) хорошо всасывается в ЖКТ. Для хорошего всасывания итраконазола необходим нормальный уровень кислотности. Если у пациента, принимающего эти препараты, кислотность понижена, то всасываемость их уменьшается и, следовательно, снижается биодоступность. Всасываемость раствора итраконазола выше, чем у капсул с итраконазолом. Итраконазол в капсулах следует принимать с пищей, а в растворе — натощак.
Итраконазол метаболизируется в печени и выводится из организма через ЖКТ. В небольших количествах он также выделяется сальными и потовыми железами. Флуконазол метаболизируется частично и в основном выводится в неизмененном виде почками (80 %).
Итраконазол взаимодействует со многими лекарственными препаратами. Биодоступность кетоконазола и итраконазола уменьшается при приеме антацидов, холиноблокаторов, Н2-блокаторов, ингибиторов протонной помпы, диданозина. Итраконазол является активным ингибитором изоферментов цитохрома Р450 и может изменять метаболизм многих лекарственных препаратов. Флуконазол влияет на метаболизм лекарственных средств в меньшей степени. Недопустим прием азолов с терфенадином, астемизолом, цизапридом, хинидином, так как могут развиться смертельно опасные желудочковые аритмии. Совместный прием азолов и пероральных антидиабетических препаратов требует постоянного контроля за содержанием глюкозы в крови, так как может развиться гипогликемия. Прием непрямых антикоагулянтов группы кумарина и азолов может сопровождаться гипокоагуляцией и кровотечениями — следовательно, необходим контроль гемостаза. Итраконазол может повышать концентрацию в крови циклоспорина и дигоксина, а флуконазол — теофиллина и вызывать развитие токсического эффекта. Требуется корректировка доз и постоянный мониторинг за концентрацией препаратов в крови. Противопоказано совместное применение итраконазола с ловастатином, симвастатином, рифампицином, изониазидом, карбамазепином, циметидином, кларитромицином, эритромицином. Флуконазол не следует применять с изониазидом и терфенадином.
Итраконазол применяют при дерматомикозах (эпидермофитии, трихофитии, микроспории), отрубевидном лишае, кандидозе кожи, ногтей и слизистых оболочек, пищевода, кандидозном вульвовагините, криптококкозе, аспергиллезе, феогифомикозе, споротрихозе, хромомикозе, эндемичных микозах, для профилактики микозов при СПИДе.
Флуконазол применяется для лечения генерализованного кандидоза, всех форм инвазивного кандидоза, в том числе и у иммуноскомпрометированных больных, генитального кандидоза, кандидоза кожи, ее придатков и слизистых. Последнее время благодаря своей безопасности и хорошей переносимости все чаще флуконазол применяется для терапии больных дерматомикозами с поражением как кожи, так и ее придатков (ногтей и волос).
Аморолфин входит в состав лака, применяемого для лечения онихомикоза. Механизм действия аморолфина заключается в нарушении синтеза эргостерола — основного компонента клеточной мембраны гриба. Он оказывает фунгистатическое и фунгицидное действие. Обладает широким спектром действия. Концентрация аморолфина в ногтевой пластинке значительно превышает МПК для основных возбудителей дерматомикозов в течение 7 дней. Поэтому аппликация препарата может осуществляться не чаще 1–2 раз в неделю, что делает его применение экономически выгодным. Противопоказания: аллергические реакции на аморолфин, грудной и детский младший возраст. Лак в качестве монотерапии назначают при поражении не более 1–3 ногтевых пластинок и не более чем на 1/2 по площади с дистального конца. Также аморолфин можно использоваться в сочетании с системными антимикотиками при более распространенном поражении ногтей (табл. 2).
Циклопирокс обладает фунгистатическим действием. Активен в отношении дерматомицетов, дрожжеподобных и мицелиальных грибов, плесеней, а также некоторых грамотрицательных и грамположительных бактерий. Циклопирокс (лак) применяется в качестве монотерапии при поражении не более 1–3 ногтевых пластинок не более чем на 1/2 по площади с дистального конца. Также циклопирокс можно использовать в сочетании с системными антимикотиками при более распространенном поражении ногтей. Противопоказания: аллергические реакции на циклопирокс, грудной и младший детский возраст, беременность и лактация.
Перечень рекомендуемых лабораторных исследований при назначении системных антифунгальных препаратов.
Лечение фоновых заболеваний. Эффективность применения антимикотиков повышается при коррекции патологических состояний, способствовавших развитию онихомикоза. Перед началом антимикотической терапии у больных с соматическими, эндокринными, неврологическими заболеваниями, с нарушениями кровообращения в конечностях необходимо провести обследование для выявления основного симптомокомплекса, способствовавшего развитию дерматомикозов. Так, основными задачами патогенетической терапии являются улучшение микроциркуляции в дистальных отделах конечностей, венозного оттока конечностей, нормализация уровня тиреотропных гормонов у больных с заболеваниями щитовидной железы, углеводного обмена у больных сахарным диабетом и т. д. В результате многолетних исследований, проведенных в Военно-медицинской академии и Санкт-Петербургской медицинской академии последипломного образования, установлено, что одной из основных причин развития дерматомикозов являются нарушения со стороны системы гипофиз–гипоталамус–гонады. Это приводит к расстройству кровообращения в дистальных отделах конечностей, нарушениям микроциркуляции, периферической иннервации. Комплекс мероприятий, направленный на коррекцию этих нарушений, включает иглорефлексотерапию, транскраниальную электростимуляцию подкорковых центров головного мозга, назначение препаратов, корригирующих работу симпатической и парасимпатической вегетативной нервной системы. Все это позволяет добиться более быстрого клинического эффекта при терапии дерматомикозов. Проведение патогенетической терапии у больных дерматомикозами с фоновыми заболеваниями целесообразно назначать до начала этиотропного лечения и продолжать ее во время всего курса приема антифунгальных препаратов.
Симптоматическая терапия дерматомикозов, направленная на уменьшение субъективных жалоб больных и объективных проявлений заболевания, не может заменить этиотропную терапию. Однако ее применение в сочетание с антифунгальными препаратами позволяет быстрее добиться улучшения состояния больных, уменьшить чувство дискомфорта и устранить косметический дефект. При онихомикозах наибольшее беспокойство больным доставляют деформированные, значительно утолщенные (гипертрофированные) ногтевые пластинки — онихогрифоз. Для коррекции этого состояния применяют аппаратный педикюр. С помощью аппарата, напоминающего стоматологическую турбину, за короткий промежуток времени механическим путем удаляются измененные участки ногтей, гиперкератотические, роговые массы с кожи, омозолелости. При этом не происходит травматизации матрикса ногтя, и пациент после процедуры остается работоспособен.
При ограниченном поражение ногтей (не более 3 ногтевых пластинок и не более чем на 1/2 по площади с дистального края) применяются препараты для местного применения. Лечение рекомендуется начинать с подчистки пораженного участка ногтевой пластинки при помощи набора «Микоспор», аппаратного педикюра или кератолитических средств. Далее на пораженную ногтевую пластинку наносятся антифунгальные препараты. Раствор аморолфина, содержащий циклопирокс, наносится на ногтевую пластинку 1–2 раза в неделю. Перед нанесением лака не нужно предварительно очищать ногтевую пластинку от предыдущих слоев препарата. Лак наносится ежедневно до полного отрастания здоровой ногтевой пластинки. На 7-й день ногтевая пластинка очищается с помощью любого косметического средства для снятия лака. В литературе встречаются противоречивые сообщения об эффективности этого метода лечения. Указывается процент излеченности больных от 5–9 до 50 %.
При распространенном поражении ногтевых пластинок на пальцах кистей комплекс лечебных мероприятий должен включать назначение системного антимикотика, подчистку ногтей и наружную терапию антифунгальными препаратами. С целью профилактики повторного заражения необходимо обработать перчатки больного, подвергнуть дезинфекции предметы личной гигиены (мочалки, полотенца, пилочки для ногтей, терки и скребки для обработки кожи и ногтей).
Препаратом выбора при лечении онихомикоза любой локализации является тербинафин. Его назначают взрослым и детям весом более 10 кг по 250 мг в сутки в течение 6 нед. Детям от 2 лет весом менее 20 кг тербинафин назначают из расчета 67,5 мг/кг в сутки, от 20 до 40 кг — 125 мг/кг в сутки в течение 6 нед. Препаратами резерва являются средства, содержащие итраконазол и флуконазол. Итраконазол применяется по двум схемам: по 200 мг ежедневно в течение 3 мес или по 200 мг дважды в день в течение 7 дней на первой и пятой неделях с начала терапии. Для лечения онихомикозов у детей итраконазол не назначается. Флуконазол рекомендуется принимать по 150 мг 1 раз в неделю в течение 3–6 мес.
Проведение комплексной терапии, состоящей из приема системного антимикотика, подчистки ногтей, местного применения антифунгальных препаратов, а также противоэпидемиологические мероприятия, обеспечивают высокую эффективность излечения онихомикоза стоп. Тербинафин назначают взрослым и детям весом более 10 кг по 250 мг в сутки в течение 12 и более недель. Детям от 2 лет весом менее 20 кг препарат назначают из расчета 67,5 мг/кг в сутки, от 20 до 40 кг — 125 мг/кг в сутки в течение 12 нед. Флуконазол рекомендуется применять по 150–300 мг 1 раз в неделю в течение 6–12 мес. Итраконазол применяется по двум схемам: по 200 мг ежедневно в течение 3 мес или по 200 мг дважды в день в течение 7 дней на первой, пятой и девятой неделях. При поражении больших пальцев стоп рекомендуется проводить 4-й курс пульс-терапии на тринадцатой неделе от начала терапии. Для лечения онихомикозов у детей итраконазол не применяется.
Критериями микологической излеченности онихомикоза являются отрицательные результаты микроскопического и культурального исследования ногтевой пластинки. После окончания лечения итраконазолом и тербинафином здоровые ногтевые пластинки отрастают не полностью, поэтому полное клиническое выздоровление можно наблюдать только спустя 2–4 мес после окончания приема антифунгальных препаратов.
Литература
Л. П. Котрехова, кандидат медицинских наук, доцент
К. И. Разнатовский, доктор медицинских наук, профессор
Н. Н. Климко, доктор медицинских наук, профессор
СПбМАПО, Санкт-Петербург