Луд в медицине что это
Диагностика и лечение раковых опухолей с использованием радиоактивных изотопов
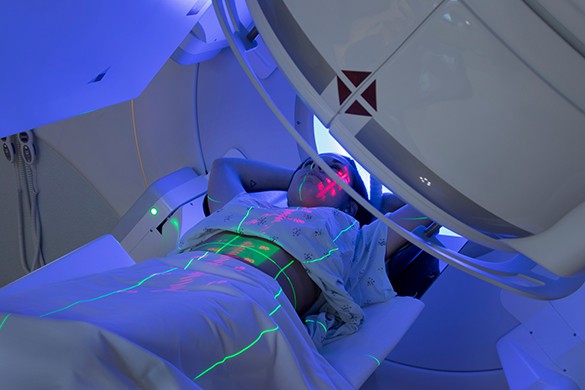
Лучевая терапия уже давно является одним из основных способов лечения злокачественных новообразований. Однако среди ее недостатков — широкая зона облучения, которая поражает не только саму опухоль, но и окружающие здоровые ткани.
Современная медицина постепенно отказывается от традиционной лучевой терапии, поскольку появляются новые, более эффективные и безопасные методы ядерной медицины. Одним из таких является лечение радиоизотопами, которое активно применяют специалисты медицинского центра «Анадолу».
Какие виды такой терапии существуют?
Терапия «Лютеций-177-ПСМА»
Это лечение основано на использовании радиоактивного изотопа элемента лютеция. Его применяют для борьбы с раком предстательной железы на поздних стадиях. Терапия основана на том, что раковые клетки железы имеют на своей поверхности большое количество рецепторов к особому белку — простат-специфическому мембранному антигену (ПСМА). Комплексы, состоящие из изотопа лютеция-177 и ПСМА, с высокой избирательностью присоединяются именно к этим рецепторам, а значит основная часть излучения будет воздействовать именно на опухолевые клетки.
Терапия «Лютеций-ДОТАТАТ»
Принцип действия этого метода лечения схож с терапией «Лютеций-177-ПСМА», только здесь в качестве мишени выступают клеточные рецепторы к гормону соматостатину. Они в большом количестве присутствуют на мембранах клеток нейроэндокринных опухолей желудочно-кишечного тракта и поджелудочной железы.
Терапия «Актиний-225-ПСМА»
Данный способ основан на тех же принципах, что и терапия «Лютеций-177-ПСМА», и точно так же предназначен для уничтожения радиоактивным излучением раковых клеток в предстательной железе. Отличие тут в применении другого радиоизотопа — актиния-225. Если лютеций-177 при распаде излучает бета-частицы, то есть высокоэнергетические электроны, то актиний-225 при распаде излучает альфа-частицы — ядра гелия. Терапию «Актиний-225-ПСМА» применяют в случаях, когда пациент не демонстрирует хорошего ответа на радионуклидное лечение лютецием-177.
Терапия радием
Основана на природной радиоактивности данного элемента, который производит альфа-излучение, а в организме человека ведет себя подобно кальцию. Это означает, что более 80% попадающего в наше тело радия накапливается в костях. А следовательно, его удобно использовать для местного радиационного воздействия на метастазы злокачественных опухолей в костной ткани.
Каковы цели радионуклидной терапии?
В первую очередь, задача такого лечения — уничтожить максимальное количество опухолевых клеток в организме больного. Уменьшение размера злокачественных очагов, а также уничтожение отдельных метастазов позволяет затем прибегнуть к радикальной операции по удалению новообразования. Кроме того, сокращение числа опухолевых элементов благотворно отражается на самочувствии пациента и облегчает симптомы развернутого онкологического заболевания. Снижение выраженности болевого синдрома и других проявлений особенно важно, поскольку обычно радионуклидную терапию назначают на поздних стадиях опухолевого процесса или при слишком сильных побочных эффектах от химиотерапии.
Безопасно ли лечение радиоизотопами?
Строго говоря, и рецепторы к простат-специфическому мембранному антигену, и рецепторы к соматостатину имеются и на здоровых клетках. Но на мембранах злокачественно перерожденных клеток их количество в разы больше. А значит именно к этим клеткам и присоединится подавляющее большинство молекулярных комплексов с радиоактивными элементами. Следовательно, и доза излучения, полученная опухолью, будет намного выше. Это свойство радионуклидной терапии называют таргетностью (от слова target, или «цель»), оно означает высокую точность воздействия именно на злокачественное новообразование, а не на здоровые ткани.
Кроме того, важную роль для безопасности лечения играют типы радиационного излучения, которые при нем используются. Лютеций-177 производит бета-излучение, а актиний-225 и радий — альфа-излучение. Проникающая способность бета-частиц довольно невелика — их останавливают всего 2–2,5 сантиметра живой ткани. То есть воздействовать это излучение будет исключительно на местном уровне. Проникающая способность альфа-частиц еще меньше — оно способно пройти всего через 5–10 соседних клеток. А значит здесь таргетность воздействия на опухолевые клетки будет максимально высокой.
Лудомания
Содержание:
Лудомания (с латинского «лудо» – играю, «мания» – влечение, страсть) – неконтролируемое человеком патологическое пристрастие к различным азартным играм (игровые автоматы, реальные и онлайн-казино и т. п.). Альтернативные обозначения лудомании – гэмблинг-зависимость, игровая зависимость.
Причины лудомании
В целом считается, что все зависимости такого плана (шопоголизм, лудомания, клептомания и пр.) имеют в основном психологические причины. Хотя последние исследования говорят о том, что факторы, способствующие развитию лудомании, могут быть наследственными или физиологическими (гормональные сбои, недостаточная выработка дофамина).
К основным психологическим причинам развития зависимости от азартных игр относят:
Неспособность к самостоятельной регуляции состояния возбуждения. Зачастую игрок не может не только контролировать свое состояние, погружение в игровой транс, но и осознать существование такой проблемы.
Проблемы в отношениях – в семье, с друзьями, родителями, чувство одиночества.
Факторами, способствующими развитию зависимости, часто становятся также:
то, что в азартные игры играют также родственники или друзья;
переоцененное значение денег в глазах человека, убежденность, что с их помощью можно решить все проблемы;
стремление к легкому заработку;
финансовая неграмотность, неумение распоряжаться деньгами.
Как развивается лудомания
Стадии зависимости
Со временем без лечения лудомания прогрессирует. Есть несколько классификаций этапов игровой зависимости. Рассмотрим самую простую, состоящую из 3 стадий.
Не все, кто играет – заложники лудомании, лечение многим вовсе не требуется. Это люди, которые сохраняют трезвое мышление, контролируют потраченную сумму, проводят за игрой разумное количество времени, не стремятся к выигрышу и рассматривают игру всего лишь как эпизодическое развлечение.
Главные критерии, по которым можно понять, что у человека именно зависимость, это:
отсутствие разумных, рациональных причин для игры;
невозможность отказаться от предложения сыграть;
все большее количество времени, проводимое за играми;
приоритет участия в игре над всеми остальными аспектами жизни (работой, учебой, семейными обязанностями и т. д.);
причинение вреда себе и окружающим (потеря работы, финансовые долги, продажа семейного имущества, воровство и т. д.).
Лудомания отражается и на здоровье. Большое количество гормонов, выбрасываемых в кровь, заставляет внутренние органы работать в ненормально интенсивном режиме, что приводит к нарушениям в их работе. Истощается психика. Внешне лудоман часто напоминает человека с алкогольной или наркотической зависимостью.
Последствия лудомании
Любая патологическая зависимость, оставленная без лечения, тем или иным образом разрушает жизнь и/или здоровье человека.
Лудомания приводит к:
разрушению карьеры, потере профессиональной репутации. Из-за зависимости лудоман пропускает или вовсе бросает работу, плохо выполняет профессиональные обязанности, срывает сроки проектов;
серьезным финансовым проблемам. Зависимые игроки тратят все накопления, влезают в долги, распродают имущество, иногда даже лишаются жилья.
разрушению семьи и социальных связей. Лудоман резко ограничивает круг общения, почти не уделяет время семье, занимает и не отдает деньги друзьям и знакомым, чем портит отношения с ними.
Самые серьезные последствия – это:
Правонарушения, которые начинает совершать лудоман (воровство, кражи, и т. п.).
Попытки самоубийства – до 40% больных пытаются покончить с собой.
Лечение лудомании
Из-за мощной психологическо-биохимической основы игровой зависимости вылечиться от нее самостоятельно практически невозможно. Больной часто даже не осознает необходимость лечения.
Первый и необходимый шаг к лечению – это принятие больным существования проблемы. Для этого может потребоваться одна или несколько бесед с психотерапевтом. После чего можно начинать непосредственно терапию.
Лечение запущенной лудомании, когда у больного уже развилиь депрессия, неврозы, присутствуют суицидальные мысли, проводится с применением медикаментов. На начальных этапах есть шанс обойтись без фармакологии. Однако медикаменты в любом случае – не основной способ.
Лечение лудомании осуществляется с помощью психотерапевтических методик. Эффективно сочетание групповой и индивидуальной терапии.
В лечении применяются:
лечение при помощи гипноза, в том числе эриксоновского;
программа «12 шагов», аналогичная лечению алкогольной зависимости.
Профилактика игровой зависимости
Профилактика игромании направлена на устранение/уменьшение влияния факторов, которые приводят к зависимости.
Уменьшить уровень стресса, решать появляющиеся проблемы, не накапливать, не игнорировать их.
Вести активный образ жизни, иметь хобби.
Сохранять оптимизм, вовремя обращаться к специалисту при первых признаках депрессии, неврозов.
Статья написана под кураторством доктора Воронцов А.Л
Гипервентиляционный синдром и дисфункциональное дыхание
Клинические особенности, диагностические критерии гипервентиляционного синдрома (ГВС) и дисфункционального дыхания (ДД) недостаточно знакомы широкому кругу врачей [1, 2, 3]. К одной из исторических вех, связанной с понятиями о функциональных нарушениях
Клинические особенности, диагностические критерии гипервентиляционного синдрома (ГВС) и дисфункционального дыхания (ДД) недостаточно знакомы широкому кругу врачей [1, 2, 3]. К одной из исторических вех, связанной с понятиями о функциональных нарушениях дыхания, относят 1871 год, когда Да Коста (Da Costa Jacob, 1833–1900), американский врач, принимавший участие в Гражданской войне США, применил термин «гипервентиляционый синдром» (ГВС) у пациентов с так называемым «солдатским сердцем». С тех пор для характеристики дыхательных расстройств предлагались различные альтернативные определения: «дыхательный невроз», «нейрореспираторная дистония», «респираторный синдром», «респираторная дискинезия», «идиопатическая гипервентиляция», «нейрореспираторный синдром», «неустойчивое дыхание» и др. Однако указанные термины не получили широкого признания. Они являются достаточно общими и не отражают особенностей нарушений дыхания у конкретного больного [4]. Перечисленные определения нередко связывают с понятием «непонятная одышка» (unexplained dyspnea).
ГВС встречается в 6–11% от числа пациентов общей практики. Соотношение мужчин и женщин составляет 1:4, 1:5; чаще наблюдается в 30–40 лет, но возможно развитие в других возрастных группах, включая детей и пожилых. L. Lum (1987) подчеркивал, что «каждый врач в течение недели может встретить хотя бы одного больного с ГВС». Врачи различных специальностей — невропатологи, кардиологи, пульмонологи, психиатры — могут наблюдать у своих пациентов явления гипервентиляции. Острое течение ГВС встречается значительно реже, чем хроническое, и составляет лишь 1–2% от общего числа больных [2, 6, 7].
Причины развития ГВС довольно многочисленны. Это неврологические и психические расстройства, вегетативные нарушения, болезни органов дыхания, некоторые заболевания сердечно-сосудистой системы, органов пищеварения, экзогенные и эндогенные интоксикации, лекарственные средства (салицилаты, метилксантины, β-агонисты, прогестерон) и др. Считается, что в 5% случаев ГВС имеет только органическую природу, в 60% случаев — только психогенную, в остальных — комбинации этих причин [6].
Важной особенностью развития ГВС является то обстоятельство, что если причины, являющиеся триггерными, устраняются, то гипервентиляция, которая уже не соответствует требованиям конкретной ситуации, сохраняется, сохраняется и гипокапния. Происходит стабилизация гипокапнических нарушений газообмена и формируется «порочный круг» ГВС, который начинает циркулировать автономно, и симптомы могут персистировать достаточно долго — феномен «махового колеса». Эти изменения реакции дыхания указывают на уязвимую систему контроля дыхания, которая не способна поддержать нормальное парциальное давление углекислого газа в крови (РСО2) и кислотно-щелочной гомеостаз [8, 9, 10, 11].
В основе развития клинических проявлений ГВС лежат гипокапнические нарушения газообмена [2, 3, 10]. Среди множества клинических проявлений ГВС одышка является ведущей жалобой и встречается практически в 100% случаев. Одышка может быть единственным клиническим проявлением, но чаще сочетается с другими симптомами.
Основные клинические проявления ГВС
Респираторные: одышка, вздохи, зевота, сухой кашель.
Общие: снижение трудоспособности, слабость, утомляемость, субфебрилитет.
Кардиальные: кардиалгия, экстрасистолия, тахикардия.
Психоэмоциональные: тревога, беспокойство, бессонница.
Гастроэнтерологические: дисфагия, боли в эпигастрии, сухость во рту, аэрофагия, запоры.
Неврологические: головокружение, обмороки, парестезии, тетания (редко).
Мышечные: мышечная боль, тремор.
Диагностика ГВС в первую очередь опирается на знание врачей самых различных специальностей об особенностях клинической картины ГВС. ГВС должен устанавливаться только после проведения дифференциальной диагностики с другими заболеваниями, протекающими с синдромом одышки. Полиморфизм клинических проявлений ГВС вызывает диагностические проблемы. Назначаются многочисленные обследования, дорогостоящие, ненужные, а иногда и опасные для больного. L. Lum (1987), обсуждая диагностические проблемы, называет среди врачебных ошибок бесполезные абдоминальные операции, операции на позвоночнике и других органах, инвазивные исследования, проводимые не без риска, и, что еще хуже, такие диагнозы, как эпилепсия и инфаркт миокарда. Взаимосвязи гипокапнии и ассоциированных с ней симптомов являются чрезвычайно сложными. Многие врачи при регистрации у больных низких значений РСО2 автоматически устанавливают диагноз ГВС, что является неправильным. Известно, что явления гипокапнии могут быть у больных рестриктивными легочными процессами, при лихорадочных состояниях, сердечной патологии, однако при этом «классических» гипокапнических жалоб может и не быть. И наоборот, так называемые гипокапнические жалобы, например тревога, одышка, парестезии и др., встречаются у пациентов с нормокапнией.
В практической медицине больной с ГВС — это пациент, предъявляющий жалобы на одышку, которая не соответствует данным объективного осмотра, показателям клинико-инструментальных исследований дыхания, с диспропорциональной, непонятной одышкой, субъективное восприятие которой является довольно тягостным. К сожалению, при отсутствии достоверных объяснений одышки больные обычно направляются для консультаций в различные лечебные учреждения. В конечном итоге они и формируют основной контингент альтернативной медицины, различных псевдоспециалистов «по тренировке правильного дыхания».
Исследование функции внешнего дыхания, имеющее важное значение в дифференциальной диагностике одышки, не помогает в верификации функциональных нарушений дыхания. Основным подтверждением ГВС служит выявление гипокапнических нарушений газообмена. Снижение РСО2 — прямое свидетельство альвеолярной гипервентиляции. Однако исходная гипокапния у больных с ГВС встречается не так часто. Поэтому в тех случаях, когда у пациента с предположительным ГВС в условиях покоя определяются нормальные значения углекислоты, рекомендуется определение изменений уровня СО2 при различных провокационных тестах. К «золотому стандарту» диагностики ГВС относят пробу с произвольной гипервентиляцией.
Департаментом пульмонологии университета г. Наймиген (Голландия) разработан Наймигенский опросник (Nijmegen questionnaire) для выявления физиологических показателей дизрегуляции вентиляции, сопоставимых с ГВС (табл.). Анкета содержит 16 пунктов, которые оцениваются по 5-балльной шкале (0 — никогда, 4 — очень часто). Минимальные и максимальные достижимые числа — 0 и 64 соответственно.
Данный опросник нашел свое применение прежде всего для скрининг-диагностики ГВС. Существует положение, согласно которому использование данного опросника позволяет корректно предсказывать ГВС в 90% от всех случаев [2, 12].
В последние годы в клиническую практику начинает внедряться понятие «дисфункциональное дыхание» (ДД). Приоритет внедрения термина принадлежит Ван Диксхорну (J. van Dixhoorn), который привел его в работе Hyperventilation and dysfunctional breathing (1997). Основанием для этого явилось понимание, что при функциональных нарушениях дыхания возможны различные изменения паттерна дыхания и значений РCO2, а не только гипокапнические расстройства, характерные для ГВС. ДД может проявляться также быстрым, аритмичным, поверхностным дыханием, частыми вздохами, преобладанием грудного типа дыхания.
Одной из сложных и дискуссионных проблем в пульмонологии является понимание взаимоотношений ГВС, ДД и бронхиальной астмы (БА) [15–18]. С. И. Овчаренко и др. (2002) у 22 из 80 больных БА выявили нарушения дыхания, соответствующие критериям ГВС. Сведений относительно встречаемости дисфункциональных нарушений дыхания при астме немного. Установлено, что среди лиц с диагнозом БА и по крайней мере с одним предписанием антиастматического препарата 29% имеют клинические признаки ДД [19]. Указывается, что ДД может усиливать симптомы БА и приводить к избыточному назначению лекарств.
Достаточно сложным является понимание механизмов развития дисфункциональных расстройств дыхания при БА; существует ряд предположений. К достаточно обоснованным факторам развития гипервентиляции относят тревожные расстройства. Использование больными бронходилататоров (β-2-агонисты, теофиллин), которые обладают эффектами стимуляции дыхания, также относят к факторам развития гипервентиляции. Обсуждается роль изменений перцепции одышки при БА. Анализ существующих проблем взаимосвязи ДД и БА провел M. Morgan (2002), представив следующие ключевые положения:
В зависимости от установления особенностей ДД должна осуществляться и программа лечения больных. При выявлении ГВС релаксирующие методы дыхательной гимнастики проводятся под руководством опытных инструкторов, назначаются β-адреноблокаторы, бензодиазепины [5, 22, 23]. При явлениях гиповентиляции — массаж дыхательных мышц, использование дыхательных тренажеров. Выявление ГВС при БА указывает на необходимость применения методов коррекции функциональных нарушений дыхания. Релаксирующие дыхательные упражнения за счет неспецифических механизмов дыхательного тренинга улучшают качество жизни у этих больных.
По вопросам литературы обращайтесь в редакцию.
В. Н. Абросимов, доктор медицинских наук, профессор
Рязанский ГМУ им. акад. И. П. Павлова, Рязань
Скрининговая ультразвуковая диагностика рака ободочной кишки
УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Введение
В последнее время во всех высокоразвитых странах отмечается быстрый рост заболеваемости раком ободочной кишки 5. Многочисленными исследованиями доказано, что прогноз заболевания в значительной степени зависит от своевременности постановки диагноза опухоли, т.е. ранняя диагностика имеет важнейшее значение. К сожалению, у 60-80% больных с впервые установленным диагнозом определяется III-IV стадии заболевания 8. Своевременная диагностика рака ободочной кишки обычно возможна на доклинической стадии, что требует проведения специальных лабораторно-инструментальных скрининговых исследований. Существует ряд требований, предъявляемых к скрининговым методикам: безопасность для пациента, неинвазивность, высокая чувствительность и специфичность, низкая стоимость и др. В настоящее время в США и развитых странах Западной Европы внедряются скрининговые программы, основанные на определении скрытой крови в кале, однако они недостаточно специфичны, а количество ложноотрицательных результатов составляет от 30 до 70% 8.
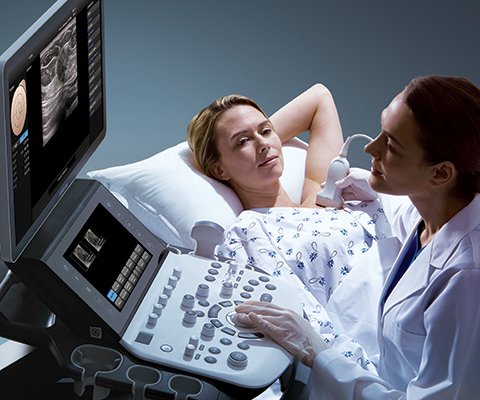
Ультразвуковое исследование (УЗИ) является одним из нетрадиционных, неинвазивных и широко распространенных методов диагностики, причем большая часть населения позитивно настроена к данной методике. Ранее считалось, что провести УЗИ органов, содержащих газ, нельзя, поскольку они полностью отражают ультразвуковые волны. В последнее время наблюдается значительный прогресс трансабдоминальной ультразвуковой диагностики заболеваний полых органов, в частности, толстой кишки.
Материалы и методы
Работа осуществлялась на базе 7 лечебно-профилактических учреждений областного, городского и районного уровней. Предварительно для врачей проводился двухдневный обучающий семинар по ультразвуковой диагностике онкологической патологии желудочно-кишечного тракта на базе областной клинической больницы и областного онкологического диспансера. Проанализирован 1-3-летний катамнез у 9000 больных, прошедших скрининговое УЗИ ободочной кишки. При оценке катамнеза использовались данные областного онкорегистра. Обследовано 29 467 больных с разнообразной патологией. Возраст пациентов составлял 23-89 лет. Никому из обследованных больных не был выставлен диагноз рака ободочной кишки до УЗИ.
Для ультразвуковой диагностики рака ободочной кишки можно применять любую современную ультразвуковую диагностическую аппаратуру, работающую в режиме real-time. Оптимальным выбором являются линейные, трапециевидные или конвексные датчики частотой 3,5-5 МГц, которые нами использовались. В некоторых случаях для более детального изучения структуры стенок кишки применяли датчик частотой 7,5 МГц, однако у пациентов с избыточным развитием подкожно-жировой клетчатки возможности использования такого датчика ограничены.
Предлагаемая методика являлась элементом обычного рутинного УЗИ органов брюшной полости. Исследование осуществляли натощак, через 8-10 ч после последнего приема пищи. Пациентам, страдающим метеоризмом, за 2-3 дня до исследования исключали из питания продукты, способствующие избыточному газообразованию в кишечнике (свежие овощи, фрукты, молоко и др.). При необходимости назначали полиферментные препараты и активированный уголь. Не рекомендуется проводить УЗИ ободочной кишки после рентгенологического исследования желудочно-кишечного тракта, после эндоскопических процедур, особенно лапароскопических вмешательств. Это связано с тем, что воздух, нагнетаемый при эндоскопии, и сернокислый барий, применяемый в рентгенологии, отражают ультразвуковые волны и тем самым затрудняют исследование.
Скрининговое УЗИ ободочной кишки начинали в положении больного лежа на спине. Методика основана на обнаружении неспецифического симптома «пораженного полого органа». Осуществляли обзорное сканирование брюшной полости, как показано на рис. 1а (датчик располагают поперечно) для выявления патологических изменений стенки ободочной кишки и оценки ее положения. Затем методично осматривали ободочную кишку соответственно ее обычному расположению. Для этого ультразвуковой датчик устанавливали в правой подвздошной области перпендикулярно длиннику кишки (рис. 1б). Проводили последовательное сканирование по часовой стрелке вдоль проекции ободочной кишки, начиная с купола слепой кишки и перемещая датчик по ходу восходящего, поперечного и нисходящего отделов ободочной кишки, при этом осматривали печеночный и селезеночный изгибы толстой кишки. Заключительным этапом являлось сканирование сигмовидной кишки.
Затем датчик располагали продольно, по ходу ободочной кишки, и повторяли сканирование в той же последовательности, что и на втором этапе (рис. 1в). Для обнаружения патологии в латеральных и задних сегментах стенки ободочной кишки проводили сканирование с боковых поверхностей брюшной стенки.