Лимфоидные элементы в желудке что это такое
Особенности эндоскопической семиотики и антихеликобактерная терапия MALT-лимфом желудка
Лимфомы гастроинтестинального тракта охватывают от 14% до 27% всех экстранодальных поражений и составляют от 1% до 15% всех злокачественных опухолей желудочно-кишечного тракта. Чаще всего поражается желудок (50–75%), сравнительно реже тонкая кишка (20–35%
Лимфомы гастроинтестинального тракта охватывают от 14% до 27% всех экстранодальных поражений и составляют от 1% до 15% всех злокачественных опухолей желудочно-кишечного тракта. Чаще всего поражается желудок (50–75%), сравнительно реже тонкая кишка (20–35%). Лимфомы толстой кишки наблюдаются в 5–10% случаев. Самыми редкими признаны первичные неходжкинские лимфомы пищевода [1].
В 1983 году Brooks и Enterline [2] провели клинико-морфологическое исследование, где показали, что нодальные и экстранодальные лимфомы отличаются по биологическим свойствам и что экстранодальные варианты лимфомы имеют более благоприятный прогноз.
Brooks и Enterline впервые отметили патогенетическую связь между хроническим воспалением слизистой оболочки желудка и развитием лимфомы. Было высказано предположение, что многие типы лимфом желудка представляют собой злокачественную трансформацию доброкачественных и длительно текущих лимфоцитарных поражений желудка. Авторы пришли к тому заключению, что длительная антигенная стимуляция вместе с аутоиммунным феноменом в клетках слизистой оболочки желудка в целом приводят к появлению злокачественного клона. Эта гипотеза была подтверждена результатами клинико-морфологических исследований, проведенных при лимфомах слюнной и щитовидной желез. Было показано, что лимфомы этих желез могут возникнуть на фоне хронического тиреоидита и сиалоаденита с синдромом Шегрена или без него.
P. Isaacson и D. H. Wright [3] обратили внимание на то, что большая часть первичных лимфом желудка развивается на фоне хронических гастритов. Более того, было показано, что другие варианты экстранодальных лимфом также связаны с хроническими воспалительными процессами. Доказано, что Нelicobacter pylori — грамотрицательная спиралевидная бактерия, впервые выделенная из гастробиоптата австралийскими исследователями Warren и Marschall в 1983 году, является причиной подавляющего большинства случаев хронических гастритов. Она приводит к возникновению язвенной болезни желудка, 12-перстной кишки, является одним из факторов риска аденокарциномы желудка.
Показано, что при эрадикации этого микроорганизма симптомы хронического воспаления становятся менее интенсивными и снижается степень лимфоцитарной инфильтрации. В 1993 году были представлены доказательства, что Н. pylori играет важную роль в возникновении подгруппы лимфом желудка MALT-типа [4]. Рядом авторов [5] было высказано мнение, что Н. pylori вызывает нарушение физиологических и иммунологических процессов, окислительное повреждение ДНК и пролиферацию как гемапоэтических, так и клеток слизистой оболочки желудка. В дальнейшем было установлено, что 90% больных MALT-лимфомой инфицированы Н. pylori [6, 7, 8]. Было показано также, что Н. pylori непосредственно и посредством цитотокина вызывает пролиферацию Т-клеток и макрофагов, что сопряжено с высвобождением цитокинов (интерлейкина-2 и интерлейкина-6). Последние, в свою очередь, вызывают пролиферацию В-клеток, способствуют развитию лимфоидных фолликулов и агрегатов лимфоцитов в толще слизистой оболочки желудка [9].
Материалы и методы исследования
Эндоскопическая картина лимфом желудка изучена нами у 250 пациентов, при этом поражение у 160 (64%) больных расценено как первичное, а у 90 (36%) — как вторичное, наблюдаемых в РОНЦ с 1995 года, из которых было 99 пациентов с MALT-лимфомой желудка. Разработаны эндоскопические и эндосонографические критерии диагноза MALT-лимфомы, ее дифференциально-диагностические признаки, проведена оценка лекарственной терапии.
Результаты и их обсуждение
При тщательном анализе развития болезни нами установлено, что в группе с первичными лимфомами желудка практически одна треть (32%) пациентов имели гастроэнтерологический анамнез: язвенную болезнь желудка, хронический атрофический, гипертрофический или смешанные гастриты, зачастую ассоциированные с инфекцией H. pylori.
Согласно нашим наблюдениям длительность существования гастроэнтерологической патологии до установления наличия опухоли в группе с первичной лимфомой желудка весьма вариабельна: в течение первых трех месяцев диагноз установлен у 30,6% (49 больных), в течение 6 месяцев у 18,1% (29 больных), в срок от 6 до 12 месяцев у 15,6% (25 больных). Отдельно следует отметить, что практически у трети пациентов (27,5% — 44 пациента) диагноз первичной лимфомы желудка был установлен спустя год (табл. 1).
Также отдельно необходимо отметить, что диагноз первичной лимфомы желудка у 8% пациентов выявлен при плановом обследовании по поводу сопутствующей патологии и оказался диагностической находкой, так как заболевание у части больных протекало бессимптомно.
В группе пациентов со вторичным поражением желудка от момента установления диагноза первичной локализации процесса до времени выявления поражения желудка сроки были различны и представлены в табл. 2.
Как видно из представленных в таблице данных, поражение желудка в большинстве случаев развилось в первые два года от начала заболевания, что диктует нам необходимость обязательных периодических эндоскопических исследований желудка с целью своевременного выявления метастатического поражения его при лимфомах.
В нашей работе чаще всего при лимфомах желудка имело место инфильтративно-язвенное и инфильтративное его поражение — 28,4% и 21,6% соответственно, затем в 14,8% встречается язвенная форма роста опухоли. Гастритоподобный вариант опухоли отмечен в 14,4%. Реже встречались смешанная и экзофитная формы роста опухоли — 12,0% и 8,8% соответственно.
Причем, как показывает анализ наших данных, при MALT-лимфоме преобладала гастритоподобная форма роста, которая составила 34,3%.
Эндоскопическая картина гастритоподобной формы лимфомы желудка является наиболее вариабельной и по преобладанию макроскопических признаков может проявляться в виде:
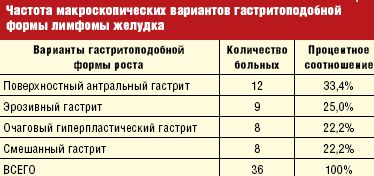
Естественно, такое деление является относительно условным, и эти формы выделяются нами по преобладанию наиболее выраженных указанных признаков, симулирующих ту или иную форму гастрита (табл. 3).
Анализируя полученные данные, чаще всего, в 33,4%, отмечался поверхностный антральный гастрит, вторым по частоте стал эрозивный гастрит — 25,0%, с одинаковой частотой в 22,2% встречается очаговый гиперпластический гастрит и смешанный гастрит.
При гастритоподобной форме лимфомы желудка в виде антрального гастрита, как следует из самого определения, визуальные проявления опухоли симулируют воспалительные изменения в антральном отделе желудка, которые отмечены нами в 33,4%. При сохраненной эластичности стенок желудка отмечается пастозность, разрыхленность и очаговая гиперемия слизистой антрального отдела желудка, чередующаяся с участками белесоватого цвета, ее повышенная контактная кровоточивость. Как и при других вариантах, характерным является появление стекловидного блеска. При проведении биопсии подвижность и эластичность слизистой оболочки снижена, отмечается ее фрагментация.
Изменения при лимфоме желудка в виде эрозивного гастрита отмечаются в 25,0% случаев и характеризуются наличием множественных поверхностный острых эрозий неправильной или щелевидной формы на фоне пастозной, неравномерно гиперемированной слизистой с усиленным сосудистым рисунком. Участки эрозий могут локализоваться в различных отделах желудка, чередуясь с неизмененной слизистой, либо занимать изолированную, ограниченную зону. Эластичность стенок остается, как правило, сохраненной или снижена незначительно.
Лимфома желудка в виде локального гиперпластического гастрита. Этот тип лимфомы отмечается в 22,2% случаев и характеризуется умеренным неравномерным утолщением складок на ограниченном участке чаще по большой кривизне и в проксимальном отделе желудка иногда с переходом на переднюю или заднюю стенки. Эластичность стенки сохранена, подвижность складок может быть сохраненной или сниженной. Поверхность складок покрыта вязкой стекловидной слизью, разрыхлена. При инсуффляции складки слизистой пораженного участка, как правило, не расправляются полностью.
В нашем исследовании инфицирование H. pylori было выявлено практически у всех больных при мелкоклеточном варианте и составило 96,7%, при промежуточном варианте MALT-лимфомы желудка — 90%, в отличие от смешанно-клеточных MALT-лимфом, при которых частота инфицирования составила только 53,8%.
При выявлении инфицирования H. pylori мы также определяли степень обсемененности. Оказалось, что при мелкоклеточных MALT-лимфомах высокая частота инфицирования сочетается с выраженной степенью обсемененности чаще (75,9%), чем при других подвариантах. Так, у больных с промежуточным вариантом наличие H. pylori-инфекции сопровождается выраженной степенью обсемененности достоверно реже и выявлено в 38,9%, при смешанных MALT-лифмомах выраженная степень обсемененности установлена у 57,1% пациентов.
Умеренная степень обсемененности при мелкоклеточных опухолях выявлена у 20,7%, при промежуточном варианте чаще — у 61,1%, а при смешанной MALT-лимфоме — у 14,3%.
Слабая степень обсемененности H. pylori встречается у больных MALT-лимфомой желудка крайне редко, она была определена лишь у трех пациентов.
Терапия больных первичной MALT-лимфомой представляет ряд особенностей. Это обусловлено тем, что в мировой практике накоплен относительно небольшой опыт использования всех видов лечебного воздействия — антихеликобактерной терапии, химиотерапии, лучевой терапии, хирургического лечения и их сочетаний.
Антихеликобактерная терапия использовалась нами только при I стадии (классификация Lugano, 1993) MALT-лимфомы желудка мелкоклеточного строения. Лечение проводилось в соответствии с рекомендациями Международного протокола LY03 по изучению MALT-лимфом желудка низкой степени злокачественности [10]. Нами применялась трехкомпонентная схема первой линии эрадикационной терапии, включающая одновременное применение в течение 10–14 дней следующих препаратов:
В результате проведенного лечения у 14 пациентов (87,5%) из 16 больных была достигнута полная ремиссия, у 2 больных (12,5%) констатирована стабилизация заболевания.
Терапевтический эффект антибиотикотерапии реализовался постепенно. Нами установлена последовательность исчезновения проявлений болезни. Первыми ликвидировались клинические симптомы: боль, изжога, тошнота, желудочный дискомфорт.
Вслед за эрадикацией H. pylori постепенно уменьшались визуальные эндоскопические проявления опухолевого поражения: сокращались размеры опухолевого поражения, подслизистой инфильтрации, уменьшался калибр складок слизистой, происходило рубцевание специфических язвенных дефектов, затем восстанавливалась нормальная архитектоника слизистой, исчезала деформация стенок желудка.
Необходимо акцентировать внимание на том, что сроки наступления полного терапевтического эффекта весьма вариабельны. Полная ремиссия, подтвержденная гистологическим и иммунологическим исследованием гастробиоптатов, была диагностирована у больных, получавших антихеликобактерное лечение, в сроки от 2 до 10 месяцев (медиана 5,5 месяцев).
Это означает, что лечение мелкоклеточных MALT-лимфом с применением антихеликобактерных препаратов — это терапия, осуществленная всего за 10–14 дней, но требующая в последующем взвешенного динамического наблюдения и корректной оценки происходящих изменений. Темп наступления полного клинического благополучия является косвенным признаком прогнозирования терапевтического эффекта.
Из 14 больных с подтвержденной полной ремиссией вследствие антихеликобактерной терапии только у одной больной в возрасте 51 год был констатирован рецидив заболевания при контрольном обследовании через 7 месяцев после окончания лечения без каких-либо клинических проявлений. Трактовка эндоскопической картины была сложной: осуществлялась дифференциальная диагностика между эрозивным гастритом и минимальными проявлениями лимфомы. Рецидив был подтвержден иммуноморфологическими исследованиями. В последующем больная получала последовательное лечение Лейкераном (хлорамбуцил), COP с эффектом, который расценен нами как стабилизация заболевания. Учитывая клиническое благополучие, а также наличие тяжелой сопутствующей патологии, было решено хирургическое лечение не применять, а больную оставить под динамическим наблюдением. В течение последующих 36 месяцев больной проводится регулярное обследование (каждые 4–5 месяцев). За этот период наблюдения прогрессирования заболевания не наступило по настоящее время.
Это наблюдение демонстрирует особое свойство мелкоклеточной MALT-лимфомы. Сочетание клинического благополучия с объективными данными стабилизации позволяет длительно наблюдать за больными на фоне проведения регулярного полноценного обследования.
Таким образом, антихеликобактерная терапия правомочна и эффективна при первичных MALT-лимфомах желудка, но при обязательном строгом соблюдении показаний к ее использованию — I стадия процесса с небольшим локализованным поражением слизистого и подслизистого слоев при H. pylori-позитивных опухолях. Обязательным является динамическое исследование опухолевого субстрата на наличие H. pylori, эрадикация которого необходима для реализации противоопухолевого эффекта. Отсутствие эрадикации H. pylori требует использования химиотерапии с повторными курсами антибиотикотерапии.
Предраковые заболевания желудка
Облигатный предрак — заболевания, на почве которых всегда или в большинстве случаев, если их не лечить, возникает рак. К таким заболеваниям относят каллезную язву желудка, ригидный антральный гастрит, полипы, полипоз желудка.
факультативный предрак — хронические заболевания желудка, при которых рак развивается относительно редко, но чаще, чем У здоровых людей. Это хронический атрофический гастрит, болезнь оперированного желудка, пернициозная анемия, болезнь Менетрие и др.
Национальный раковый конгресс в Японии трактует ряд заболеваний, на фоне которых может возникнуть рак желудка, как фоновые, объединяя в одну группу облигатный и факультативный предрак.
По данным Национального ракового конгресса, рак желудка может развиться на фоне хронического атрофического гастрита в 0-13% случаев, пернициозной анемии — в 0,5-12,3%, хронической язвы желудка — в 1-2%, гиперпластического полипа — в 1-2%, плоской аденомы — в 6-21%, папилловирусной аденомы — в 20-75%, болезни Менетрие — в 5-10%, резекции желудка в анамнезе — в 0,4-7,8% случаев.
С морфологической точки зрения мультицентрически расположенные участки пролиферации атипического эпителия называются дисплазией.
Дисплазия — это нарушение структуры ткани, характеризующееся патологической пролиферацией и атипией эпителия. В слизистой оболочке желудка дисплазия может быть трех степеней (легкая, умеренная и тяжелая).
При дисплазии I и II степени изменения слабо выражены и носят обратимый характер. Изменения же, относящиеся к дисплазии III степени, постоянны и могут рассматриваться как рак in situ. У 40-45% людей в возрасте старше 60 лет в слизистой оболочке желудка происходит перестройка эпителия по кишечному типу — кишечная метаплазия (тонкокишечная, толстокишечная). Толстокишечная метаплазия трактуется как предраковое состояние.
Хронический гастрит — самое распространенное заболевание среди патологии желудочно-кишечного тракта, которое составляет 35% всех болезней органов пищеварения и 85% болезней желудка.
Хронический гастрит — заболевание полиэтиологическое. Существует много причин, вызывающих его, однако в соответствии с этиопатогенезом их можно объединить в три основные группы:
•I группа — инфекционные (экзогенные), связанные с желудочным хеликобактером (гастрит В — бактериальный);
•II группа — эндогенные аутоиммунные, обусловленные образованием антител к обкладочным клеткам желез желудка (гастрит А — аутоиммунный) — атрофический гастрит;
•III группа — экзоэндогенные, связанные с частичными термическими раздражениями, медикаментозными воздействиями выражаются гастродуоденальным рефлюксом (гастрит С — реактивный или химический).
На фоне хронического атрофического гастрита в 0-13% случаев возникает рак желудка.
Клиника. В клинической картине хронического гастрита нет типичных характерных признаков, на основании которых можно было бы распознать те или иные его формы.
Основные жалобы: нарушение аппетита, неприятные ощущения в эпигастральной области, связанные с приемом пищи отрыжка, изжога, тошнота, иногда рвота.
Синдромы желудочной и кишечной диспепсии могут быть в самых различных сочетаниях (чувство переполнения желудка пищей, метеоризм, урчание в животе, тенезмы, запоры, сменяющиеся поносами).
Диагностика. Рентгенологический метод исследования в диагностике хронического гастрита играет относительную роль. Он больше пригоден для выявления язвенного, полипозного и опухолевого поражения желудка. Исключение составляет ригидный антральный гастрит. Решающее значение в распознавании различных форм хронического гастрита принадлежит гастрофиброскопии и гастробиопсии. Диагноз: кишечная метаплазия, дисплазия разной степени выраженности, инфекция, вызванная Helicobacter pylori (HP), — только цитологический и гистологический.
Лечение. К терапевтическим мероприятиям при хроническом гастрите неинфекционной этиологии относятся: устранение основных факторов, способствующих развитию заболевания или поддерживающих его, диетотерапия, седативные средства в период обострений, средства, улучшающие микроциркуляцию и трофику слизистой оболочки, витаминотерапия, санаторно-курортное лечение.
Особого отношения требует инфекционный гастрит, вызванный микроорганизмами Helicobacter pylori. На сегодняшний день учеными мира доказано, что 30-50% населения земного шара — носители HP-инфекции (больной человек или бактерионоситель). HP-бактерии обычно размножаются под слоем слизи над слизистой оболочкой привратника, прикрепляются к апикальной части клеток эпителия, выделяют энзимы — цитотоксины и уреазу, и в эпителии развиваются отек, гиперемия, нарушение трофики, дегенерация клеток слизистой оболочки. Процессы воспаления и атрофии тесно связаны между собой и имеют инфекционно-иммунное происхождение.
В последние 10 лет многих исследователей интересуют проблемы хеликобактериоза и рака желудка. На сегодняшний день доказано, что Helicobacter pylori вырабатывается множество патогенных ферментов и токсинов, некоторые из них могут быть вовлечены в канцерогенез.
•Показана взаимосвязь между наличием HP-инфекции и кишечной метаплазией, разновидность которой — неполная кишечная метаплазия — считается предраковым состоянием.
•Установлено, что HP с помощью энзима экстрацеллюлярной уреазы расщепляет мочевину с образованием аммиака, активизирует процессы перекисного окисления липидов, повышает концентрацию свободных радикалов — производных кислорода, что стимулирует процессы канцерогенеза.
•В экспериментах in vitro показана способность HP стимулировать рост культуры опухолевых клеток.
Рак желудка в большинстве случаев сопровождается инфицированием слизистой оболочки HP; при этом НР-инфекция имеет большую распространенность, чем при язвенной болезни, приобретает характер тотального обсеменения всех отделов желудка, в том числе и самой опухоли.
Хеликобактерный гастрит (гастрит В) требует особого лечения. Чтобы уничтожить эти бактерии, необходимо обязательное применение трех препаратов, обладающих антибактериальной активностью: амоксициллина или ампициллина, производного нитронидазола (метронидазола) и производного нитрофурина (фуразолидона). Базисный препарат — де-нол (соль лимонной кислоты с висмутом).
Язва желудка. Малигнизация рецидивирующих и каллезных язв желудка отмечается у 2-10% больных.
Клиника. В отличие от хронического гастрита хроническая язва желудка имеет довольно четкую клиническую картину.
Наиболее постоянный симптом язвенной болезни — боль, связанная с приемом пищи. Боли могут быть ранними, возникающими либо сразу после приема пищи, либо через 0,5-1 ч, и поздними, наступающими через 2-3 ч после приема пищи и позднее. Иногда боли возникают ночью и проходят после приема пищи (молока).
Для язвенной болезни желудка характерна также сезонность — обострения в осенне-зимние и весенние месяцы, ремиссии в летний период.
Важным симптомом заболевания является изжога; у большей половины больных бывает рвота, тошнота. В рвотных массах — кислая жидкость с примесью пищи. При рубцовых стенозах привратника рвота становится более частой, при этом рвотные массы обильны, с остатками пищи, съеденной накануне. Нередко отмечаются нарушения функции кишечника — запоры часто сменяются поносами.
Диагностика. В распознавании язвенной болезни желудка, кроме клинической семиотики, определенную роль играет исследование желудочного сока. У большинства больных имеет место повышение секреции и кислотообразования. Лишь при длительном течении заболевания, особенно при каллезных язвах, кислотность желудочного сока понижается. Важно также исследование кала на скрытую кровь.
При рентгенологическом исследовании желудка главным симптомом является ниша. Большая ниша с окружающим валом и конвергенцией складок слизистой оболочки указывает обычно на каллезный характер язвы. Отличить доброкачественную язву желудка от злокачественной помогает эндоскопическое, цитологическое исследование, а также множественная биопсия с разных участков язвы.
Лечение. Острые и рецидивирующие язвы в стадии обострения лечатся, как правило, консервативным путем. Обычно для заживления язвы требуется от 4 до 8 нед, а при больших или застарелых язвах — и более длительный промежуток времени. Эндоскопический или рентгеноскопический контроль проводится через 8 нед и до полного заживления. Если полное заживление не наступает, проводится повторная биопсия.
При осложнениях язвы (пенетрация, перфорация, рубцовый стеноз, повторяющиеся кровотечения), отсутствии эффекта от консервативной терапии, частом рецидивировании неосложненной пептической язвы, лишающем больного трудоспособности, подозрении на злокачественную язву желудка показано хирургическое лечение.
Полипы и полипоз желудка. Полипы бывают гиперпластическими и аденоматозными.
Гиперпластические изменения встречаются в 80-90% случаев всех полипозных образований в желудке и относятся к опухолеподобным поражениям. В 10-20% случаев возникают аденоматозные полипы — доброкачественные эпителиальные опухоли. Обычно они имеют вид выступающих в просвет желудка округлых образований, расположенных на тонкой ножке или широком основании.
К числу предраковых относят железистые аденоматозные полипы. Дисплазия разной степени выраженности в аденоматозных полипах отмечается в 40-60% случаев, а дисплазия III степени — в 5-10%. Если гиперпластические полипы перерождаются в рак в 1-2% случаев, то плоская аденома — в 6-21%, а папилловирусная аденома — в 20-75% случаев;
Клиника. Одиночные полипы могут протекать бессимптомно и быть случайной находкой. Клинически они проявляются, как правило, при сопутствующем хроническом гастрите. При распаде опухоли возможны кровотечения, при ущемлении полипа — приступ боли в эпигастрии, тошнота, рвота.
Диагностика. Ведущая роль в распознавании полипоза и полипов желудка принадлежит рентгенологическому и гастроскопическому методам.
Биопсия при эндоскопии позволяет дать цитологическую и морфологическую характеристику полипов.
Лечение. Аденоматозные полипы лечат хирургически. При одиночных полипах возможна эндоскопическая полипэктомия, при множественных — выполняется резекция желудка или гастрэктомия.
Оперированные больные находятся под диспансерным наблюдением. Не реже одного раза в 6 мес проводится эндоскопическое исследование, также периодически комплексное лечение, включающее рациональную диету, витаминотерапию, седативные средства, санаторно-курортное лечение.
Пернициозная анемия (болезнь Аддисона) может быть определена как отсутствие внутреннего фактора Касла, связанное с полной атрофией слизистой оболочки фундального отдела желудка и потерей париетальных клеток. Болезнь диагностируется, когда отмечается полная атрофия слизистой оболочки фундального отдела желудка, как правило, это бывает после 50 лет. На момент обнаружения болезни воспаление в слизистой оболочке отсутствует, т. е. патологический процесс представляет собой атрофию без гастрита.
Некоторые данные указывают на иммунологическую и наследственную основу пернициозной анемии, называемой также гастритом типа А.
При этой болезни в 90% случаев в организме присутствуют антитела к париетальным клеткам желудка; а в 60% случаев — антитела к внутреннему фактору Касла (как блокирующие, так и связывающие его). Анемия обычно развивается постепенно и незаметно, прогрессируя по мере истощения запасов витамина В в печени.
Рак желудка при пернициозной анемии встречается в 0,5-12,5% случаев.
Больные с пернициозной анемией обычно наблюдаются у терапевта и гематолога. Для больных старше 50 лет обязательно эндоскопическое исследование желудка 1 раз в год.
Болезнь Менетрие — поражение желудка неизвестной этиологии, проявляющееся очень большими желудочными складками, большими железами с незначительным их воспалением и кистозным расширением; при этом изредка затрагивается подслизистый слой; часто процесс ограничивается телом и дном желудка (антральный отдел обычно не поражается). Иногда ширина и высота складок достигает 3,5 см. Характерно повышенное слизеобразование, гипосекреция соляной кислоты и пепсина, Уменьшение содержания сывороточных белков, приводящее к появлению гипоальбумических отеков.
Клиника. Характерны боль в эпигастрии, потеря массы тела, тошнота.
Течение заболевания хроническое (ремиссии, обострения), иногда наступает спонтанное выздоровление либо переход в атрофический гастрит.
Болезнь Менетрие, как правило, встречается в возрасте 30-60 лет.
Диагностика. При рентгенологическом и эндоскопическом исследовании выявляются очень крупные складки, которые никогда не переходят на пилорический отдел (показана биопсия на всю толщину складки). В 5-10% случаев развивается рак желудка.
Лечение — консервативное; в случае тяжелой гипоальбуминемии может быть необходимой резекция желудка.
Атрофический гастрит резецированного желудка. Закономерным исходом резекции желудка является развитие хронического гастрита в культе, который сопровождается дисплазией и кишечной метаплазией эпителия вследствие снижения кислотности желудочного сока и заброса желчи в культю желудка.
Рак культи желудка возникает у 0,4-7,8% больных из числа оперированных по поводу неопухолевых заболеваний желудка через 10, 15, 20 лет после операции.
Пациенты с резецированным желудком нуждаются в постоянном диспансерном наблюдении на протяжении всей жизни. Один раз в год им должно выполняться гастроскопическое обследование культи желудка.